Magnesiumbicarbonat, også kendt under dets IUPAC-navn magnesiumhydrogencarbonat, er et salt indeholdende bicarbonatanion og magnesiumkation repræsenteret ved formlen C2H2MgO6 eller Mg(HCO3)2 . Da magnesiumbicarbonat er ustabilt i fast tilstand, findes det i en fortyndet vandig opløsning .
identifikation af Magnesiumbicarbonat |
|
| CAS-nummer | 2090-64-4 |
| PubChem CID | 102204 |
| ChemSpider ID | 92335 |
| EF-nummer | 235-192-7 (EU-midler til forbedring af fødevarer)
218-240-1 (ECHA) |
| UNII | 19E9A0647O |
| InChI nøgle | |
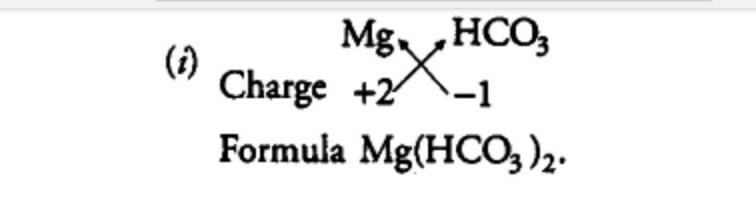
Magnesiumbicarbonatformel
hvordan fremstilles Magnesiumbicarbonat
det kan syntetiseres ved behandling af magnesiumacetat med natriumbicarbonat, der involverer følgende reaktion:
Mg(CH3COO) 2 + 2nahco3 liter Mg (HCO3) 2 + 2CH3COONa
en opløsning af Mg (HCO3) 2, der almindeligvis kaldes magnesiumbicarbonatvand, kan produceres gennem reaktionen af magnesiumhydroksid (såsom mælk af magnesia) og kulsyre under tryk (som seltservand) :
Mg(OH)2 + 2CO2 liter Mg (HCO3) 2
den resulterende opløsning, når den tørres, nedbrydes magnesiumbicarbonat til magnesiumcarbonat, vand og kulsyre:
Mg + 2hco3 liter MgCO3 + CO2 + H2O

Magnesiumbicarbonat
egenskaber og egenskaber ved Magnesiumbicarbonat
generelle egenskaber |
|
| molær masse / molekylvægt | 146.337 g / mol |
fysiske egenskaber |
|
| farve og udseende | lys, hvid, ustabil sprød masse eller pulver |
| lugt | lugtfri |
| smeltepunkt | Ikke relevant |
| kogepunkt | 333, 6 liter C, 632.48 kr f |
| opladning | 0 (Mg2 + og HCO3–) |
| stoftilstand ved stuetemperatur | ustabil i fast form, men findes i flydende tilstand |
| opløselighed | uopløselig i ethanol |
| opløselighed i vand | næsten uopløseligt i vand (0, 077 g pr. 100 mL) |
anvendelser
- Magnesiumbicarbonat har adskillige sundhedsmæssige fordele og bruges til at modstå ændringer i blodets pH og holde det inden for et optimalt interval .
- som et essentielt mineral hjælper det med blodtryksregulering, proteinsyntese, nerve-og muskelfunktioner og blodglukosekontrol i den menneskelige krop .
- det bruges som fødevaretilsætningsstoffer som surhedsregulatorer, alkali, anti-krakning og blegemidler .
- kulsyre, magnesiumsalt (2: 1) – Pubchem.ncbi.nlm.nih.gov
- Magnesiumbicarbonat-Mg (HCO3) 2 – Byjus.com
- Magnesiumbicarbonat – Chemspider.com
- fremstilling af opløsninger af Magnesiumbicarbonat til Afsyring – Jstor.org
- Magnesiumbicarbonatvand – betydningen af bicarbonater og magnesium – Dancingwithwater.com
- surhedsregulatorer – Chm.bris.ac.uk