Magnesiumbicarbonat, auch bekannt unter dem IUPAC-Namen Magnesiumhydrogencarbonat, ist ein Salz, das Bicarbonatanion und Magnesiumkation enthält, dargestellt durch die Formel C2H2MgO6 oder Mg(HCO3)2 . Da Magnesiumbicarbonat in festem Zustand instabil ist, liegt es in einer verdünnten wässrigen Lösung vor .
Magnesiumbicarbonat Identifizierung |
|
| CAS-Nummer | 2090-64-4 |
| PubChem CID | 102204 |
| ChemSpider ID | 92335 |
| EG-Nummer | 235-192-7 (EU-Lebensmittelverbesserungsmittel)
218-240-1 (ECHA) |
| UNII | 19E9A0647O |
| InChI Schlüssel | QWDJLDTYWNBUKE-UHFFFAOYSA-L |
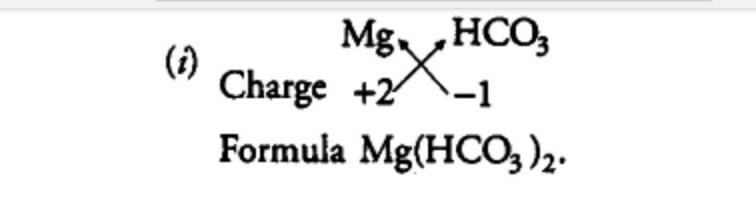
Magnesiumbicarbonat-Formel
Wie wird Magnesiumbicarbonat hergestellt
Es kann synthetisiert werden, indem Magnesiumacetat mit Natriumbicarbonat behandelt wird, wobei die folgende Reaktion durchgeführt wird:
Mg (CH3COO) 2 + 2NaHCO3 → Mg (HCO3) 2 + 2CH3CO3
Eine Lösung von Mg (HCO3) 2, die allgemein als Magnesiumbicarbonatwasser bezeichnet wird, kann durch die Reaktion von Magnesiumhydroxid (wie Magnesiummilch) und unter Druck stehendem Kohlendioxid (wie Selterwasser) hergestellt werden :
Mg (OH)2 + 2CO2 → Mg(HCO3)2
Die resultierende Lösung zersetzt nach dem Trocknen Magnesiumbicarbonat in Magnesiumcarbonat, Wasser und Kohlendioxid:
Mg + 2HCO3 → MgCO3 + CO2 + H2O

Magnesiumbicarbonat
Eigenschaften und Eigenschaften von Magnesiumbicarbonat
Allgemeine Eigenschaften |
|
| Molmasse/Molekulargewicht | 146.337 g/mol |
Physikalische Eigenschaften |
|
| Farbe und Aussehen | Leichte, weiße, instabile bröckelige Masse oder Pulver |
| Geruch | Geruchlos |
| Schmelzpunkt | N/A |
| Siedepunkt | 333,6 °C, 632.48 ° Fahrenheit |
| Ladung | 0 (Mg2+ und HCO3–) |
| Materiezustand bei Raumtemperatur | In fester Form instabil, aber im flüssigen Zustand vorhanden |
| Löslichkeit | Unlöslich in Ethanol |
| Löslichkeit in Wasser | Fast unlöslich in wasser (0,077 g pro 100 ml) |
Verwendet
- Magnesiumbicarbonat hat zahlreiche gesundheitliche Vorteile und wird verwendet, um Veränderungen des Blut-pH-Werts zu widerstehen und ihn in einem optimalen Bereich zu halten .
- Als essentielles Mineral hilft es bei der Blutdruckregulation, der Proteinsynthese, den Nerven- und Muskelfunktionen und der Blutzuckerkontrolle im menschlichen Körper .
- Es wird als Lebensmittelzusatzstoffe wie Säureregulatoren, Alkali, Anti-Cracking und Bleichmittel verwendet.
- Kohlensäure, Magnesiumsalz (2:1) – Pubchem.ncbi.nlm.nih.gov
- Magnesiumbicarbonat – Mg(HCO3)2 – Byjus.com
- Magnesiumbicarbonat – Chemspider.com
- Herstellung von Lösungen von Magnesiumbicarbonat zur Entsäuerung – Jstor.org
- Magnesiumbicarbonatwasser – Die Bedeutung von Bicarbonaten und Magnesium – Dancingwithwater.com
- Säureregulatoren – Chm.bris.ac.uk