Die übliche glatte Muskulatur ist normalerweise unkompliziert; Es ist gekennzeichnet durch ineinandergreifende Bündel einheitlicher spindelnder Zellen mit langen ovalen Kernen mit abgestumpften Enden und sich verjüngenden bipolaren zytoplasmatischen Prozessen. Aufgrund der faszikulären Anordnungen erscheinen die Kerne im Querschnitt klein und rund, im Längsschnitt lang und oval (siehe folgende Abbildung).
 Normale Faszikel der glatten Muskulatur.
Normale Faszikel der glatten Muskulatur. Leiomyome weisen gelegentlich kleine, aber auffällige Nukleolen und leichte Unregelmäßigkeiten der Kerngrenze auf. Gelegentlich weist ein Leiomyom hamartomatöse Komponenten wie Fett, Knorpel und Knochen auf; Solche Tumoren werden entsprechend den Komponentenmerkmalen (z. B. Lipoleiomyom, chondroides Leiomyom) benannt und haben keinen Einfluss auf das maligne Potenzial.
In seltenen Fällen erscheinen die glatten Muskelzellen basaloid und weniger faszikulär und ähneln Endometriumstroma, was die Möglichkeit eines Stromaknotens oder, von klinischer Bedeutung, eines endometrialen Stromasarkoms erhöht. In solchen Fällen umfassen histologische Hinweise darauf, dass das Neoplasma eine glatte Muskulatur ist, faszikuläres Wachstum und großkalibrige Gefäße. Die Differenzierung durch Immunhistochemie kann hilfreich sein, ist aber leider nicht immer aufschlussreich (siehe Immunhistochemie). Die Beurteilung der infiltrativen Grenzen, die für das endometriale Stromasarkom charakteristisch sind, ist hilfreich.
Obwohl gutartig, können Leiomyome extrem groß werden (20-30 cm). Obwohl ein solcher Tumor im Weichgewebe definitionsgemäß als Malignität angesehen würde, gilt dies nicht für Tumoren, die im Uterus auftreten. Aufgrund hormoneller Einflüsse können Leiomyome sehr hypertroph und mitotisch aktiv sein.
Es kommt häufig vor, dass Infarkte auftreten. Diese sind in der Regel leicht an der Narbenbildung entlang der Peripherie des Infarkts zu erkennen (klassifiziert als hyaline Nekrose) (siehe Bild unten). Zusätzlich sind bei einem Infarkt die glatte Muskulatur und die Gefäße nekrotisch.
 Hyalinisierte Nekrose gekennzeichnet durch Narbenbildung.
Hyalinisierte Nekrose gekennzeichnet durch Narbenbildung. Nach einem Infarkt erfährt das Leiomyom manchmal hydropische Veränderungen. Die gelöste Matrix wird ödematös und verleiht der Läsion ein myxoides Aussehen. Ein Hinweis auf hydropische Veränderungen ist das Vorhandensein großer Gefäße, die im leeren Raum schweben, wobei die glatten Muskelzellen an die Peripherie gedrückt werden. Reaktive Atypien und erhöhte Mitosen werden häufig neben einem Infarktbereich beobachtet; daher sollte die zytologische Atypie außerhalb von Nekrose- oder Infarktregionen beurteilt werden.
Leiomyosarkome sind selten und in der Regel leicht zu diagnostizieren. Die Bewertung der folgenden 3 Merkmale ist weiterhin das zuverlässigste Mittel zur Beurteilung der Malignität: mitotische Aktivität, Tumorzellnekrose und zytologische Atypie. Angesichts der Bedeutung dieser Merkmale wird jedes im Folgenden erörtert.
Mitotische Aktivität
Der mitotische Index ist an sich kein unabhängiger Prädiktor für Malignität. Mitotisch aktive Leiomyome sind gut untersucht und berichtet. Diese sind definiert als glatte Muskeltumoren mit bis zu 20 Mitosen / 10 Hochleistungsfeldern (HPF), aber sie sind frei von Atypien und Tumorzellnekrosen. Obwohl dieses Merkmal allein keine Malignität bezeichnet, wird die mitotische Aktivität bei der Beurteilung des malignen Potenzials äußerst wichtig, wenn andere besorgniserregende Merkmale vorhanden sind.
Um den mitotischen Index zu messen, finden Sie den mitotisch aktivsten Bereich des Tumors (vermeiden Sie jedoch Bereiche neben hyalinisierter Nekrose) und zählen Sie 10 HPF (40 ×).
Apoptotische Körper, degenerierende glatte Muskelzellen und infiltrierende Lymphozyten können manchmal mitotische Zahlen simulieren; Daher sollten mitotische Zählungen nur definitive Mitosen umfassen. Wenn mehr als eine einzige atypische mitotische Figur gefunden wird, ist eine wachsame Beurteilung gerechtfertigt; Der Tumor sollte nicht kategorisch als gutartig eingestuft werden. Mehrere Diagnosen können in Betracht gezogen werden, einschließlich atypischer glatter Muskelneoplasmen, niedriggradiger glatter Muskelneoplasmen und Leiomyosarkomen.
Zytologische Atypie
Das angrenzende nicht-neoplastische Myometrium kann als interne Kontrolle für die Histologie der glatten Muskulatur zu Studienbeginn des Patienten verwendet werden. Typischerweise haben Leiomyome nur geringfügig größere Zellen und fokale Kernmembranunregelmäßigkeiten. Die zytologische Atypie wird durch Bestimmung der Kerngröße, Untersuchung der Membrankonturen und Bewertung der Prominenz und Anzahl der Nukleolen beurteilt (siehe Abbildung unten).
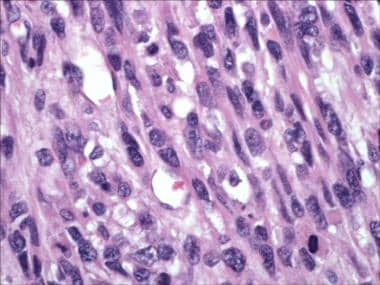 Leiomyosarkom mit ausgeprägter zytologischer Atypie.
Leiomyosarkom mit ausgeprägter zytologischer Atypie. Es ist allgemein bekannt, dass die fokale schwere zytologische Atypie in Ermangelung anderer Merkmale normalerweise gutartig ist (möglicherweise ähnlich einer Veränderung bei anderen Tumoren wie Schwannomen). Diese Tumoren wurden früher als symplastische Leiomyome bezeichnet und werden heute als Leiomyom mit Atypie klassifiziert (siehe folgende Abbildung). Diffuse schwere Atypien sind kein typisches Merkmal gutartiger Tumoren und sollten mit großer Sorgfalt beurteilt werden. In solchen Fällen hilft der mitotische Index bei der Klassifizierung des Tumors.
 Leiomyom mit Atypie (früher symplastisches Leiomyom genannt). Beachten Sie die fokale Natur der schweren Atypie. Definitionsgemäß sind Tumoren dieses Typs frei von Tumorzellnekrosen und Mitosen von mehr als 10 Mitosen pro 10 Hochleistungsfeld (HPF).
Leiomyom mit Atypie (früher symplastisches Leiomyom genannt). Beachten Sie die fokale Natur der schweren Atypie. Definitionsgemäß sind Tumoren dieses Typs frei von Tumorzellnekrosen und Mitosen von mehr als 10 Mitosen pro 10 Hochleistungsfeld (HPF). Koagulative Tumorzellnekrose
Von den 3 diskutierten Merkmalen scheint die koagulative Tumorzellnekrose das prädiktivste histologische Merkmal der Malignität zu sein. Das größte Problem besteht darin, es zu erkennen und nicht als Infarkt / hyalinisierte Nekrose einzustufen. Die koagulative Tumorzellnekrose ist durch eine abrupte Veränderung lebensfähiger Myozyten neben nekrotischen Myozyten ohne dazwischen liegende sklerotische Kante (die für Infarkte charakteristisch ist) gekennzeichnet (siehe folgende Abbildung). Einzelne nekrotische Tumorzellen (Geisterzellen) sind meist erkennbar, und die Gefäße sind meist noch lebensfähig.
 Leiomyom mit Atypie (früher symplastisches Leiomyom genannt). Beachten Sie die fokale Natur der schweren Atypie. Definitionsgemäß sind Tumoren dieses Typs frei von Tumorzellnekrosen und Mitosen von mehr als 10 Mitosen pro 10 Hochleistungsfeld (HPF).
Leiomyom mit Atypie (früher symplastisches Leiomyom genannt). Beachten Sie die fokale Natur der schweren Atypie. Definitionsgemäß sind Tumoren dieses Typs frei von Tumorzellnekrosen und Mitosen von mehr als 10 Mitosen pro 10 Hochleistungsfeld (HPF). Wenn es große Bereiche hyalinisierter Nekrose und einen fokalen Bereich gibt, der einer Tumorzellnekrose verdächtig ist, können die Spiegel manchmal helfen, eine sklerotische Kante zu identifizieren und jüngere Infarkte zu bestätigen. Wenn ein Myom vor der Operation embolisiert wurde, um Blutungen zu kontrollieren, ähneln die histologischen Merkmale der Tumorzellnekrose, obwohl die Gefäße in den Nekrosebereichen ebenfalls nekrotisch sind. Wenn es sich um eine Tumorzellnekrose handelt, kann eine zusätzliche Probenahme der myomatösen Masse zur Klärung der Art der Nekrose beitragen, entweder durch zusätzliche Herde von Tumorzellnekrosen oder andere für das Leiomyosarkom charakteristische Merkmale.
Der Begriff „glatter Muskeltumor mit ungewissem malignen Potenzial“ (STUMPF) wird manchmal auf Fälle angewendet, in denen unbestimmte Merkmale der Malignität oder eine Kombination von Merkmalen vorliegen, die ungewöhnlich sind und daher in der Literatur nicht ausführlich beschrieben werden. Dieser Begriff sollte für Fälle reserviert werden, in denen das maligne Potenzial wirklich unbekannt ist, und er sollte sparsam verwendet werden.
STUMPF ist im Wesentlichen eine Nichtdiagnose, und es ist voller Frustration für Kliniker und Patienten. Die meisten Studien über STUMPF berichten von gutartigen Ergebnissen, die wahrscheinlich die Tatsache widerspiegeln, dass der Begriff überbeansprucht wird. Wenn der Tumor Merkmale aufweist, die normalerweise gutartig sind, aber wenn seltene Rezidivfälle bekannt sind, kann der Begriff „niedriges wiederkehrendes Potenzial“ dem STUMPF vorzuziehen sein, da dieser Begriff mehr Informationen über das vorhergesagte und bekannte maligne Potenzial vermittelt.
Das benigne metastasierende Leiomyom ist ein mitotisch inaktiver, zytologisch milder, nicht nekrotischer Tumor, der sich auf Lunge und Lymphknoten ausbreitet. Es kann mit Resektion und Hormontherapie behandelt werden. Diese Tumoren haben ein ausgeprägtes zytogenetisches Profil. Da die Histologie des gutartigen metastasierenden Leiomyoms mit der von Leiomyomen identisch ist, wird die Diagnose immer retrospektiv gestellt (z. B. bei einer Frau, die Lungenknoten aufweist). Es gibt keine histologischen Merkmale, die bei der Vorhersage helfen, welche milden Uterus-Leiomyome „metastasieren“ werden.“
Intravaskuläre Leiomyomatose ist eine milde Proliferation der glatten Muskulatur innerhalb der Gefäßkanäle. Es kann fokal (mit vaskulärem Eindringen) oder multifokal und stark sichtbar sein. Die fokale vaskuläre Intrusion ist normalerweise selbstlimitiert. Gelegentlich tritt eine prominente vaskuläre Leiomyomatose in Becken- oder Bauchgefäßen auf; Selten erstreckt es sich in die Vena cava inferior und betrifft schließlich das Herz. Da Leiomyosarkome Blutgefäße betreffen können, ist der Begriff „intravaskuläre Leiomyomatose“ Tumoren vorbehalten, die keine verdächtigen histologischen Merkmale aufweisen (siehe Abbildung unten).
 Die vaskuläre Invasion des Leiomyosarkoms.
Die vaskuläre Invasion des Leiomyosarkoms. Myxoide uterine glatte Muskelneoplasmen (MUSMN) sind selten; Diese Tumoren wurden nur in wenigen kleinen Studien berichtet. Die histologischen Kriterien für die Vorhersage einer aggressiven myxoiden Läsion sind mit Schwierigkeiten behaftet, da myxoide Leiomyosarkome pauzizellulär und täuschend fad sein können. Ihre Histologie reicht von reichlich vorhandenem Myxoidstroma, das an ein Myxom erinnert (siehe erstes Bild unten), über ein Lungenödemmuster, bei dem die Tumorzellen dünne septenartige Alveolen aufweisen (wie im zweiten Bild unten gezeigt), bis hin zu einem klassischeren Erscheinungsbild der glatten Muskulatur ähnlich der Myxoidknotenfasziitis. Das Myxoidmuster scheint nicht mit dem malignen Potenzial zu korrelieren.
 Das Myxommuster von myxoiden glatten Muskeltumoren. Dieser Tumor hat nur minimale Atypien.
Das Myxommuster von myxoiden glatten Muskeltumoren. Dieser Tumor hat nur minimale Atypien.  Myxoides Leiomyom mit ausgeprägtem Lungenödemmuster.
Myxoides Leiomyom mit ausgeprägtem Lungenödemmuster. Einige gemeinsame Merkmale gutartiger Läsionen sind gut umschriebene Grenzen, milde Zytologie und im Wesentlichen keine mitotische Aktivität (weniger als 2 pro 10 HPF) (siehe folgendes Bild). Merkmale, die auf Malignität hindeuten, umfassen Tumorzellnekrose (unabhängig von anderen Merkmalen), infiltrative Grenzen (erkannt durch das benachbarte normale Myometrium, das durch das myxoide Stroma gespreizt und getrennt ist) und Mitosen von mehr als 2 pro 10 HPF. Aufgrund des Verdünnungseffekts des myxoiden Stromas befürworten einige Forscher das Zählen von 50 HPF, um eine bessere Darstellung des mitotischen Index zu erhalten.
 Mitotische Figur in einem myxoiden glatten Muskeltumor. Im Durchschnitt haben die meisten Leiomyosarkome mindestens 2 Mitosen pro 10 High Power Field (HPF) (oder mehr als 10 pro 50 HPF).
Mitotische Figur in einem myxoiden glatten Muskeltumor. Im Durchschnitt haben die meisten Leiomyosarkome mindestens 2 Mitosen pro 10 High Power Field (HPF) (oder mehr als 10 pro 50 HPF). Einige frühe Berichte über myxoide glatte Muskeltumoren ergaben, dass Tumore, die durch einen mitotischen Index von 0 pro 10 HPF, eine milde Zytologie und infiltrative Grenzen gekennzeichnet waren, mit schlechten Ergebnissen assoziiert waren. Obwohl diese Befunde bisher nicht reproduziert wurden, sollten sie wahrscheinlich mit Vorsicht diagnostiziert werden; Eine Stumpfkategorie kann am besten geeignet sein.
Ödeme können einem myxoiden Stroma ähneln und die Beurteilung eines Tumors der glatten Muskulatur beeinträchtigen. Ödeme infolge einer perinodulären hydropischen Degeneration können eine Schwellung des Leiomyoms verursachen (die Autoren haben eine mit einer Größe von 35 cm gesehen). Die hydropische Degeneration ist normalerweise durch Ödeme gekennzeichnet, die sich um die großen Gefäße konzentrieren. Dies führt zu einer Verlagerung normaler glatter Muskelzellen an die Peripherie des Ödems. Die Schiffe scheinen im freien Raum zu schweben. Normalerweise sind die Tumorzellen bei einem milden myxoiden glatten Muskeltumor klein, bei hydropischer Degeneration haben die Tumorzellen jedoch die Größe normaler glatter Muskelzellen.
Epitheloide uterine glatte Muskeltumoren sind durch polygonale Zellen mit zentral platzierten, runden Kernen gekennzeichnet. Häufig bildet sich eine azelluläre eosinophile Matrix um die Zellen herum, die ihr bei Betrachtung unter Scanvergrößerung ein knöchernes Aussehen verleiht. Diese Tumoren wurden unter zahlreichen Namen klassifiziert, einschließlich XYZ. Wie bei ihren myxoiden Cousins ist die Schwelle für die Klassifizierung von epitheloiden glatten Muskeltumoren als Leiomyosarkom niedriger als bei üblichen glatten Muskeltumoren (siehe die 2 Bilder unten).
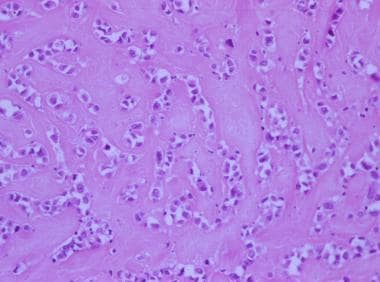 Markierte extrazelluläre Matrix in einem epitheloiden Leiomyom.
Markierte extrazelluläre Matrix in einem epitheloiden Leiomyom.  Zellulärer epitheloider glatter Muskeltumor.
Zellulärer epitheloider glatter Muskeltumor. Epitheloide glatte Muskeltumoren überlappen sich stark mit perivaskulären Epithelzelltumoren (PEComen). Pecome sind Tumoren unsicherer Differenzierung, die häufig im Rahmen von tuberöser Sklerose auftreten. Die glatten Muskelzellen des PEComs teilen den seltsamen Immunphänotyp von Angiomyolipom und Lymphangioleiomyomatose und weisen eine glatte Muskelaktin (SMA) -Positivität sowie eine perivaskuläre HMB 45-Positivität auf (siehe die 2 Bilder unten). Obwohl Uteruskarzinome auch bei tuberöser Sklerose auftreten können, handelt es sich bei den meisten um sporadische Fälle.
 Perivaskulärer Epithelzelltumor (PEComa), der die epitheloiden und klaren Zellmerkmale demonstriert.
Perivaskulärer Epithelzelltumor (PEComa), der die epitheloiden und klaren Zellmerkmale demonstriert.  HMB45 immunhistochemische Färbung eines perivaskulären Epithelzelltumors (PECOM), der eine fokale Immunreaktivität in der Nähe von Gefäßen zeigt.
HMB45 immunhistochemische Färbung eines perivaskulären Epithelzelltumors (PECOM), der eine fokale Immunreaktivität in der Nähe von Gefäßen zeigt. In 2 umfassenden Studien von Vang und Kempson und Folpe et al. Es wurden jedoch keine zuverlässigen Merkmale gefunden, um aggressives Potenzial vorherzusagen. Einige Autoren haben festgestellt, dass die Unterscheidung von Pecomen von epitheloiden glatten Muskeltumoren nicht notwendig ist, und die HMB45-Positivität kann bei ansonsten üblichen epitheloiden glatten Muskeltumoren beobachtet werden. Die Gene der tuberösen Sklerose regulieren jedoch den Rheb / mTOR / p70S6K-Signalweg, und selbst sporadische Fälle von Pecomen weisen erhöhte p70S6K-Spiegel auf. Dies ist ein potenzieller Bereich für eine gezielte Therapie wie Rapamycin, das mTOR hemmt. Obwohl die Nomenklatur keine Rolle spielt, könnte die genetische Beurteilung für mögliche Behandlungsmöglichkeiten kritischer werden.
Gelegentlich können epitheloide Leiomyosarkome infiltrativ sein und einen epitheloiden trophoblastischen Schwangerschaftstumor simulieren. Das prämenopausale Alter, die Ausdehnung der Zellen in den endozervikalen Kanal oder die Verteilung im gesamten Endometrium sind ungewöhnliche Muster für das Leiomyosarkom. Obwohl die Differentialdiagnose schwierig sein kann, ist die Unterscheidung mit der Immunhistochemie einfach.