En marzo de 2017, un mini simposio en el 11o Congreso de Controversias en Neurología (CONy), Atenas, Grecia, se dedicó a la enfermedad de neuro – Behçet (NBD). Una introducción a las características clínicas clave de la enfermedad de Behçet (EB) fue seguida de una revisión de sus manifestaciones neurológicas y una presentación enfocada de los desafíos del diagnóstico diferencial. Este examen representa un informe del mini simposio en forma de resumen actualizado de los temas que se presentaron. Sigue la estructura del mini simposio y, en parte, amplía la información presentada allí. Sin embargo, un examen sistemático está fuera del alcance del presente informe. La introducción general a BD será sucinta, ya que el foco de esta revisión es NBD. Los detalles de BD en general se pueden encontrar en revisiones recientes, por ejemplo, Yazici et al.1
Enfermedad de Behçet
Historia y epidemiología
La EC es una enfermedad crónica, multisistémica y polisintomática con exacerbaciones y remisiones impredecibles. Todos los sistemas pueden verse afectados de forma concomitante o consecutiva.1 Hay varios subconjuntos clínicos y hay variación geográfica que indica diferentes mecanismos de la enfermedad. En vista de esto, algunos autores prefieren usar el término síndrome de Behçet en lugar de enfermedad de Behçet. Con fines de coherencia y armonización, y para seguir la terminología de los debates del mini simposio, en esta revisión se utilizará el término Enfermedad de Behçet. En 1930, el oftalmólogo Adamantiades describió la coexistencia de lesiones oculares, cutáneas y mucosas en un paciente.2 En 1937, Hulusi Behçet identificó la EB en dos pacientes, que sufrían de úlceras orales y genitales, además de enfermedad ocular, y la describió como una enfermedad separada que se cree que es causada por un virus.3
Los estudios epidemiológicos han mostrado una amplia variabilidad en la prevalencia de EB dependiendo de los orígenes geográficos y étnicos de la población. La evidencia muestra que la prevalencia de BD es mayor en las áreas en las que la población tiene una alta incidencia de alelo HLA-B51.4 A menudo se le llama «enfermedad de la ruta de la seda» debido a su prevalencia relativamente alta en los países del Mediterráneo, Oriente Medio y Extremo Oriente a través de la antigua ruta comercial de la seda. Turquía tiene la prevalencia más alta, con 119,8 por 100.000.4
Fisiopatología
Los patomecanismos de la EB no se conocen por completo; sin embargo, puede verse como una afección asociada con respuestas autoinmunes, autoinflamación y lesión vascular. La susceptibilidad parece estar determinada por una interacción entre factores genéticos y ambientales. Entre los genes de susceptibilidad, se han implicado los de citocinas como la interleucina (IL)-17, IL-12, IL-23, IL-21, IL-23, factor de necrosis tumoral (TNF)-α, IL-1β e IL-8.5 La desregulación de estas citoquinas proinflamatorias puede reflejar una activación incontrolada del sistema inmunitario innato con o sin activación de las respuestas inmunitarias adaptativas que parecen ser responsables de las características patológicas. La producción elevada de citocinas proinflamatorias, como TNF-α, IL-1β e IL-8, da lugar a la activación de neutrófilos y al aumento de las interacciones celulares entre neutrófilos y células endoteliales.6 Estos neutrófilos activados producen superóxidos y enzimas lisosomales excesivos que causan lesiones en los tejidos. Las lesiones resultantes se caracterizan histológicamente por infiltrados angiocéntricos neutrófilos con vasculitis leucocitoclástica (temprana) o linfocítica (tardía) con o sin trombosis mural y necrosis.7 Además, se ha notificado que la función de los linfocitos B es anormal en algunos pacientes.8
Entre los factores ambientales responsables de la susceptibilidad a la EB, los agentes infecciosos que se han implicado con mayor frecuencia incluyen bacterias como el Estreptococo sanguíneo y los virus, principalmente los virus herpesvirus. De hecho, la interacción gen–ambiente en BD está indicada por estudios de genotipado densos que vinculan la respuesta inmune desregulada del huésped a antígenos bacterianos con la susceptibilidad a BD.9
manifestaciones Clínicas y diagnóstico
BD tiene una amplia gama de manifestaciones clínicas. Las úlceras orales suelen ser el primer síntoma; pueden aparecer años antes del diagnóstico y están presentes durante el curso de la enfermedad con una frecuencia de casi el 100%. En el 75% de los pacientes, se observan aftas anogenitales, principalmente en el escroto y el pene en los hombres y en la vulva en las mujeres. En alrededor del 60% de los pacientes, se han notificado varias lesiones cutáneas, que incluyen eritema nodoso, lesiones papulopustulares, pseudofoliculitis, pioderma gangrenoso y vasculitis cutánea.1,10
Además, muchas otras áreas se ven comúnmente afectadas por la EB. Las presentaciones oculares de BD ocurren en el 30-80% de los pacientes (predominantemente en hombres) y son una causa importante de morbilidad, ya que pueden resultar en ceguera, particularmente en el entorno de vasculitis retiniana.1 El compromiso de las articulaciones también se notifica con frecuencia en la EC. La mono / poliartritis en BD es cursiva, no erosiva y las articulaciones más afectadas son las rodillas, los tobillos, los pies y las manos cursivas. La afectación gastrointestinal se caracteriza por dolor, hemorragia, ulceraciones de la mucosa intestinal o perforación intestinal. También puede producirse afectación vascular en cursiva, con mayor frecuencia trombosis venosa periférica profunda/superficial y también enfermedad arterial aneurismática / oclusiva. La afectación cardíaca incluye arteritis coronaria, enfermedad vascular, trombos intracardiacos o trombosis de vasos colaterales venosos y vena cava superior, miocarditis y arritmias ventriculares recurrentes.1 La afectación neurológica también es una manifestación común de la EB, y se discutirá más a fondo en la siguiente sección.
Los criterios diagnósticos para la EC se publicaron hace 28 años.11 El criterio principal son las ulceraciones orales recurrentes (aftosas o herpetiformes) observadas por el médico o notificadas de forma fiable por el paciente al menos tres veces en un período de 12 meses. Además, se deben cumplir dos de los cuatro criterios menores:
- ulceración genital recurrente;
- lesiones oculares: uveítis anterior, uveítis posterior, células en el vítreo mediante examen con lámpara de hendidura o vasculitis retiniana observada por un oftalmólogo;
- lesiones cutáneas: eritema nodoso, pseudofoliculitis, lesiones papulopustulares o nódulos acneiformes en pacientes postadolescentes que no reciben corticosteroides; y
- una prueba patergológica positiva (prueba de pinchazo cutáneo): reactividad cutánea inespecífica del itálico en respuesta a reacciones menores de trauma leído por un médico a las 24-48 horas (>pústula de 2 mm, después de un pinchazo en la piel del antebrazo (profundidad de 5 mm) con aguja de 20-22 g).
Opciones de tratamiento
El objetivo del tratamiento con BD es suprimir rápidamente las exacerbaciones inflamatorias y las recidivas para prevenir el daño irreversible a los órganos y es necesario un enfoque multidisciplinario. El manejo de la EB depende de si hay manifestaciones autolimitadas o afectación grave de órganos, y debe individualizarse según la edad, el sexo y el tipo.12,13 En caso de enfermedad sistémica grave, se pueden elegir corticosteroides de pulso intravenoso seguidos de dosis orales diarias, azatioprina, ciclofosfamida, ciclosporina-A, metotrexato, micofenolato mofetilo, tacrolimus, inhibidores de interferón (IFN)-α o TNF-α (etanercept, infliximab).Se ha estudiado un nuevo inhibidor oral de la fosfodiesterasa-4, apremilast, en pacientes sin afectación importante de órganos y se ha demostrado una respuesta completa en un número significativamente mayor de pacientes.14
Otros tratamientos tienen como objetivo controlar los síntomas específicos de la EB. Los inhibidores del TNF-α son muy eficaces en la EB, especialmente en la afectación ocular.La administración a largo plazo del inhibidor de TNF-α infliximab puede reducir la frecuencia de recidivas oculares, incluso en casos resistentes. Como tratamiento de primera línea, infliximab se debe iniciar junto con un fármaco inmunosupresor (azatioprina, corticosteroides o itálico, metotrexato) y, en caso de remisión, se deben reducir los corticosteroides concomitantes. Muchos estudios han demostrado la eficacia de infliximab en la BD.15-17 En pacientes con afectación ocular del segmento posterior, se debe iniciar el tratamiento con azatioprina, ciclosporina-A, IFN-α o anti-TNF-α, a menudo combinados con corticosteroides sistémicos. En pacientes con afectación ocular del segmento posterior, se debe iniciar el tratamiento con azatioprina, ciclosporina-A, IFN-α o anti-TNF-α, a menudo combinados con corticosteroides sistémicos.12,13
Para el tratamiento de la enfermedad de los vasos mayores con episodios trombóticos en el DO, se recomiendan corticosteroides e inmunosupresores como azatioprina, ciclofosfamida o ciclosporina-A12,y en cursiva se podría considerar el anti-TNF-α en pacientes refractarios. Se consideran anticoagulantes cuando el riesgo de sangrado, en general, es bajo y se descartan aneurismas de arteria pulmonar coexistentes.Para los síntomas gastrointestinales, se pueden utilizar derivados del ácido 5-aminosalicílico, incluyendo sulfasalazina o mesalamina, corticosteroides sistémicos, azatioprina, anti-TNF-α y talidomida. La afectación del sistema nervioso central, incluidos los ataques agudos de afectación del parénquima cerebral, se tratan con dosis altas de corticosteroides seguidas de disminución gradual, junto con inmunosupresores. La ciclosporina, aunque barata, debe evitarse debido al riesgo de neurotoxicidad. El anti-TNF-α debe considerarse en enfermedad grave o refractaria como primera línea en cursiva. El primer episodio de trombosis venosa cerebral (TVC) debe tratarse con dosis altas de corticosteroides, seguido de una reducción gradual. Se pueden agregar anticoagulantes durante un corto período de tiempo.
Afectación neurológica en la enfermedad de Behçet
Al igual que con la enfermedad sistémica, las manifestaciones neurológicas de la EB son variadas.18-22 La afectación neurológica en el BD se puede clasificar como; 1) primaria, en la que la afectación neurológica se debe directamente a la BD y se denomina NBD o síndrome de neuro-Behçet (NBS); y 2) secundaria, en la que las manifestaciones neurológicas son el resultado de complicaciones neurológicas secundarias a la afectación sistémica del BD (p. ej. embolia cerebral por complicaciones cardíacas de la EB, aumento de la presión intracraneal secundario al síndrome de vena cava superior) o debido a las terapias utilizadas para las manifestaciones sistémicas de la EB (es decir, neurotoxicidad del sistema nervioso central con ciclosporina; neuropatía periférica secundaria a talidomida o colchicina). Estas son causas indirectas de problemas neurológicos en pacientes con BD y no se denominan NBD.
La afectación neurológica primaria con NBD ocurre en hasta el 10% de todos los pacientes.18-22 NBD normalmente se presenta dentro de la cuarta década y aproximadamente 5 años después del inicio de la enfermedad sistémica. Aunque algunos pacientes pueden presentar afectación neurológica sin cumplir los criterios de clasificación del Grupo de Estudio Internacional (ISG) para la EC11,por lo general no se puede hacer un diagnóstico de ECB a menos que haya al menos antecedentes o secuelas de algunas de las manifestaciones sistémicas de la EC. Aunque la EB se observa casi por igual en ambos sexos, la EB es más común en los hombres (3:1).23 BD y NBD son raros en la población pediátrica; sin embargo, cuando se produce compromiso neurológico en niños, a menudo es poco después de la aparición de la enfermedad sistémica.20.21
Los hallazgos clínicos y de neuroimagen indican que hay dos formas principales de NBD: 1) Enfermedad inflamatoria del parénquima del SNC (p-NBD); y, con menos frecuencia, 2) una forma extra parenquimatosa (ep-NBD) que involucra estructuras vasculares extra parenquimatosas grandes, principalmente senos durales venosos, que causan trombosis del seno venoso cerebral (CVST). En contraste con la p-NBD, TSVC es más comúnmente observadas en pacientes pediátricos con NBD y estos dos tipos de participación que se producen muy rara vez en el mismo individuo y, por lo tanto, pueden tener diferentes pathogeneses. En raras ocasiones, una meningitis aséptica puede ser la presentación de NBD extra parenquimatoso. Se pueden observar síntomas psicóticos y de comportamiento, que se denominan «neuro-psico-Behçet», durante el curso de NBD. También es probable que las funciones cognitivas se vean afectadas en un subgrupo de pacientes con EB y la disfunción frontal (ejecutiva) es el patrón más común observado. Se ha notificado compromiso primario del sistema nervioso periférico en la EB, pero es extremadamente raro.18,19
El síntoma neurológico más común visto en NBD es el dolor de cabeza, que se produce tanto en el parénquima (p-NBD) y extra-parénquima NBD (ep-NBD, TSVC). Sin embargo, la cefalea también puede ser un síntoma de inflamación ocular grave; puede estar asociada con exacerbaciones de los síntomas sistémicos de la EB, con algunas características similares a la migraña, y se conoce como «cefalea no estructural de la EB»; o puede ser independiente de la EB y coexistir como cefalea primaria en tasas similares a las de la población general. Otros síntomas frecuentes son debilidad (hemiparesia), trastornos de la marcha (ataxia), dificultades del habla (disartria) y, con menos frecuencia, cambios cognitivos y de comportamiento. La pérdida visual debido a la neuritis óptica, los síntomas sensoriales y extrapiramidales y las convulsiones son raros.18-22
Se sugiere el uso de los criterios de la Recomendación de Consenso Internacional (RCI) en el diagnóstico de la NBD.24 Estos criterios pueden resumirse como » la aparición de síntomas y signos neurológicos en un paciente que cumple los Criterios de Diagnóstico ISG para la EB que no se explican de otro modo por ninguna otra enfermedad o tratamiento sistémico o neurológico conocido y en el que se detectan anomalías objetivas compatibles con la EB en exámenes neurológicos, estudios de neuroimagen, RMN o exámenes anormales del líquido cefalorraquídeo (LCR)».24 Los criterios ICR también incluyen un criterio de «probable NBD», pero uno debe ser más prudente al hacer un diagnóstico de este tipo.
Enfermedad parenquimatosa de neuro-Behçet
Aproximadamente el 75-80% de los pacientes con NBD presentan compromiso parenquimatoso. Los principales síntomas y signos de p-NBS incluyen dolor de cabeza, disartria, ataxia, hemiparesia y neuropatías craneales (principalmente afectación de los nervios motor-oculares y faciales) y estos generalmente se desarrollan de manera subaguda. p-NBD es una de las principales causas de morbilidad y mortalidad en NBD. De manera similar a la esclerosis múltiple (EM), el curso clínico de la p-NBD puede permanecer con un solo ataque, puede tener una forma recidivante o puede ser progresivo. Sin embargo, los pacientes con p-NBD generalmente se quedan con déficits neurológicos. Las lesiones de las lesiones p-NBD comúnmente involucran la unión telencefálica / diencefálica y el tronco encefálico, que generalmente son grandes, sin bordes distintivos. En la fase aguda, es probable que estas lesiones se intensifiquen y, por lo general, aparezcan en un patrón heterogéneo. Se pueden observar lesiones cerebrales tumefactivas, y las lesiones de la médula espinal, aunque no son comunes, cuando se producen, es probable que sean extensas longitudinalmente. En estos pacientes, los anticuerpos anti-MOG y AQP4 suelen estar ausentes. El compromiso focal cerebeloso es poco frecuente, pero se ha notificado atrofia cerebelosa aislada.25 Las lesiones en los territorios arteriales principales intraparenquimatosos son inusuales y se han notificado casos de compromiso de arterias extraparenquimatosas grandes o intraparenquimatosas más pequeñas, aunque en casos extremadamente raros, lo que indica que puede existir un subgrupo de d-NBD arterial.26 Con base en los hallazgos radiológicos e histopatológicos, una patogénesis venosa es la explicación probable de las lesiones del SNB-p.17-19, 26
Los hallazgos en el LCR pueden revelar una pleocitosis prominente y un nivel de proteína elevado durante el episodio agudo de p-NBD. El predominio neutrófilo es típico durante la fase aguda, pero esto más tarde es reemplazado por una forma linfocítica. Las bandas oligoclonales rara vez se detectan.
Enfermedad extraparenquimatosa de neuro-Behçet / trombosis del seno venoso cerebral
Hasta el 20% de los pacientes con NBD tienen TSVC. Estos pacientes presentan dolor de cabeza intenso, que generalmente se desarrolla en unas pocas semanas. Por lo general, el examen fundoscópico y neurológico muestra papiledema y ocasionalmente parálisis del sexto nervio. En comparación con otras causas de trombosis del seno dural, la alteración de la conciencia, los déficits neurológicos focales, como la hemiparesia y las crisis epilépticas, son poco frecuentes en NBD extraparenquimatoso, y los infartos venosos son poco probables. Una venografía por resonancia magnética confirmará el diagnóstico y mostrará la extensión de la TSVC. Con la excepción de una presión de apertura elevada, los hallazgos de LCR son generalmente normales, excepto en la presentación meningítica rara, donde se puede encontrar un gran número de neutrófilos. Como ya se mencionó, esta forma de NBD ocurre con más frecuencia en la población pediátrica, lo que sugiere que la edad puede influir en la forma de afectación neurológica.
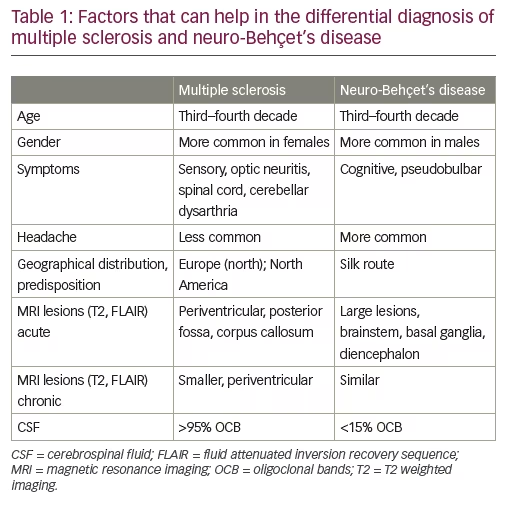
Diagnóstico diferencial de enfermedad de Neuro-Behçet
El diagnóstico diferencial de NBD sigue siendo un desafío importante. Particularmente difíciles son las situaciones en las que un paciente sin BD completo presenta manifestaciones neurológicas. Es importante saber que las manifestaciones neurológicas de la EB reflejan una enfermedad más grave y rara vez se observan de forma aislada. Por lo tanto, los médicos que sospechan de NBD deben estar atentos para buscar el probable desarrollo de síntomas y signos fuera del SNC. Esto también es importante en pacientes con EB conocida, ya que las manifestaciones neurológicas tienden a aparecer durante los brotes graves y se deben buscar manifestaciones sistémicas de EB. En las presentaciones meningíticas, el diagnóstico diferencial de la meningitis bacteriana aguda es esencial. La meningitis bacteriana aguda es una emergencia médica y el tratamiento antibiótico a menudo se inicia en entornos de emergencia antes de la confirmación microbiológica. Aunque el LCR en la NBD meningítica a menudo tiene menos leucocitos, a veces puede alcanzar los números encontrados en la meningitis bacteriana y la falta de reconocimiento puede tener consecuencias graves. Se puede observar una mejoría clínica transitoria tras la institución de medidas de apoyo y antibióticos, lo que puede retrasar el tratamiento agresivo de la EB.
Los síndromes uveomeníngeos son un grupo heterogéneo de trastornos inflamatorios caracterizados por inflamación meníngea y afectación ocular (uveítis).27 El diagnóstico diferencial incluye muchas entidades, y las características sistémicas asociadas, la afectación de órganos específicos (por ejemplo, pulmón en sarcoidosis) y las características de imágenes y biomarcadores pueden ayudar a distinguir las NBD de las otras afecciones. Además de NBD, los síndromes uveomeníngeos incluyen:
- sarcoidosis;
- granulomatosis con poliangitis;
- sífilis;
- enfermedad de Vogt-Koyanagi-Harada; y
- epiteliopatía pigmentaria placoide multifocal posterior aguda.
Una de las consideraciones más importantes y desafiantes en el diagnóstico diferencial de ECNB es la EM. 18, 28 Cuando el diagnóstico para cualquiera de las entidades está bien establecido, la distinción es relativamente fácil; sin embargo, en las fases iniciales, la distinción puede ser difícil. Las lesiones parenquimatosas de NBD pueden imitar a las de la EM en la RMN en la mayoría de los aspectos, incluida la forma ovoide de la callosa ‘dedos de Dawson’ y la presencia de una vena central. Debido a la distribución perivenular de las lesiones en ambas condiciones, la utilidad del signo central y su papel en el diagnóstico diferencial de SM versus NBD sigue siendo objeto de debate en las discusiones de consenso de expertos.28,29 Si bien esto es particularmente relevante al comienzo de la enfermedad y las pruebas recientes muestran que más lesiones de MS que de sustancia blanca NBD tienen venas centrales, es necesario tener en cuenta que, en general, los pacientes con NBD tienen menos lesiones de sustancia blanca que los pacientes con MS, por lo que el uso de la vena central para la distinción puede seguir siendo difícil. En el cuadro 1 se pueden ver otras cuestiones que han sido útiles para distinguir las dos entidades. Es importante tener en cuenta que la manifestación inicial de NBD puede ser una lesión cerebral tumefactiva, que puede ser casi indistinguible tanto de una presentación tumefactiva de EM como de un tumor cerebral, siendo este último una consideración esencial para el diagnóstico diferencial.30,31 Los médicos deben ser conscientes de que la NBD y la EM no tienen por qué excluirse mutuamente. De hecho, un grupo de pacientes con NBD establecido también cumple los criterios diagnósticos para la EM y tiene características clínicas, de imagen y de laboratorio (bandas oligoclonales en el LCR) de la EM.32
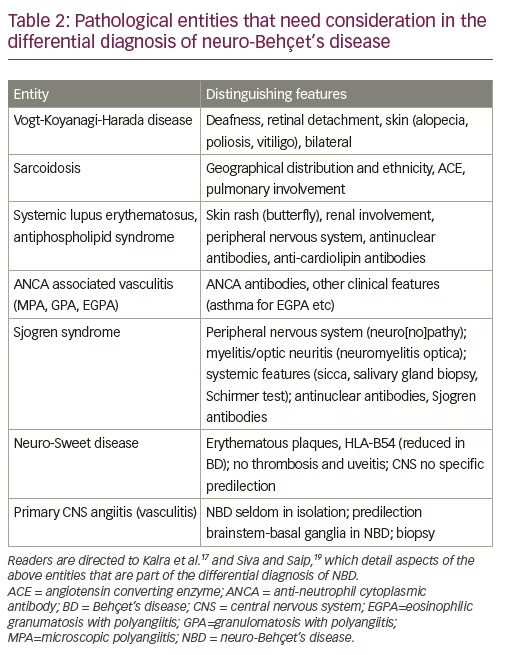
Otro aspecto importante del diagnóstico diferencial es la vasculitis sistémica, que puede ser primaria o secundaria a otras enfermedades inflamatorias sistémicas con manifestaciones neurológicas. En la Tabla 2 se presenta una lista de la enfermedad inflamatoria sistémica con o sin vasculitis secundaria que puede ser mal diagnosticada como NBD y sus características distintivas que pueden ayudar en el diagnóstico diferencial de NBD. Estos se discuten con más detalle en Kalra et al. y Siva y Saip.18,24
En pacientes que presentan ictus agudo, la variante vascular de NBD a veces representa parte del diagnóstico diferencial. Para distinguirlo del ictus aterosclerótico no vasculítico, es útil tener en cuenta la mayor frecuencia de trombosis venosa en comparación con el ictus de territorio arterial en NBD. Por otro lado, algunos accidentes cerebrovasculares en NBD involucran territorios arteriales, por lo que un accidente cerebrovascular arterial puede ser una manifestación de NBD. También es importante recordar que los pacientes con EB tienen un mayor riesgo de eventos cardiovasculares, incluido el accidente cerebrovascular, independientemente de si tienen o no DBE.33 Las disecciones arteriales y las hemorragias, aunque son relativamente raras en NBD, deben desencadenar la sospecha de ello en el entorno clínico apropiado.
La ECB psiquiátrica es una manifestación rara, generalmente con una presentación subaguda y progresiva, y tiene manifestaciones muy diversas, imitando demencia degenerativa primaria, depresión o psicosis franca. Es muy importante considerar NBD en tales pacientes.34
Un aspecto importante del diagnóstico diferencial es el desarrollo de un problema neurológico en un paciente con EB establecida. Los médicos deben establecer si el problema está relacionado con la NBD o no. Además del accidente cerebrovascular, el dolor de cabeza es una queja muy común en personas con EB y generalmente no representa una manifestación de NBD. Sin embargo, se necesita vigilancia, ya que el dolor de cabeza a menudo anuncia otras manifestaciones de NBD.
La neuropatía periférica ocurre raramente como manifestación clínica de NBD y cuando se diagnostica en una persona con BD y sin otras manifestaciones neurológicas, se justifica la búsqueda de etiologías alternativas.35
Finalmente, un aspecto emergente del diagnóstico diferencial se refiere a las complicaciones neurológicas del tratamiento de la EB. Es fundamental no confundir tales complicaciones con el desarrollo de NBD. El papel de la ciclosporina en la NBD es importante, ya que se ha relacionado de manera consistente con una posible aceleración y empeoramiento de la NBD. Otros tratamientos también pueden tener complicaciones. Los agentes inmunosupresores ocasionalmente pueden facilitar la meningitis, que puede confundirse con NBD. El uso de agentes anti-TNF como infliximab, que ha demostrado ser exitoso en NBD36,debe requerir vigilancia, ya que se han notificado desmielinización y otras complicaciones neurológicas con estos agentes, aunque todavía no se ha notificado ninguna con el uso en BD.
La talidomida, que se utiliza ocasionalmente para el BD, causa previsiblemente una neuropatía que no está relacionada con NBD. El síndrome de encefalopatía reversible posterior se ha notificado como una complicación de varias terapias inmunitarias, incluidos agentes anti-TNF, y en el simposio de CONy de 2017, el Dr. George Vavougios de Grecia informó de un caso interesante en EB (Comunicación oral, Congreso de CONy, Atenas 2017).
En conclusión, la NBD es una afección neuroinflamatoria grave que plantea grandes desafíos diagnósticos, diagnósticos diferenciales y terapéuticos. El conocimiento de sus características clínicas y posibilidades terapéuticas junto con el diagnóstico precoz son esenciales en el manejo de la NBD.