háttér
Hashimoto encephalopathia (HE) egy ritka neuropszichiátriai szindróma társított pajzsmirigy antitestek és először számolt be Brain 1996-ban (Brain et al., 1966). A klinikai tünetek széles skáláját mutatja be, beleértve a neurológiai megnyilvánulásokat, mint például a stroke-szerű epizódok, rohamok, zavartság, myoclonus, ataxia, remegés és demencia, valamint pszichiátriai megnyilvánulások, beleértve az akut pszichózist, depressziós rendellenességeket, személyiségváltozásokat, hallucinációkat és skizofréniát (Kirshner, 2014; Menon et al., 2017). Ebben az esettanulmányban egy HE-ben szenvedő beteget írunk le, akinek klinikai tünetei és laboratóriumi vizsgálati eredményei utánozták a vírusos encephalitist.
esettanulmány
egy 59 éves férfit, akinek láza, fejfájása és kínos beszéde volt, amely kifejezetten lassú és homályos beszédként nyilvánult meg, kórházba vitték. Tagadta a közelmúltbeli fertőzéseket, például az influenzát vagy a gastroenteritist, az utazást és más lehetséges okokat, amelyek felelősek lehetnek a lázért, amely 39,5-nél tetőzött C. A korábbi kórtörténet köszvényt mutatott 20 évig, de nem írtak fel gyógyszereket. Neurológiai vizsgálata és koponya komputertomográfiája (CT) és mágneses rezonancia képalkotása (MRI) (1.ábra) normális volt. Az EEG-eredmények kisebb szabálytalanságokat mutattak a kétoldali félgömbök által kibocsátott hullámokban (5-20 6V 14-20 Hz). A vér rutinja, a C-reaktív fehérje, a szérum B12-vitamin és a folsav, valamint az antinukleáris antitestet (ANA), az anti-neutrofil citoplazmatikus antitesteket (ANCA) és a reumatoid faktorokat tartalmazó autoimmunitás készítői mind figyelemre méltóak voltak. A cerebrospinális folyadék (CSF) megnövekedett fehérvérsejtszámot (WBC) mutatott (104 606/l, referenciatartomány 0-8 10^6/L) és emelkedett fehérjeszintet (1,68 g/L, referenciatartomány 0,15–0,45 g/L). A tenyészet, a kenet, valamint a bakteriális, gombás, vírusos és tubercle bacillus antitestek a szérumban és a CSF-ben negatívak voltak. Vírusos agyvelőgyulladást diagnosztizáltak nála, és vírusellenes szerekkel kezelték. A tünetek egy héten belül enyhültek, és kiengedték a kórházból. Öt hónappal később ismét a kórházunkba utalták, 38,5 C-os láza és alkalmanként az ítélet zavara miatt. Újabb lumbálpunkciót hajtottak végre; a CSF FEHÉRVÉRSEJTSZÁMA 39 volt 60 ^ 6 / l, a fehérjetartalom pedig 1,32 g / l volt. A koponya MRI és a laboratóriumi vizsgálatok eredményei majdnem normálisak voltak, kivéve a csökkent pajzsmirigyfunkciót és a szérum és a CSF anti-pajzsmirigy autoantitest (ATA) szintjének emelkedését. A kezdeti eredmények a következők voltak: a szérumban a pajzsmirigy–stimuláló hormon (TSH) koncentrációja 43,39 uIU/ml volt (referencia tartomány (RR): 0,27–4,2 uIU/ml), a szabad trijód–tironin (FT3) koncentrációja 2,89 pmol/ml (RR: 3,1–6,8 pmol/ml), a szabad tiroxin (FT4) koncentrációja 7,18 pmol/ml (RR: 12,0-22,0 pmol/ml), a teljes trijód-tironin (TT3) koncentráció 1,17 pmol/ml volt (RR: 1,3-3.1 pmol/ml), and total thyroxine (TT4) concentration was 44.26 pmol/ml (RR: 66–181 pmol/ml); the titer of anti-thyroglobulin autoantibodies (TgAb) was 1274 IU/ml (RR: < 115 IU/ml) and the titer of anti-thyroperoxidase autoantibodies (TPOAb) was 600 IU/ml (RR: < 35 IU/ml). In the CSF, ATA was positive (TPOAb 17.06 IU/ml, TgAb 16.02 IU/ml). Ultrasound imaging indicated diffuse lesions of the thyroid. Az anti-NMDAR, AMPA1, AMPA2, LGI1, CASPR2, GABA, GAD, anti-Hu, Yo, Ri, MAI, MA2, CV2, Amfifizin, SOX-1, Tr, Zic4 és GAD65 antitest analízise mind a szérumban, mind a CSF-ben negatív volt. A betegnél végül HE-t, Hashimoto pajzsmirigygyulladását és hypothyreosisát diagnosztizálták, és metilprednizolont és Euthyroxot írtak fel. A metilprednizolont 80 mg/nap dózisban kezdték el 1 héten keresztül, és 40 mg/napra csökkentették a 2 héten; ezt követően orális prednizolont írtak fel, amelyet heti 5 mg-os elválasztással, azaz orális prednizolont használtak összesen 8 hétig. Tünetei 3 nap alatt enyhültek. A beteg 1 éves követési időszak alatt egészséges maradt.
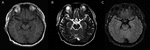
1. ábra. Az agy MRI képalkotása. A beteg agyi MRI képalkotásában nincsenek rendellenes eredmények. (A) T1-súlyozott kép; (B) T2-súlyozott kép; (C) FLAIR kép.
Vita
a HE becsült előfordulási aránya 2,1 a 100 000-ből, A nemek aránya (nő és férfi) 4:1 (Ferracci et al., 2004). Az ő lefolyása progresszív lehet, visszaeső-remittáló, vagy akár önkorlátozó. Ebben az esetben úgy tűnt, hogy a beteg relapszus-remittáló lefolyású.
a beteg tüneteivel, a normál MRI eredményekkel, a szérum magas ATA-titerével és a CSF ATA-pozitivitásával kombinálva a beteget végül HE-vel diagnosztizálták, miután kizárták az egyéb lehetséges okokat, beleértve a stroke – ot, a tumort, a központi idegrendszeri fertőzést, az autoimmun encephalitist és a paraneoplasztikus szindrómát.
összességében a He patofiziológiája még mindig nem meggyőző. A neuropatológiai eredmények alapján autoimmun vasculitis mechanizmust javasoltak. Egy korábbi vizsgálatban az agyi biopsziák azt mutatták, hogy a venulák és az arteriolák körüli limfocita infiltráció részt vehet (Duffey et al., 2003). Egy másik lehetséges mechanizmus az, hogy az ATAs megtámadja a pajzsmirigy és az agy által megosztott antigéneket, és ezért az ATAs magas titerei, beleértve a tpoab, a TgAb és az anti-TSH receptor (TSH-R) antitesteket a szérumban, és néha a CSF-ben, a HE fémjelzi (Yoneda, 2018). Hasonlóképpen, az ATA és a CSF-ATA magas titereit találtuk esetünkben. Egy korábbi vizsgálatban a plazmacsere-terápia a betegek tüneteinek mélyreható javulását eredményezte (Tran et al., 2018). Ezek az eredmények együttesen azt sugallják, hogy az ATA fontos szerepet játszik a HE-ben. Ugyanakkor a szérum emelkedett ATA-szintje az általános populációban is megtalálható,és különösen gyakori az időseknél. Ezenkívül az ATA-emelkedés mértéke nem függ össze a HE súlyosságával. Bár a betegek szérum ATA-szintje továbbra is magas maradt a metilprednizolon-kezelés után, tünetei megszűntek (anti-tiroglobulin autoantitestek titere (TgAb): 041 NE / ml, RR: < 115 NE/ml; anti-tiroperoxidáz autoantitestek titere (TPOA): 600 NE/ml, RR: <35 NE / ml). Eredményeink megerősítik, hogy nincs kapcsolat az ATA-emelkedés mértéke és a HE súlyossága között.
bár az ATA és a HE közötti összefüggés még mindig nem tisztázott (Kirshner, 2014), A Lancet Neurology szakértői csoportja 2016-ban javasolta a He diagnosztikai kritériumait. A kritériumok a következők: (1) görcsrohamokkal, myoclonusszal, hallucinációkkal vagy stroke-szerű epizódokkal járó encephalopathia; (2) szubklinikai vagy enyhe nyilvánvaló pajzsmirigybetegség (általában hypothyreosis); (3) az agyi MRI által kimutatott normál leletek vagy nem specifikus rendellenességek; (4) pajzsmirigy antitestek jelenléte a szérumban (pajzsmirigy peroxidáz, tiroglobulin); (5) jól jellemzett neuronális antitestek hiánya a szérumban és a CSF-ben; és (6) az alternatív okok ésszerű kizárása. Diagnosztizálható, ha a beteg megfelel az összes kritériumnak (Graus et al., 2016). Betegünk teljesítette a fenti kritériumokat, ezért diagnosztizálható volt HE-vel. A legtöbb HE-ben szenvedő beteg jól reagál a szteroidokra; Mindazonáltal, ha a betegek szteroidrezisztensek, más immunszuppresszív terápiák, köztük a plazmacsere, az IVIg, a metotrexát és a mikofenolát hatásosnak bizonyultak. A leggyakrabban nagy dózisú metilprednizolont (500-1000 mg) alkalmaznak. Mivel a beteg enyhe tüneteket mutatott, és elutasította a nagy dózisú metilprednizolon alkalmazását, alacsony dózisú metilprednizolont írtunk fel. Betegünk szteroid terápián esett át, azóta egészséges maradt. A beteg nem kapott más immunterápiás kezelést a nyomon követés során. Egy retrospektív megfigyelési tanulmányban, amelyet Mamoudjy et al. (2013) a kutatási eredmények azt mutatták, hogy néhány HE-beteg relapszuson esett át, még egy harmadik rohamon is, amelynek rövidebb időintervalluma volt (átlagosan 18 nap) a második rohamhoz képest (átlagosan 213 nap). A relapszusban szenvedő betegeknek ismét metilprednizolonra vagy immunszuppresszív terápiára volt szükségük (Mamoudjy et al., 2013). Betegünk egy visszaesést szenvedett körülbelül 150 nappal az első roham után, és a szteroid terápia hatékony volt. A következmények, mint például a fejfájás, a memóriazavarok stb., szintén gyakoriak voltak (Mamoudjy et al., 2013), azonban a betegünknek szerencsére nem maradt következménye.
Hashimoto encephalopathiáját nehéz pontosan diagnosztizálni, mivel a klinikai tünetek széles skálájával, valamint a nem specifikus neuro-képalkotással és elektroencefalogrammal kapcsolatos megjelenéssel jár. Egy korábbi cikk arról számolt be, hogy a HE-t eredetileg tévesen diagnosztizálták vírusos encephalitisként (He et al., 2013), amelyben a beteg fokozatosan károsodott kognitív funkcióval és kontrollálatlan rohamokkal jelentkezett láz nélkül. Esetünkben a megnövekedett fehérvérsejtszám és a CSF fehérje lázzal és fejfájással kombinálva arra késztet bennünket, hogy vírusos encephalitisként diagnosztizáljuk. A lázat számos pajzsmirigy-rendellenességgel vagy anélkül szenvedő HE-ben szenvedő betegnél írták le (Huang et al., 2011; Lu et al., 2015). Bár a láz oka nem világos, Lu et al. (2015) azt javasolta, hogy az autoimmun vasculitissel kombinált gyulladás közvetlen következménye lehet.
Hashimoto encephalopathiája sokféle módon manifesztálódhat, beleértve a stroke-szerű epizódokat, rohamokat, zavartságot, myoclonust, akut pszichózist, depressziós rendellenességeket és hallucinációkat, ami összetéveszthető más betegségekkel. Uwatoko et al. (2018) egy olyan beteg esetéről számolt be, aki parkinsonizmussal és az agyi MRI által feltárt tumorszerű elváltozással jelentkezett. A biopszia után kiderült, hogy az elváltozás nem daganat, és végül megerősítést nyert (Uwatoko et al., 2018). A HE-ben szenvedő betegeknél szokatlan tünetek is jelentkezhetnek, mint például pseudobulbar bénulás, szenzomotoros polyneuropathia, katatonikus tünetek, vertigo, izomgyengeség, chorea, opsoclonusés trigeminus neuralgia típusú fejfájás, többek között (Beckmann et al., 2011; Salazar et al., 2012; Sharan et al., 2015; Ueno et al., 2016; Karthik et al., 2017; Emeksiz et al., 2018; Oz Tuncer et al., 2018). A gyorsan progresszív demencia, mint a HE közös megnyilvánulása, szükségessé teszi a HE megkülönböztetését más érrendszeri, fertőző, toxikus-metabolikus és autoimmun faktorok, metasztázis/neoplázia, iatrogén/veleszületett anyagcsere-hibák, neurodegeneratív betegségek és szisztémás betegségek/rohamok által okozott betegségektől (Paterson et al., 2012).
következtetés
összefoglalva, a HE diagnózisa meglehetősen összetett, de értékes az immunszuppresszív terápiára adott drámai válasz miatt. Ha a klinikusok megmagyarázhatatlan encephalitissel szembesülnek, a pajzsmirigy működését és az ATA szintjét hagyományos vizsgálatoknak kell tekinteni. Kizárható diagnózisként az ATA normál szérumszintjével rendelkező betegek számára. Azoknál a betegeknél, akiknél megnövekedett az ATA szintje, mérlegelni kell az egyéb lehetséges betegségek kizárása után.
Data Availability Statement
az ehhez a tanulmányhoz létrehozott adatkészletek kérésre rendelkezésre állnak a megfelelő szerző számára.
etikai nyilatkozat
az emberi résztvevőket érintő vizsgálatokat a kínai Jilin Egyetem Első Kórházának Etikai Bizottsága felülvizsgálta és jóváhagyta. A betegek / résztvevők írásbeli tájékozott beleegyezésüket adták a részvételhez ebben a tanulmányban. Az egyén(ek) től írásbeli tájékoztatáson alapuló beleegyezést kaptak az e cikkben szereplő bármely potenciálisan azonosítható kép vagy adat közzétételéhez.
szerzői hozzájárulások
HM hozzájárult a koncepció és a tervezés a kézirat. Én írtam a kézirat első vázlatát. YY, XM, YXÉS NS írta a kézirat részeit. Minden szerző hozzájárult a kézirat átdolgozásához, elolvasta és jóváhagyta a benyújtott verziót.
finanszírozás
ezt a munkát támogatta a Nemzeti kulcs R& D Program Kína (no.2017yfc0110304).
összeférhetetlenség
a szerzők kijelentik, hogy a kutatást olyan kereskedelmi vagy pénzügyi kapcsolatok hiányában végezték, amelyek potenciális összeférhetetlenségnek tekinthetők.
Beckmann, Y. Y., Top, D. és Yigit, T. (2011). Hashimoto encephalopathia szokatlan bemutatása: trigeminus neuralgiaform fejfájás, ferde eltérés, hypomania. Endokrin 40, 495-496. doi: 10.1007 / s12020-011-9506-x
PubMed absztrakt / CrossRef teljes szöveg / Google Tudós
Brain, L., Jellinek, E. H. és Ball, K. (1966). Hashimoto-kór és encephalopathia. Lancet 2, 512-514.
Google Scholar
Duffey, P., Yee, S., Reid, I. N. és Bridges, L. R. (2003). Hashimoto encephalopathia: postmortem eredmények halálos status epilepticus után. Neurológia 61, 1124-1126.
PubMed absztrakt / Google Scholar
Emeksiz, S., Kutlu, N. O., Alacakir, N. és Caksen, H. (2018). Szteroidrezisztencia Hashimoto encephalopathiája szenzomotoros polyneuropathiával jelentkezik. Turk. J. Pediatr. 60, 310–314. doi: 10.24953 / turkjped.2018.03.012
PubMed absztrakt / CrossRef teljes szöveg / Google Scholar
Ferracci, F., Bertiato, G. és Moretto, G. (2004). Hashimoto encephalopathia: epidemiológiai adatok és patogenetikai megfontolások. J. Neurol. Sci. 217, 165–168.
PubMed absztrakt / Google Scholar
Graus, F., Titulaer, M. J., Balu, R., Benseler, S., Bien, C. G., Cellucci, T., et al. (2016). Az autoimmun encephalitis diagnózisának klinikai megközelítése. Lancet Neurol. 15, 391–404.
Google Scholar
ő, L., Li, M., hosszú, X. H., Li, X. P. és Peng, Y. (2013). Hashimoto encephalopathiáját tévesen vírusos encephalitisként diagnosztizálták. Az vagyok. J. Ügy Rep. 14, 366-369.
Google Scholar
Huang, W., Xia, C. és Chatham, M. (2011). Fertőző betegség vagy Hashimoto encephalopathia fellángolása: esettanulmány. Lefoglalás 20, 717-719. doi: 10.1016 / j. lefoglalás.2011.04.011
PubMed absztrakt / CrossRef teljes szöveg / Google Scholar
Karthik, M. S., Nandhini, K., Subashini, V. és Balakrishnan, R. (2017). Hashimoto encephalopathiája szokatlan viselkedési zavarokat mutat egy serdülő lánynál. Case Rep. Med. 2017, 3494310. doi: 10.1155/2017/3494310
PubMed absztrakt / CrossRef teljes szöveg / Google Tudós
Kirshner, H. S. (2014). Hashimoto encephalopathia: rövid áttekintés. Curr. Neurol. Neurosci. REP. 14:476.
Google Scholar
Lu, T., Zhou, Z., Wu, A., Qin, B. és Lu, Z. (2015). Lázas Hashimoto encephalopathia Hashitoxicosissal társul. Acta Neurol. Belg. 115, 811–813.
Google Tudós
Mamoudjy, N., Korff, C., Maurey, H., Blanchard, G., Steshenko, D., Loiseau-Corvez, M. N., et al. (2013). Hashimoto encephalopathia: azonosítás és hosszú távú eredmény gyermekeknél. Eur. J. Paediatr. Neurol. 17, 280–287. doi: 10.1016 / j. ejpn.2012.11.003
PubMed absztrakt / CrossRef teljes szöveg / Google Tudós
Menon, V., Subramanian, K. és Thamizh, J. S. (2017). Hashimoto encephalopathia: a szakirodalomban jelentett esetek szisztematikus áttekintése és elemzése. J. Neurosci. Vidéki. Gyakorlat. 8, 261–267. doi: 10.4103 / jnrp.jnrp_440_16
PubMed absztrakt / CrossRef teljes szöveg / Google Scholar
Oz Tuncer, G., Teber, S., Kutluk, M. G., Albayrak, P. és Deda, G. (2018). Hashimoto encephalopathiája pszeudobulbáris bénulásként jelentkezik. Childs Nerv. Syst. 34, 1251–1254. doi: 10.1007 / s00381-018-3720-2
PubMed absztrakt / CrossRef teljes szöveg / Google Tudós
Paterson, R. W., Takada, L. T. és Geschwind, M. D. (2012). A gyorsan progresszív demenciák diagnosztizálása és kezelése. Neurol Clin. Gyakorlat. 2, 187–200.
PubMed absztrakt / Google Scholar
Salazar, R., Mehta, C., Zaher, N. és Miller, D. (2012). Opsoclonus, mint Hashimoto encephalopathia megnyilvánulása. J. Clint. Neurosci. 19, 1465–1466. doi: 10.1016 / j. jocn.2012.02.012
PubMed absztrakt / CrossRef teljes szöveg / Google Tudós
Sharan, A., Sengupta, S., Mukhopadhyay, S. és Ghosh, B. (2015). Hashimoto encephalopathiája jelentkezik a Chorea – val. J. Assoc. Orvosok India 63, 83-84.
PubMed absztrakt / Google Scholar
Tran, M. H., Mkhikian, H., Sy, M., Perez-Alvarez, I. és Demetriou, M. (2018). Hosszú távú plazmacsere a cerebelláris típusú Hashimoto encephalopathia fenntartó terápiájaként, esettanulmány. Transfus. Apher. Sci. 57, 418–420. doi: 10.1016 / j. transci.2018.05.027
PubMed absztrakt / CrossRef teljes szöveg / Google Scholar
Ueno, H., Nishizato, C., Shimazu, T., Watanabe, H., Mizukami, T., Kosuge, H., et al. (2016). Hashimoto encephalopathiája szédüléssel és izomgyengeséggel jár egy férfi gyermekbetegnél. Nincs Hattatsu 48, 45-47.
PubMed absztrakt / Google Scholar
Uwatoko, H., Yabe, I., Sato, S., Abe, M., Shirai, S., Takahashi, I., et al. (2018). Hashimoto agydaganatot utánzó encephalopathiája és kóros eredményei: esettanulmány. J. Neurol. Sci. 394, 141–143. doi: 10.1016 / j. jns.2018.09.008
PubMed Absztrakt / CrossRef Teljes Szöveg / Google Scholar
Yoneda, M. (2018). Hashimoto encephalopathia és autoantitestek. Agyideg 70, 305-314. doi: 10.11477 / mf.1416201004
PubMed Absztrakt / CrossRef Teljes Szöveg / Google Tudós