Reaksjoner i oppløsning som ikke katalyseres, er langsomme siden ladningsutvikling og separasjon oppstår i overgangsstatus. Når bindinger er laget eller brutt, ladede mellomprodukter er ofte dannet som er høyere i energi enn reaktantene. Siden mellomproduktet er høyere i energi enn reaktantene, vil overgangsstaten være enda høyere i energi, og dermed mer likne det ladede mellomproduktet. Alt som kan stabilisere ladningene på mellomproduktet og dermed utviklingskostnadene i overgangsstatene, vil senke energien i overgangsstaten og katalysere reaksjonen. I denne delen vil vi undersøke mekanismen bak katalyse av små molekyler av kjemiske reaksjoner. Formentlig vil biologisk makromolekylær katalysator (som protein enzymer) bruke lignende mekanismer i deres katalytiske effekter (som vil bli diskutert i neste avsnitt).
Katalysatorer, inkludert enzymer, kan bruke minst 5 forskjellige måter å stabilisere overgangsstater.
Ladningsutvikling i TS kan reduseres ved enten donasjon av et proton fra generelle syrer (som eddiksyre eller en protonert indolring) til et atom som en karbonyl O som utvikler en delvis negativ ladning i TS når DEN er festet av en nukleofil. Protondonasjon reduserer det utviklende negative I TS. Alternativt kan en nukleofil som vann som utvikler en delvis positiv ladning i TS når DEN begynner å danne en binding til en elektrofil C i en karbonyl stabiliseres ved tilstedeværelse av en generell base (som acetat eller den deprotonerte indolringen). Protonabstraksjon reduserer den utviklende positive ladningen
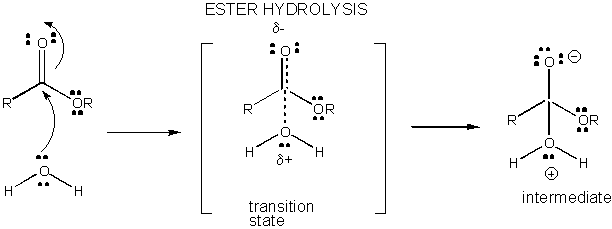
Figur: LADNINGSUTVIKLING I OVERGANGSSTATUS FOR ESTERHYDROLYSE
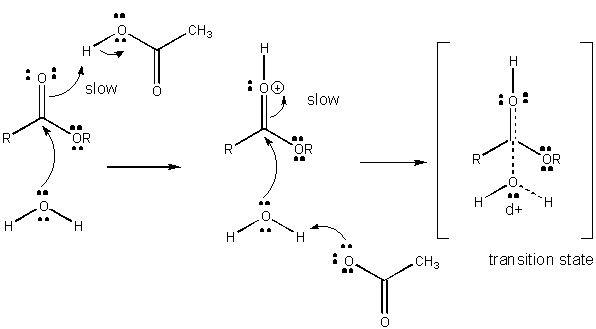
Figur: MEKANISME FOR GENERELL SYREKATALYSE
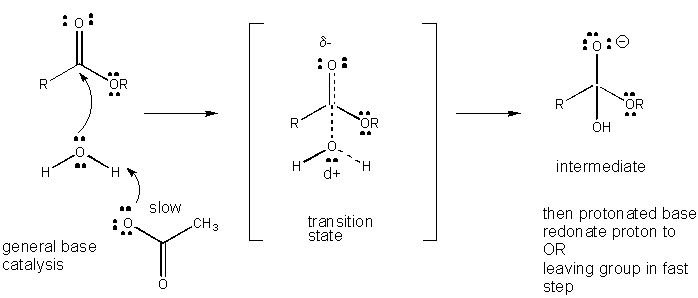
Figur: MEKANISME FOR GENERELL BASEKATALYSE
Bidragsytere Og Attribusjoner
- Prof. Henry Jakubowski (College Of St. Benedict / St. John ‘ S University)