Vitamin E Behandling For Pasienter Med Ikke-Alkoholisk Steatohepatitt
Jhonathan Ferney Vé M. (1), Gustavo Amador Crespo H. (1), Juan Carlos Restrepo G. MD. Esp, MSc, PhD. (2)
(1) Medisinstudent ved Det Medisinske Fakultet Ved Universidad De Antioquia I Medellí, Colombia.
(2) Førsteamanuensis Ved Institutt For Indremedisin og Gastrohepatologigruppen Ved Universidad De Antioquia og Hepatolog Ved Sykehuset Pablo Tiló Uribe i Medellí, Colombia. [email protected]
Mottatt: 12-02-14 Akseptert: 05-11-14
Abstrakt
Nonalcoholic Steatohepatitis (NASH) karakteriseres histologisk ved ballongdannelse av hepatocytter, lobulær betennelse og steatose. Hvis denne diagnosen mistenkes, er det viktig å utelukke andre årsaker til leverskade, spesielt overdreven forbruk av alkohol. Likevel er en biopsi til dags dato den eneste metoden som er tilgjengelig for å bekrefte diagnosen. E-Vitamin bør betraktes som en førstelinjebehandling for behandling av denne sykdommen fordi flere kliniske studier har vist at en dose på 800 UI / dag forbedrer histologien til ikke-diabetiske voksne som lider AV NASH, selv når det ikke er noen signifikant innvirkning på fibrose. Disse resultatene ble bekreftet av biopsier. Til tross for de påviste fordelene ved bruk av dette stoffet, er det viktig å være oppmerksom på at bruken ikke kan erstatte endringer i kosthold og mosjon, men heller bør ses som et supplement til disse tiltakene.
Nøkkelord
Ikke-Alkoholisk steatohepatitt, Vitamin E, oksidativt stress.
INNLEDNING
NASH karakteriseres histologisk av ballongdannelse av hepatocytter, lobulær inflammasjon og steatose (1, 2). FOR TIDEN kan NASH bare diagnostiseres gjennom en leverbiopsi som er diagnostisk gullstandard. Det gir også informasjon om tilstedeværelse og grad av betennelse, nekrose og fibrose som alle er viktige for å etablere pasientens prognose (2-5). Forskjellene MELLOM nash og alkoholisk steatohepatitt er mikroskopisk små, noe som gjør det vanskelig å histologisk skille mellom dem. Av denne grunn er det viktig å innhente informasjon fra pasienten om hans eller hennes drikkevaner (4).
NASH er en del av EN mye bredere enhet kalt NAFLD (nonalcoholic fatty liver disease) som inkluderer de tidlige stadier av hepatisk steatose: steatosis uten betennelse, og steatosis med mild betennelse. TIL slutt utvikler NAFLD seg til den karakteristiske inflammatoriske tilstanden TIL NASH som utvikler seg til fibrose og til slutt cirrhose (1, 2, 5). Det er ennå ikke helt klart at individer utvikler seg fra enkel steatose til inflammatorisk tilstand. Interaksjoner mellom genetisk følsomhet, metabolske forstyrrelser og oksidativt stress er de viktigste faktorene (6, 7).
NAFLD er den mest utbredte leversykdommen i verden (2, 4, 6). Forekomsten AV NAFLD er estimert til å være fra 20% til 30%, og forekomsten AV NASH antas å være fra 2% til 3% i den generelle befolkningen i den vestlige verden (8).
På grunn av dens antioksidantegenskaper har Vitamin E blitt anbefalt i gjeldende Amerikanske retningslinjer for behandling AV NASH. «Vitamin E (α-tokoferol) administrert i daglig dose på 800 IE / dag forbedrer leverhistologi hos ikke-diabetiske voksne med biopsi-bevist nash» dette utelukker ikke betydningen av intervensjon i pasientens livsstil og diett som en del av grunnleggende behandling for pasienter MED NASH (9, 10). I denne artikkelen vurderer vi patofysiologien TIL NASH med vekt på rollen som vitamin E i behandlingen av pasienter med denne sykdommen.
PATOFYSIOLOGI
mens patogenesen til NASH ennå ikke er helt klar, er den beste aksepterte hypotesen foreslått til dags dato for å forklare hendelsene som førte til steatose og deretter til steatohepatitt» to-hit » teorien. Det første treffet i begynnelsen av denne sykdommen er fettoverbelastning (11, 12). En stillesittende livsstil, genetiske faktorer og økt kaloriinntak gjør individer mer utsatt for utvikling av insulinresistens og hyperinsulinemi som fører til en økning i hepatisk lipidsyntese og frigjøring av frie fettsyrer fra fettvev. Hvis leveren opprettholdes i denne tilstanden, blir den ikke i stand til å metabolisere alle fettsyrene den produserer og som fjernes fra sirkulasjon. Denne tilstanden fører til slutt til det andre treffet som er hepatisk steatose og oksidativt stress (4, 5, 13).
Oksidativt stress er en ubalanse som favoriserer prooksidanter over antioksidanter (3). Under hepatisk steatose går hepatocytter inn i en hypermetabolisk tilstand som fører til økt produksjon av frie radikaler i celleorganeller (13). Økende mengder reaktive oksygenarter (ROS) i hepatocytter fører til lipidperoksydasjon, som er en reaksjon som gir en kontinuerlig tilførsel av ytterligere frie radikaler med potensielt ødeleggende effekter (14, 15).
en antioksidant er vitamin e (tokoferol) som reagerer med lipidperoksider for å redusere dem mot fettsyrer. De danner den relativt stabile radikale tokoferoksyl som vedvarer lenge nok til å passere tilbake til tokoferol ved hjelp av en reaksjon Med vitamin C på celleoverflaten (12). På grunn av denne egenskapen har Vitamin E blitt vurdert til bruk som behandling for pasienter MED NASH (13, 16).
MANIFESTASJONER OG DIAGNOSE
NAFLD er et vanlig syndrom som spenner fra enkel steatose til steatohepatitt (NASH)med påfølgende fibrose og cirrhose (5). Selv om diagnosen de fleste pasienter er asymptomatiske, kan noen pasienter, spesielt barn, klage over tretthet og ubehag. Ubehag i høyre øvre kvadrant i magen, mistanke på grunn av økte nivåer av aminotransferaser og en abdominal ultralyd med en lys leversykdom er alle tegn på denne sykdommen. Fedme, diabetes og dyslipidemi bør også tas med i vurderingen av tilstander som kan være forbundet MED NAFLD og NASH (5, 17).
under den diagnostiske evalueringen bør andre vanlige årsaker til leversykdom utelukkes, men til slutt er en leverbiopsi den eneste metoden som er tilgjengelig for å bekrefte diagnosen. Det er også viktig å definere pasientens prognose (Tabell 1) (3, 4). Til tross for sin store kliniske verdi, er en biopsi dyr og fører til en liten økning i sykelighet og i sjeldne tilfeller resulterer i dødelighet. Dette verktøyet bør kun vurderes for pasienter hvor det er mistanke om ikke-alkoholisk hepatisk steatose som har høy risiko for steatohepatitt og fremskreden fibrose (fedme, TYPE II diabetes mellitus, dyslipidemi og metabolsk syndrom) og i tilfeller med usikker diagnose (3, 9).

ROLLE AV VITAMIN E I BEHANDLINGEN av ALKOHOLISK STEATOHEPATITIS
For tiden er det ingen effektiv behandling FOR NASH. Likevel, med tanke på den viktige rollen som vitamin E som en antioksidantfaktor, har det vært flere kliniske studier for å demonstrere fordelene i den kliniske og histopatologiske utviklingen av denne sykdommen (Tabell 2).
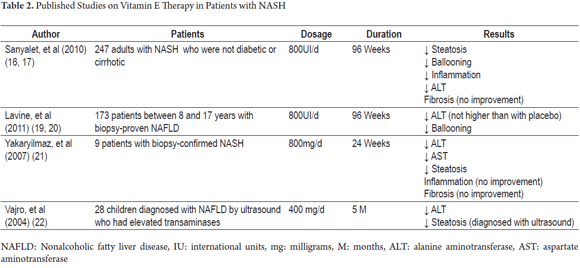
BLANT disse er pivens-studien (Pioglitazon versus vitamin e versus placebo for behandling av ikke-diabetespasienter med alkoholfri steatohepatitt). Dette var en multisenter, dobbeltblind, placebokontrollert studie hvor histologisk forbedring ble evaluert hos 247 ikke-diabetiske og ikke-cirrhotiske pasienter som hadde NASH. Pasientene ble randomisert til å motta en daglig dose pioglitazon (80 pasienter), vitamin E (84 pasienter) eller placebo (83 pasienter) i nittiseks uker (18). De daglige dosene var 30 mg for pioglitazon og 800u for vitamin e. denne studien fant at 43% av pasientene som fikk vitamin E (P = 0,001) forbedret seg mot 34% av de som fikk pioglitazon (P = 0,04) og 19% av de som fikk placebo. Forskjellen i forbedringsraten mellom pioglitazon og placebo var ikke statistisk signifikant, mens forskjellen mellom forbedringsraten For Vitamin E og placebo var. Likevel var begge legemidlene forbundet med forbedring av aminotransferasenivåer, reduksjon av steatose og lobulær betennelse, men ingen av dem resulterte i forbedring av fibrose. Den samme studien viste at etter behandling med vitamin e ble suspendert aminotransferase nivåer økt indikerer at ubestemt administrasjon av behandlingen kan være nødvendig. I tillegg ble det ikke funnet signifikante forskjeller mellom bivirkninger av vitamin E og bivirkninger av placebo (19).
en revurdering AV pivens-studien av Hoofnagle et al. fokusert på responsen av serum ALAT hos pasienter som fikk vitamin E eller placebo og på sammenhengen av denne responsen med de første kliniske, histologiske endringer og interaksjoner med endringer i kroppsvekt. De fant at endringer I ALT var vanligere blant de som fikk vitamin E (48%) enn hos de som fikk placebo (16%; p <0,001). BLANT gruppen som fikk vitamin E, var ALAT-responser assosiert med redusert aktivitet av ikke-alkoholisk fettleversykdom (NAFLD), men det var ingen forbedring i fibrose etter avsluttet behandling ved 96 uker. ALAT-nivåene økte i vitamin e-gruppen etter avsluttet administrering, men økte ikke i placebogruppen etter avsluttet administrering. Begge behandlingsgruppene hadde nesten identiske ALAT-nivåer ved uke 120. Disse resultatene er lik de som er vist i hele kohorten av hovedpubliseringen AV PIVENS-studien. Videre viste resultatene at vekttap (2 kg eller mer) også er assosiert med ALAT-respons, med forbedret NAFLD (<0,001) og forbedret fibrose (p <0,02), men Vitamin e hadde større effekt på NAFLD uavhengig av endringer i kroppsvekt. Til slutt bør det bemerkes at effekten av vitamin e og vekttap på ALT-respons og histologi er uavhengig, noe som betyr at selv de pasientene som mister vekt, vil ha nytte av behandling med vitamin E (20).
TONISK-studien (Behandling av ikke-alkoholisk fettleversykdom hos barn) var en annen multisenter, dobbeltblind, placebokontrollert studie. Det inkluderte 173 pasienter som var mellom åtte og sytten år. Pasientene ble randomisert til å motta vitamin E (58 pasienter), metformin (57 pasienter) eller placebo (58 pasienter) i 96 uker. Doser var 400 IE to ganger daglig for vitamin E og 500 mg to ganger daglig for metformin (21). Ingen av virkestoffene var bedre enn placebo for å oppnå enten vedvarende reduksjoner på minst 50% i BASELINE ALAT-nivåer eller vedvarende ALAT-nivåer på 40 E / L eller mindre. Målinger ble tatt hver 12. uke fra uke 48 til uke 96. Denne studien fant også at oppløsningen AV NASH var signifikant høyere i gruppen pasienter behandlet med vitamin E enn i placebogruppen. Dette resultatet ble tilskrevet den signifikante reduksjonen i hepatocellulær ballongdannelse som ble funnet hos pasienter behandlet med vitamin E. Dette ligner på pivens ‘ resultater, selv om TONIC-studien ikke så på redusert hepatocellulær ballongdannelse som et primært utfall på grunn av de histopatologiske forskjellene MELLOM NALFD hos pediatriske pasienter og voksne. TONIC-studien fant ingen forbedring i fibrose (22).
Før disse to store studiene hadde det vært andre mindre studier som hadde resultater med store forskjeller i de primære utfallene som ble evaluert. I tillegg til mye mindre populasjoner hadde disse studiene mindre overvåkingstid, og noen av dem ble ikke kontrollert med placebogrupper.
en 2007 studie Av Yakaryilmaz et al. så på effekten av vitamin E på ni pasienter hvis diagnoser AV NASH hadde blitt verifisert ved biopsi. Studien evaluerte effekten av vitamin e på peroksisomproliferatoraktivert reseptor gamma (PPARG) og på insulinresistens. Pasientene fikk 800 mg vitamin e daglig i 24 uker. Før behandlingen begynte ble pasientens lever evaluert biokjemisk og histologisk. Disse evalueringene ble gjentatt etter avsluttet behandling. Ved slutten av 24-ukene ble det funnet statistisk signifikante reduksjoner AV AST, ALT OG steatose, men ingen histologiske endringer ble funnet i nivået av betennelse og fibrose. Ingen pasient opplevde bivirkninger ved denne dosen av vitamin E (23).
Vajro, Et al. (2004) gjennomført en studie av en gruppe på 28 barn med fedme relatert leverdysfunksjon. Pasientene ble delt inn i to grupper. Gjennomsnittsalderen for gruppe en var 9,88 (+/- 3,97) år, og for gruppe to var 10,7 (+/- 3,45). Pasientene ble evaluert for å avgjøre om det var noen gunstige effekter av Vitamin e-behandling på vekttap, transaminasenivåer og steatose målt ved ultralyd. Barnene som inngår i denne studien hadde alle kronisk hypertransaminasemi (ASAT eller ALAT nivåer 1,5 ganger over normalverdien i mer enn 6 måneder) og tegn på steatose i ultralyd. Studien hadde en enkeltblind design der pasientene ble randomisert til en av to grupper: Gruppe 1 (placebo pluss diett) Og Gruppe 2 (vitamin e + diett). Senere ble hver gruppe delt inn avhengig av pasientens overholdelse av behandlingen. Gruppe 1 ble delt INN I Undergruppe 1A for de som fulgte dietten og Undergruppe 1B for de som ikke hadde overholdt. Gruppe 2 ble delt INN I Undergruppe 2A for de som hadde fulgt vitamin e-terapi og Undergruppe 2b for de som ikke hadde fulgt vitamin e-terapi. Undergruppe 2A ble videre delt INN I Undergruppe 2A1 for de som ikke fulgte dietten og Undergruppe 2A2 for de som fulgte dietten. Studien fant at Dosen på 400 mg/dag av Vitamin E ga signifikante reduksjoner I ALAT-verdier for pasienter I Undergruppe 2a som nærmet seg normalisering uavhengig av eventuelle endringer i vekt. På den annen side oppnådde de pasientene som oppnådde høye serumnivåer av vitamin E og også mistet VEKT alt normalisering og remisjon av steatose. Videre viste en sammenligning Mellom Undergruppe 1A som bare fulgte diett og Undergruppe 2a1 som bare fulgte Vitamin e-terapi at begge pasientgruppene hadde redusert nivå AV ALAT ved to måneders overvåking, men at Det var en større reduksjon I Undergruppe 1a (kun fulgt diett) enn I Undergruppe 2a1 (kun fulgt vitamin E) ved fem måneders overvåking. Alle tegn på steatose forsvant fra ultralydbilder I Undergruppe 2a2 gruppe som mistet vekt under behandling med 400 mg vitamin E. Disse resultatene fremhever viktigheten av å fremme sunn mat som en av de store behandlingstiltakene for pasienter med NASH, men vi må også merke seg at mange pasienter ikke overholder diettregimer som fører til svikt i intervensjonen. Dette understreker viktigheten av å bruke antioksidanter som vitamin E som et godt alternativ behandling for disse pasientene (24).
en pilotstudie av Kugelmas, et al. (2003) evaluerte effekten Av Trinn 1 I American Heart Association diett kombinert med økt aerob trening med og uten daglig administrasjon av vitamin E på profiler av cytokiner (TNF alfa, IL-8, IL -6) og nivåer av leverenzymer hos 16 pasienter mellom 18 og 65 år med biopsi bevist NASH. Dette var en enkeltblind studie hvor pasienter ble randomisert til å motta 800 IE Vitamin E daglig. Pasienter som ikke fikk vitamin E fikk placebo. Testen ble utført over en periode på 12 uker. Cytokinverdier ble ikke signifikant redusert med vekttap med eller uten administrasjon av vitamin E i løpet av studien. Livsstilsendringene var forbundet med forbedringer i leverenzymer og plasmakolesterol hos pasienter MED NASH, mens doseringen av vitamin E brukt i denne studien viste ingen ekstra fordel. Dette resultatet kan skyldes liten prøvestørrelse, kort oppfølgingstid eller dosering av vitamin E som brukes (25, 26).
en gjennomgang publisert i November 2013 om tilgjengelige alternativer for behandling av pasienter MED NASH anerkjente dagens anbefaling for bruk av vitamin E som førstelinjebehandling hos pasienter med NASH bekreftet av biopsi som ikke er cirrhotisk og som ikke har diabetes, men fremhevet også det faktum at denne terapien bare har vist en betydelig fordel hos mindre enn halvparten av pasientene. Av denne grunn konkluderte gjennomgangen med at fremtidige behandlingsstrategier bør være basert på patogene sykdomsveier dersom en effektiv behandling for pasienter med NASH noen gang skal utvikles (27).
Ji H-F et al. utført en meta-analyse for å evaluere effekten av vitamin e på avtagende aminotransferaser hos pasienter MED NAFLD, NASH og kronisk hepatitt C (CHC). De fire studiene de så på, inkluderte pasienter MED NASH som fikk Vitamin e-tilskudd. Studiene inkluderte TONIC-og PIVENS-studiene. De fant at Vitamin E kunne optimalisere nivåene AV AST og ALT hos disse pasientene. Det bør imidlertid bemerkes at denne meta-analysen var begrenset av en manglende evne til å utelukke en manglende evne til å utelukke effekter av tiltak som involverer livsstilsendringer, trening og bruk av andre antioksidanter og en manglende evne til å utelukke effekter av andre risikofaktorer for kronisk leversykdom som alkohol-og narkotikabruk.i tillegg til dette må heterogeniteten i studiene tas i betraktning da den begrenser den samlede analysen samt har mindre spesifisitet for aminotransferasenivåer enn biopsier tatt på tidspunktet for diagnose og vurdering av leversykdom (28).
selv om vi blant de store studiene for å vurdere effekten av bruk av vitamin E hos pasienter MED NASH ikke har funnet statistisk signifikante forskjeller med bruk av placebo og andre terapeutiske alternativer på kort sikt, er det bekymring for mulige bivirkninger av langvarig bruk Av Vitamin E.
en systematisk oversikt over ni randomiserte inkluderte nye randomiserte placebokontrollerte studier for å evaluere effekten av vitamin E i en periode på minst ett år på den totale forekomsten av cerebrovaskulære ulykker samt subtyper av cerebrovaskulære ulykker. Det fant en økt risiko for hemorragisk slag (RR = 1,22, 95% CI: 1,0 til 1,48, p = 0,045). På grunn av resultatene fra deres gjennomgang anbefaler forskerne å unngå diskriminerende bruk av vitamin E på grunn av de alvorlige konsekvensene av hemorragiske slag i sykelighet og dødelighet (29).
en randomisert placebokontrollert studie som inkluderte 35 533 pasienter fulgt i minst syv år har studert risikoen For Vitamin E relatert til prostatakreft. Det sammenlignet en placebogruppe med en gruppe som fikk vitamin E i en daglig dose på 400 IE. Det var en signifikant økning i risikoen for prostatakreft blant De som tok Vitamin E (HR 1,17; 99% CI, 1,004-1,360; p = 0,008). Den absolutte økningen i risiko var 1,6 per 1000 personår (30).
En annen meta-analyse har sett på dose-respons-forholdet mellom Vitamin E-tilskudd og total dødelighet hos voksne. Det viste at pasienter som får høye doser vitamin E (større enn eller lik 400 IE / dag) hadde økt dødelighet fra alle årsaker. Denne metaanalysen begrenset søket til randomiserte kontrollerte studier der pasientprøver besto av voksne som fikk behandling med vitamin E alene eller i kombinasjon med andre vitaminer eller mineraler, og som ekskluderte gravide kvinner og som hadde minst 1 års behandling og monitorering. Resultatene fra denne metaanalysen bør vurderes med forsiktighet fordi flere av studiene har små utvalgsstørrelser og ble utført blant pasienter med flere kroniske sykdommer. Dette begrenser studiens evne til å generalisere resultater til den friske voksne befolkningen (31).
KONKLUSJON
selv om det for tiden ikke er noen effektiv legemiddelbehandling for pasienter MED NASH, tyder bevisene vist i PIVENS-studien på at riktig administrasjon av vitamin E forbedrer leverhistologien hos voksne ikke-cirrhotiske pasienter MED NASH som ikke har diabetes. Likevel er det behov for flere studier før denne anbefalingen kan utvides til diabetespasienter eller til pasienter som har cirrhose med NASH. Studier utført på pediatriske pasienter MED NASH har ikke funnet tilstrekkelig bevis for å støtte bruken av vitamin e. i tillegg til administrering Av Vitamin E har det vist seg at vekttap reduserer steatose og leverbetennelse. Vekttap gjennom lavt kalori diett kombinert med økt fysisk aktivitet bør anbefales for alle pasienter. Når det gjelder bivirkninger, har vi ikke funnet statistisk signifikante forskjeller i kortvarig bruk av vitamin E med placebo og andre behandlingsalternativer. Likevel er ukritisk bruk Av Vitamin E ikke anbefalt i lange perioder, da det er bevis som tyder på økt risiko for prostatakreft, hemorragisk slag og død fra alle årsakene.
1. Abbas AK, Fausto N. H@gado, varí biliar og hryvnas biliares. En: Robbins SL, Mitchell RN, Kumar V, Abbas AK, Fausto N. Patologí funcional y Estructural. 8va Utg. Barcelona: Elsevier; 2012. s. 645-687.
2. Brunt E, Neuschwander-Tetri B, Burt AD. Fatty leversykdom: alkoholisk og alkoholfri. En: Burt AD, Ferrell, L Portmann BC. MacSween Er Patologi I Leveren. 6. utgave. STORBRITANNIA: Elservier; 2012. s. 293-359.
3. Corrado RL, Torres DM, Harrison SA. Gjennomgang Av Behandlingsmuligheter for Ikke-Alkoholisk Fettleversykdom. Med Clin N Am 2014; 98: 55-72.
4. Koek GH, Liedorp PR, Bast A. rollen av oksidativt stress i ikke-alkoholisk steatohepatitt. Clinica Chimica Acta 2011; 412: 1297-1305.
5. Ermelinda Camilo M. Ikke-alkoholisk fettleversykdom / ikke-alkoholisk steatohepatitt (NAFLD/NASH): diagnose og klinisk kurs. Beste Praksis & Forskning Klinisk Gastroenterologi 2004; 18(6): 1089-104.
6. Mishra A, Younossi ZM. Epidemiologi Og Naturhistorie Av Ikke-alkoholisk Fettleversykdom. Journal Of Klinisk Og Eksperimentell Hepatologi 2012; 2 (2): 135-44.
7. Rolo AP, Teodoro JS, Palmeira CM. Rolle av oksidativt stress i patogenesen av ikke-alkoholisk steatohepatitt. Gratis Radic Biol Med 2012; 52 (1): 59-69.
8. Machado MV, Cortez-Pinto H. Ikke-invasiv diagnose av alkoholfri fettleversykdom. En kritisk vurdering. Tidsskrift For Hepatologi 2013; 58 (5): 1007-19.
9. Jens m, et al. Diagnose Og Behandling Av Ikke-Alkoholisk Fettleversykdom: Praksis Retningslinje Av American Association For Study Of Liver Diseases, American College Of Gastroenterology, Og American Gastroenterological Association. Hepatologi 2012; 55.
10. Mazzella N, Ricciardi LR, Mazzotti A, Marchesini G. Rollen Av Medisiner For Behandling Av Pasienter MED NAFLD. Clin Lever Dette 2014; 18: 73-89.
11. Chunga MIN, Yeunga SF, Parka HJ, Volekb JS, Brunoa RS. Kosttilskudd α-og γ-tokoferoltilskudd demper lipopolysakkaridindusert oksidativt stress og betennelsesrelatert respons i en overvektig musemodell av ikke-alkoholisk steatohepatitt. Journal Of Nutritional Biochemistry 2010; 21: 1200-1206.
12. Dag CP, James AV. Steatohepatitis: en fortelling om to ‘treff’? Gastroenterologi 1998; 114: 842-4.
13. Harper HA, Murray RK, Rodwell VW, Bender DA. Bioquí ilustrada, 28 utg. Mé: McGraw-Hill Interamericana; 2010. s. 484-485.
14. Neuschwander-TETRI BA. Hepatisk lipotoksisitet og patogenesen av ikke-alkoholisk steatohepatitt: den sentrale rollen til ikke -riglyseridfettsyremetabolitter. Hepatologi 2010; 52 (2): 774-88.
15. Le T, Loomba R. Behandling Av Ikke-alkoholisk Fettleversykdom og Steatohepatitt. Journal Of Klinisk Og Eksperimentell Hepatologi 2012; 2: 156-173.
16. Verdam FJ, Dallinga JW, Driessen, De Jonge C, Moonen E, van Berkel J, Luijk J, Bouvy ND, Buurman AW, Rensen SS, Greve JW. Ikke-alkoholisk steatohepatitt: en ikke-invasiv diagnose ved analyse av utåndet pust. Tidsskrift For Hepatologi 2013; 58: 543-548.
17. B, de Sio I, La Mura V, et al. Rollen av lyse lever ekko mønster på ultralyd B-mod undersøkelse i diagnostisering av leveren steatosis. Grave Lever Dis 2006; 38: 485-9.
18. Aj, et al. Pioglitazon versus vitamin e versus placebo for behandling av ikke-diabetespasienter med alkoholfri steatohepatitt: pivens studiedesign. Contemp Clin Trials 2009; 30 (1): 88-96.
19. A. v., A. V., A. v., a. v., A. v., a. v., A. v., A. v., A. v., a. v., a. v., a. v., a. v., et al. Pioglitazon, vitamin e eller placebo for ikke-alkoholisk steatohepatitt. N Engl J Med 2010; 362 (18): 1675-85.
20. Hoofnagle JH, Van Natta ML, Kleiner DE, Clark JM, Kowdley KV, Loomba R, et al. Vitamin E og endringer i serumalaninaminotransferasenivåer hos pasienter med ikke-alkoholisk steatohepatitt. Aliment Pharmacol Ther 2013; 38 (2): 134-43.
21. Lavine JE, Schwimmer JB, Molleston JP, Scheimann AO, Murray KF, Abrams sh, et al. Behandling av alkoholisk fettleversykdom hos barn: TONIC trial design. Contemp Clin Trials 2010; 31 (1): 62-70.
22. Lavine JE, Schwimmer JB, Van Natta ML, et al. Effekt av vitamin e eller metformin for behandling av ikke-alkoholisk fettleversykdom hos barn og ungdom: tonic randomisert kontrollert studie. JAMA 2011; 305 (16): 1659-68.
23. M. a., M. A., M. A., M. A., M. A., M. a., m. a., m. a., m. a., m. a., et al. Effekter av vitamin e-behandling på peroksisomproliferatoraktivert reseptor-alfa-uttrykk og insulinresistens hos pasienter med ikke-alkoholisk steatohepatitt: resultater fra en pilotstudie. Intern Med J 2007; 37 (4): 229-35.
24. Vajro P, Mandato C, Franzese A, Ciccimarra E, Lucariello S, Savoia M, et al. Vitamin e behandling i pediatrisk fedme-relatert leversykdom: en randomisert studie. J Pediatr Gastroenterol Nutr 2004; 38(1): 48-55
25. Jens m, et al. Ni scoring modeller for kortsiktig dødelighet i alkoholisk hepatitt: kryssvalidering i en biopsi-bevist kohort. Aliment Pharmacol Ther 2014; 39: 721-732.
26. Kugelmas M, Hill DB, Vivian B, Marsano L, McClain CJ. Cytokiner OG NASH: en pilotstudie av effektene av livsstilsendring og vitamin e. Hepatologi 2003; 38 (2): 413-9.
27. Younossi ZM, Reyes MJ, Mishra MA, Mehta R, Henry L. Systematisk gjennomgang med meta-analyse: ikke-alkoholisk steatohepatitt – et tilfelle for personlig behandling basert på patogene mål. Aliment Pharmacol Ther2014; 39: 3-14.
28. Ji HF, et al. Effekt av vitamin e-tilskudd på aminotransferasenivåer hos pasienter MED NAFLD, NASH og CHC: Resultater Fra en meta-analyse. Ernæring 2014; 1-6.
29. Markus S, Robert JG, Pamela MR, Christophe T, Tobias K. Effekter av vitamin E på stroke subtyper: meta-analyse av randomiserte kontrollerte studier. BMJ 2010; 341.
30. Klein EA, Thompson IM, Tangen CM, et al. Vitamin e og risikoen for prostatakreft: selen og vitamin e cancer prevention trial (select). JAMA 2011; 306 (14): 1549-56.
31. Miller ER, 3rd, Pastor-Barriuso R, Dalal D, Riemersma RA, Appel LJ, Guallar E. Meta-analyse: høy dosering vitamin E-tilskudd kan øke all-årsak dødelighet. Ann Intern Med 2005; 142(1): 37-46.