Dimethyl Sulfoxide Oxidations
Dimethyl sulfoxide-based oxidation of primary alcohols to aldehydes or secondary alcohols to ketones is a mild method that does not depend upon heavy metal oxidants. Here is a brief, chronological history of the procedure.
Index:
-
Swern Oxidation (trifluoroacetic anhydride)
-
Swern Oxidation (oxalyl chloride)
Kornblum Oxidation: (1959) pierwotny tosylan jest podgrzewany w temperaturze 150o, aby spowodować przemieszczenie SN2 przez tlen sulfotlenku dimetylu (DMSO) w obecności NaHCO3. Zaakceptowanym mechanizmem była wówczas eliminacja E2, jak pokazano. Siarczek dimetylu (DMS) jest produktem redukcji reakcji. Praca ta utworzyła tosylan z jodku alkilu z tosylanem srebra. Prawdopodobnie tosylan można przygotować z alkoholu, który jest bardziej bezpośrednią drogą. Minusem zabiegu jest podwyższona temperatura, chociaż czas kontaktu wynosi zaledwie kilka minut. Zasadniczą kwestią jest znalezienie metody wytwarzania soli siarczanowej.

modyfikacja Bartona: (1964) Barton i współpracownicy byli w stanie wytworzyć sole siarczanowe przez traktowanie chloro mrówczanów alkilowych DMSO z utratą CO2. Dodatek trietyloaminy wytwarza produkt utleniania. Procedura ta poprawiła trudne warunki procedury Kornbluma. Ponadto chloro mrówczan jest łatwo dostępny przez obróbkę alkoholu, który ma być utleniony z nadmiarem fosgenu.

Utlenianie Moffatt-Pfitzner: (1963) ten wariant utleniania na bazie dimetylosulfotlenku został opracowany w firmie Syntex. Aktywator Wytwarza się przez protonację dicykloheksylo-karbodiimidu (1, DCC), który jest atakowany przez sulfotlenek dimetylu. Pośredni 2 jest ponownie protonowany, aby ułatwić dodanie tlenu alkoholowego do atomu siarki. Stabilny mocznik dicykloheksylowy 4 tworzy się wraz z solą siarczanową 3. Gatunek ten ulega rozpadowi na związek karbonylowy pod wpływem anionu diwodorofosforanowego. Chociaż kwas fosforowy jest skutecznym katalizatorem kwasowym dla tej reakcji, kwas siarkowy, chlorek wodoru i kwas trifluorooctowy nie są. Jednak trifluorooctan pirydyniowy jest skutecznym katalizatorem. Kluczowe znaczenie ma to, aby sprzężona zasada kwasu była na tyle zasadowa, aby wywołać ostatni etap reakcji.

Mechanizm Torrsella: (1966) Szwedzki chemik Torrsell wykazał, że mechanizm tych utlenień opartych na DMSO nie przebiega poprzez międzycząsteczkową eliminację β. Eliminacja jest procesem wewnątrzcząsteczkowym. Sól siarczanową 5 otrzymano metodą Moffatta-Pfitznera (patrz wyżej). Gdyby zastosowano mechanizm Kornbluma, otrzymany siarczek dimetylu byłby pozbawiony deuteru (eksperyment 1). Otrzymano jednak siarczek dimetylu-d1 (7). Wynik ten jest zgodny z zasadą, która deprotonuje grupę metylową przyłączoną do siarki tworząc ylid 6. Ylid rozkłada się poprzez wewnątrzcząsteczkową deprotonację w celu wytworzenia obserwowanych produktów.
1:

aby potwierdzić ten mechanizm, Deuter został włączony do DMSO jako DMSO-d6. W związku z tym w reakcji otrzymano siarczek dimetylu-d5(12) i nieutwardzony aldehyd 11 (eksperyment 2).
2:

utlenianie Parikh-Doeringa: (1967) to utlenianie wykorzystuje kompleks trójtlenku siarki pirydynowej (13) jako aktywator sulfotlenku dimetylu. Siarczan jest grupą opuszczającą w wyparciu przez alkohol (pierwotny lub wtórny) w pośrednim 14. Sulfenian 15 rozkłada się za pomocą mechanizmu wewnątrzcząsteczkowego (vide supra), otrzymując aldehyd lub keton.

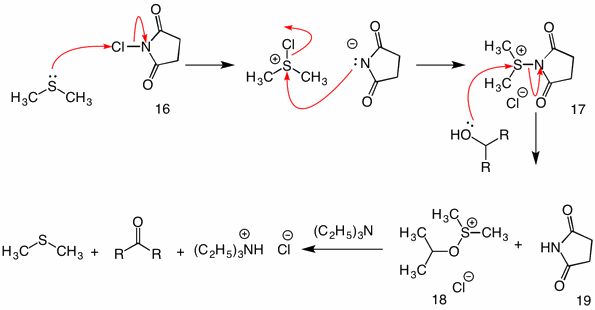
Corey-Kim: (1972) w tej procedurze siarczek dimetylu aktywuje się (utlenia) N-chlorosukcynimidem (16), aby uzyskać odczynnik 17. W reakcji tego gatunku z alkoholem Grupa sukcynimidylowa funkcjonuje jako grupa opuszczająca. Zwykły związek pośredni sulfonianu 18 rozpada się za pomocą mechanizmu wewnątrzcząsteczkowego po dodaniu trietyloaminy.
utlenianie Swerna: (1976)to wczesne utlenianie Swerna wykorzystuje bezwodnik trifluorooctowy (20) w-50oC do aktywacji dimetylosulfotlenku. Dodanie alkoholu do półproduktu 21 daje pożądany siarczan 22. Keton lub aldehyd jest wytwarzany w zwykły sposób z trietyloaminą.

utlenianie Swerna: (1978) ta późniejsza procedura Swerna jest wygodną metodą wytwarzania odczynnika 24 bez użycia siarczku dimetylu i chloru. Sulfotlenek dimetylu, który znajduje się na tym samym poziomie utleniania co sól 24, reaguje z chlorkiem oksalylu (23), uwalniając tlenek węgla, dwutlenek węgla i odczynnik 24. Dodanie alkoholu pierwotnego lub wtórnego, a następnie deprotonacja sulfonianu 25 trietyloaminą prowadzi do uzyskania odpowiednio pożądanego aldehydu lub ketonu.
