Dimethyl Sulfoxide Oxidations
Dimethyl sulfoxide-based oxidation of primary alcohols to aldehydes or secondary alcohols to ketones is a mild method that does not depend upon heavy metal oxidants. Here is a brief, chronological history of the procedure.
Index:
-
Swern Oxidation (trifluoroacetic anhydride)
-
Swern Oxidation (oxalyl chloride)
Kornblum Oxidation: (1959) ett primärt tosylat upphettas vid 150o för att orsaka SN2-förskjutning av syret av dimetylsulfoxid (DMSO) i närvaro av NaHCO3. Den accepterade mekanismen vid den tiden var en E2-eliminering som visat. Dimetylsulfid (DMS) är reduktionsprodukten av reaktionen. Detta arbete bildade tosylatet från alkylodiden med silvertosylat. Förmodligen kan tosylatet framställas från alkoholen som är en mer direkt väg. Nackdelen med proceduren är den förhöjda temperaturen även om kontakttiden bara är några minuter. Den väsentliga frågan är att hitta en metod för att generera sulfenatsaltet.

Barton modifiering: (1964) Barton och medarbetare kunde generera sulfenatsalter genom att behandla alkylkloroformater med DMSO med förlust av CO2. Tillsats av trietylamin genererar oxidationsprodukten. Detta förfarande förbättrade de hårda förhållandena i Kornblum-förfarandet. Dessutom är kloroformatet lätt tillgängligt genom behandling av alkoholen som ska oxideras med överskott av fosgen.

Moffatt-Pfitzner Oxidation: (1963) denna variant av en dimetylsulfoxidbaserad oxidation utvecklades vid Syntex. Aktivatorn framställs genom protonation av dicyklohexylkarbodiimid (1, DCC), som attackeras av dimetylsulfoxid. Intermediate 2 protoneras igen för att underlätta tillsats av alkoholsyret på svavelatomen. Stabil dicyklohexylkarbamid 4 bildas tillsammans med sulfenatsalt 3. Denna art lider kollaps till karbonylföreningen under påverkan av dihydrogenfosfatanjonen. Även om fosforsyra är en effektiv syrakatalysator för denna reaktion, är svavelsyra, väteklorid och trifluorättiksyra inte. Pyridiniumtrifluoroacetat är emellertid en effektiv katalysator. Det är kritiskt att den konjugerade basen av syran är basisk nog för att åstadkomma det sista steget i reaktionen.

Torrsell Mechanism: (1966) den svenska kemisten Torrsell visade att mekanismen för dessa DMSO-baserade oxidationer inte går vidare via en intermolekylär uteslutning av mikrober. Elimineringen är en intramolekylär process. Sulfenatsalt 5 framställdes genom Moffatt-Pfitzner-förfarandet (se ovan). Om Kornblummekanismen skulle tillämpas skulle den erhållna dimetylsulfiden sakna deuterium (Experiment 1). Emellertid erhölls dimetylsulfid-d1 (7). Detta resultat överensstämmer med en bas som deprotonerar metylgruppen bunden till svavelbildande ylid 6. Ylid sönderdelas genom intramolekylär deprotonation för att producera de observerade produkterna.
Experiment 1:

för att bekräfta denna mekanism införlivades deuterium i DMSO som DMSO-d6. Följaktligen producerade reaktionen dimetylsulfid-d5 (12) och undeuterad aldehyd 11 (Experiment 2).
Experiment 2:

Parikh-Doering Oxidation: (1967) denna oxidation använder pyridin svaveltrioxidkomplexet (13) som aktivator av dimetylsulfoxid. Sulfat är den lämnande gruppen i förskjutningen av alkoholen (primär eller sekundär) i mellanliggande 14. Sulfenat 15 sönderdelas av den intramolekylära mekanismen (vide supra) för att ge en aldehyd eller keton.

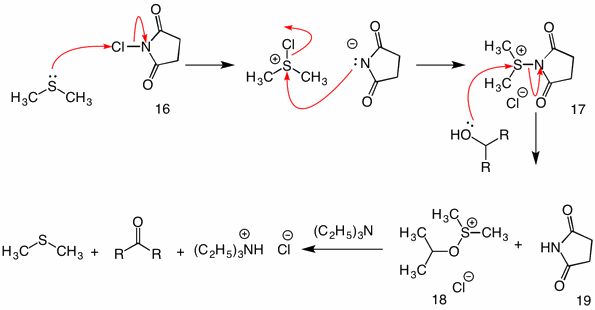
Corey-Kim Oxidation: (1972) i detta förfarande aktiveras dimetylsulfid (oxideras) med N-klorsuccinimid (16) för att tillhandahålla reagens 17. I reaktionen av denna art med en alkohol fungerar succinimidylgruppen som en lämnande grupp. Den vanliga sulfenat mellanliggande 18 kollapsar av den intramolekylära mekanismen vid tillsats av trietylamin.
Swern Oxidation: (1976) denna tidiga Swern oxidation använder trifluorättiksyraanhydrid (20) vid-50oC för att aktivera dimetylsulfoxid. Tillsats av alkoholen till mellanliggande 21 ger det önskade sulfenatet 22. Ketonen eller aldehyden produceras på vanligt sätt med trietylamin.

Swern Oxidation: (1978) detta senare Swern-förfarande är en bekväm metod för framställning av reagens 24 utan användning av dimetylsulfid och klor. Dimetylsulfoxid, som har samma oxidationsnivå som salt 24, reagerar med oxalylklorid (23) för att frigöra kolmonoxid, koldioxid och reagens 24. Tillsats av den primära eller sekundära alkoholen följt av deprotonering av sulfenat 25 med trietylamin leder till den önskade aldehyden respektive ketonen.
