Bakgrund
Hashimotos encefalopati (HE) är ett sällsynt neuropsykiatrisk syndrom associerat med sköldkörtelantikroppar och rapporterades först av hjärnan 1996 (Brain et al., 1966). Han presenterar ett brett spektrum av kliniska symtom, inklusive neurologiska manifestationer som strokeliknande episoder, anfall, förvirring, myoklonus, ataxi, tremor och demens, samt psykiatriska manifestationer, inklusive akut psykos, depressiva störningar, personlighetsförändringar, hallucinationer och schizofreni (Kirshner, 2014; Menon et al., 2017). I denna fallrapport beskriver vi en patient med Han vars kliniska symtom och laboratorietestresultat efterliknade viral encefalit.
fallrapport
en 59-årig man som presenterade feber, huvudvärk och besvärligt tal som specifikt manifesterades som långsamt och oklart tal, togs in på sjukhuset. Han förnekade nyligen infektioner som influensa eller gastroenterit, resor och andra möjliga orsaker, som kan vara ansvariga för febern, som toppade vid 39,5 kg C. tidigare medicinsk historia avslöjade gikt i 20 år, men inga läkemedel föreskrevs. Hans neurologiska undersökning och kranial datortomografi (CT) och magnetisk resonansavbildning (MRI) (Figur 1) skanningar var normala. EEG-resultat visade mindre oregelbundenheter i vågor (5-20 oc 14-20 Hz OC) som emitterades från de bilaterala halvkärmarna. Blod rutin, C-reaktivt protein, serum vitamin B12, och folsyra, liksom andra autoimmunitet beslutsfattare innehållande antinuclear antikropp (ANA), Anti-neutrofila cytoplasmatiska antikroppar (ANCA), och reumatoid faktorer var alla utmärker. Cerebrospinalvätskan (CSF) visade ett ökat antal vita blodkroppar (WBC) (104 106/L, referensintervall 0-8 10^6/l) och förhöjda proteinnivåer (1,68 g/L, referensintervall 0,15–0,45 g/L). Kultur -, smet-och bakterie -, svamp -, virus-och tuberkelbacillusantikroppar i serum och CSF var negativa. Han diagnostiserades med viral encefalit och behandlades med antivirala medel. Hans symptom lättade inom en vecka och han släpptes från sjukhuset. Fem månader senare hänvisades han till vårt sjukhus igen på grund av en feber på 38, 5 kcal C och tillfällig meningsförvirring. En annan ländryggspunktur utfördes; CSF hade ett WBC-antal på 39 10 ^ 6 / l och proteininnehållet var 1,32 g/L. De kraniala MR-och laboratorietestfynden var nästan normala förutom minskad sköldkörtelfunktion och ökade ata-nivåer (anti-thyroid autoantikropp) i serum och CSF. De initiala resultaten var följande: i serum var koncentrationen av sköldkörtelstimulerande hormon (TSH) 43,39 uIU/ml (referensområde (rr): 0,27–4,2 uIU/ml), fri triiodotyronin (FT3) koncentration var 2,89 pmol/ml (RR: 3,1–6,8 pmol/ml), fri tyroxin (FT4) koncentration var 7,18 pmol/ml (RR: 12,0–22,0 pmol/ml) var den totala koncentrationen av trijodtyronin (TT3) 1,17 pmol/ml (rr: 1,3–3.1 pmol/ml), and total thyroxine (TT4) concentration was 44.26 pmol/ml (RR: 66–181 pmol/ml); the titer of anti-thyroglobulin autoantibodies (TgAb) was 1274 IU/ml (RR: < 115 IU/ml) and the titer of anti-thyroperoxidase autoantibodies (TPOAb) was 600 IU/ml (RR: < 35 IU/ml). In the CSF, ATA was positive (TPOAb 17.06 IU/ml, TgAb 16.02 IU/ml). Ultrasound imaging indicated diffuse lesions of the thyroid. Antikroppsanalys av anti-NMDAR, AMPA1, AMPA2, LGI1, CASPR2, GABA, GAD, anti-Hu, Yo, Ri, MAI, MA2, CV2, Amphiphysin, SOX-1, Tr, Zic4 och GAD65 var alla negativa i både serum och CSF. Patienten diagnostiserades slutligen med HE, Hashimotos thyroidit och hypothyroidism och föreskrev metylprednisolon och Euthyrox. Metylprednisolon startades i en dos av 80 mg/dag i 1 vecka och reducerades till 40 mg / dag under 2-veckan; därefter föreskrevs oral prednisolon, som avvänjdes med en hastighet av 5 mg per vecka, det vill säga oral prednisolon användes i totalt 8 veckor. Hans symtom lindrades om 3 dagar. Patienten förblev frisk under en uppföljningsperiod på 1 år.
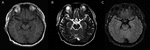
Figur 1. MR-avbildning av hjärnan. Det finns inga onormala fynd i hjärnan MR-avbildning av patienten. (A) T1-viktad Bild; (B) T2-viktad bild; (C) FLAIR-bild.
diskussion
den beräknade prevalensen för HE är 2,1 av 100 000 och könsförhållandet (kvinna till man) är 4:1 (Ferracci et al., 2004). Han kan vara progressiv, återfallande remitterande eller till och med självbegränsande. I det aktuella fallet verkade patienten ha en återfallande förlöpande kurs.
i kombination med patientens symtom, normala MR-resultat, höga titrar av ATA i serum och ata-positivitet hos CSF diagnostiserades patienten slutligen med HE efter att ha uteslutit andra potentiella orsaker inklusive stroke, tumör, infektion i centrala nervsystemet, autoimmun encefalit och paraneoplastiskt syndrom.
Sammantaget är patofysiologin hos HE fortfarande ofullständig. På grundval av de neuropatologiska fynden har en autoimmun vaskulit-mekanism föreslagits. I en tidigare studie avslöjade hjärnbiopsier att lymfocytisk infiltration runt venulerna och arteriolerna kan vara involverad (Duffey et al., 2003). En annan möjlig mekanism som är involverad är att ATAs attackerar antigener som delas av sköldkörteln och hjärnan, och av denna anledning höga titrar av ATAs inklusive tpoab, TgAb och anti-TSH-receptor (TSH-R) antikroppar i serum, och ibland i CSF, anses vara kännetecken för HE (Yoneda, 2018). På samma sätt hittades höga titrar av ATA och CSF-ata i vårt fall. I en tidigare studie resulterade plasmautbytesterapi i en djupgående förbättring av patienternas symtom (Tran et al., 2018). Tillsammans, dessa resultat tyder på att ATA spelar en viktig roll i HE. Förhöjda ata-nivåer i serum finns emellertid också inom den allmänna befolkningen och är särskilt vanliga hos äldre individer. Vidare är omfattningen av ATA-höjd inte relaterad till svårighetsgraden av HE. Även om patienternas serum ata-nivåer fortfarande var höga efter metylprednisolonbehandling, löstes hans symtom (titer av anti-thyroglobulin autoantikroppar( TgAb): 041 IE/ ml, RR: < 115 IE/ml; titer av autoantikroppar mot tyroperoxidas (TPOA): 600 IE/ml, RR: <35 IE/ml). Våra resultat bekräftar att det inte finns något samband mellan omfattningen av ATA-höjning och svårighetsgraden av HE.
även om korrelationen mellan ATA och HE fortfarande är oklar (Kirshner, 2014), föreslogs diagnostiska kriterier för HE av ett team av experter inom Lancet Neurology 2016. Kriterierna är följande: (1) encefalopati med anfall, myoklonus, hallucinationer eller strokeliknande episoder; (2)subklinisk eller mild öppen sköldkörtelsjukdom (vanligtvis hypotyreos); (3) normala fynd eller icke-specifika avvikelser som visas av MR i hjärnan; (4) närvaro av sköldkörtelantikroppar i serum (sköldkörtelperoxidas, tyroglobulin); (5) frånvaro av väl karakteriserade neuronala antikroppar i serum och CSF; och (6) rimlig uteslutning av alternativa orsaker. Han kan diagnostiseras om en patient uppfyller alla kriterier (Graus et al., 2016). Vår patient uppfyllde alla ovanstående kriterier, och han kunde därför diagnostiseras med HE. De flesta patienter med HE svarar bra på steroider; men när patienter är steroidresistenta har andra immunsuppressionsterapier inklusive plasmautbyte, IVIG, metotrexat och mykofenolat visat sig vara effektiva. Höga doser metylprednisolon (500-1000 mg) används oftast. Eftersom patienten visade milda symtom och vägrade användning av hög dos metylprednisolon, föreskrev vi en låg dos metylprednisolon. Vår patient genomgick steroidbehandling och har sedan dess varit frisk. Patienten fick inga andra immunterapibehandlingar under uppföljningen. I en retrospektiv observationsstudie utförd av Mamoudjy et al. (2013) forskningsresultaten visade att vissa HE-patienter genomgick ett återfall, till och med en tredje attack, som hade en kortare intervalltid (medelvärde 18 dagar) jämfört med den andra attacken (medelvärde 213 dagar). Patienter med återfall behövde metylprednisolon eller immunsuppressiv terapi igen (Mamoudjy et al., 2013). Vår patient drabbades av ett återfall cirka 150 dagar efter den första attacken och steroidterapi var effektiv. Följder, såsom huvudvärk, minnesstörningar och så vidare, var också frekventa (Mamoudjy et al., 2013), men vår patient hade inga följder kvar lyckligtvis.
Hashimotos encefalopati är svår att diagnostisera exakt på grund av dess samband med ett brett spektrum av kliniska symtom, liksom dess icke-specifika neuroimaging och elektroencefalogrampresentation. En tidigare artikel rapporterade ett fall av HE som ursprungligen feldiagnostiserades som viral encefalit (han et al., 2013), där patienten presenterade progressivt nedsatt kognitiv funktion och okontrollerade anfall utan feber. I vårt fall leder det ökade WBC-antalet och CSF-proteinet i kombination med feber och huvudvärk oss att diagnostisera det som viral encefalit. Feber har beskrivits hos flera patienter med HE med och utan sköldkörtelstörningar (Huang et al., 2011; Lu et al., 2015). Även om orsaken till feber i Han är oklar, Lu et al. (2015) föreslog att det kan vara ett direkt resultat av inflammation i kombination med autoimmun vaskulit.
Hashimotos encefalopati kan manifestera sig på många olika sätt, inklusive strokeliknande episoder, anfall, förvirring, myoklonus, akut psykos, depressiva störningar och hallucinationer, vilket gör att han förväxlas med andra sjukdomar. Uwatoko et al. (2018) rapporterade ett fall av en patient som presenterade parkinsonism och en tumörliknande lesion avslöjad av hjärnan Mr. Efter biopsi fann man att lesionen inte var en tumör, och han bekräftades äntligen (Uwatoko et al., 2018). Patienter med HE kan också uppvisa ovanliga symtom som pseudobulbar pares, sensorimotorisk polyneuropati, katatoniska symtom, svindel, muskelsvaghet, chorea, opsoclonus och huvudvärk av trigeminal neuralgi, bland andra (Beckmann et al., 2011; Salazar et al., 2012; Sharan et al., 2015; Ueno et al., 2016; Karthik et al., 2017; Emeksiz et al., 2018; Oz Tuncer et al., 2018). Snabbt progressiv demens, som en vanlig manifestation av HE, gör det nödvändigt att skilja HE från andra sjukdomar orsakade av vaskulära, infektiösa, toxisk-metaboliska och autoimmuna faktorer, metastas/neoplasi, iatrogena/medfödda fel i ämnesomsättningen, neurodegenerativa sjukdomar och systemiska sjukdomar/anfall (Paterson et al., 2012).
slutsats
Sammanfattningsvis är diagnosen HE ganska komplex men värdefull på grund av dess dramatiska svar på immunsuppressiv terapi. När kliniker står inför oförklarlig encefalit bör sköldkörtelfunktion och ata-nivåer betraktas som konventionella tester. Han kan uteslutas som diagnos för patienter med normala serumnivåer av ata. För patienter med ökade nivåer av ATA bör han övervägas efter att ha uteslutit andra möjliga sjukdomar.
datatillgänglighet uttalande
de dataset som genereras för denna studie är tillgängliga på begäran till motsvarande författare.
Etikuttalande
studierna med mänskliga deltagare granskades och godkändes av Etikutskottet för det första sjukhuset vid Jilin University, Kina. Patienterna / deltagarna gav sitt skriftliga informerade samtycke till att delta i denna studie. Skriftligt informerat samtycke erhölls från individen (erna) för publicering av potentiellt identifierbara bilder eller data som ingår i denna artikel.
Författarbidrag
HM bidrog till utformningen och utformningen av manuskriptet. Min skrev det första utkastet till manuskriptet. YY, XM, YX och NS skrev delar av manuskriptet. Alla författare bidrog till manuskriptrevision, läste och godkände den inlämnade versionen.
finansiering
detta arbete stöddes av National Key R&D-programmet i Kina (nr 2017yfc0110304).
intressekonflikt
författarna förklarar att forskningen genomfördes i avsaknad av kommersiella eller finansiella relationer som kan tolkas som en potentiell intressekonflikt.
Beckmann, YY, topp, D. och Yigit, T. (2011). Ovanliga presentationer av Hashimotos encefalopati: trigeminal neuralgiform huvudvärk, skev avvikelse, hypomani. Endokrina 40, 495-496. doi: 10.1007 / s12020-011-9506-X
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Brain, L., Jellinek, E. H. och Ball, K. (1966). Hashimotos sjukdom och encefalopati. Lancet 2, 512-514.
Google Scholar
Duffey, P., Yee, S., Reid, I. N. och Bridges, L. R. (2003). Hashimotos encefalopati: postmortemfynd efter dödlig status epilepticus. Neurologi 61, 1124-1126.
PubMed Abstrakt / Google Scholar
Emeksiz, S., Kutlu, N. O., Alacakir, N. och Caksen, H. (2018). Ett fall av steroidresistens Hashimotos encefalopati som presenterar sensorimotorisk polyneuropati. Turk. J. Pediatr. 60, 310–314. doi: 10.24953 / turkjped.2018.03.012
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Ferracci, F., Bertiato, G. och Moretto, G. (2004). Hashimotos encefalopati: epidemiologiska data och patogenetiska överväganden. J. Neurol. Sci. 217, 165–168.
PubMed Abstrakt / Google Scholar
han är en av de mest kända och mest kända i världen. (2016). Ett kliniskt tillvägagångssätt för diagnos av autoimmun encefalit. Lancet Neurol. 15, 391–404.
Google Scholar
Han, L., Li, M., lång, XH, Li, XP och Peng, Y. (2013). Ett fall av Hashimotos encefalopati feldiagnostiserad som viral encefalit. Är. J. Fall Rep. 14, 366-369.
Google Scholar
Huang, W., Xia, C. och Chatham, M. (2011). Infektionssjukdom eller Hashimotos encefalopatifläckar: en fallrapport. Beslag 20, 717-719. doi: 10.1016/j.beslag.2011.04.011
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Karthik, ms, Nandhini, K., Subashini, V. och Balakrishnan, R. (2017). Hashimotos encefalopati uppvisar ovanliga beteendestörningar hos en ung flicka. Case Rep. Med. 2017, 3494310. doi: 10.1155/2017/3494310
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Kirshner, H. S. (2014). Hashimotos encefalopati: en kort recension. Curr. Neurol. Neurovetenskap. Rep. 14: 476.
Google Scholar
Lu, T., Zhou, Z., Wu, A., Qin, B. och Lu, Z. (2015). Febril Hashimotos encefalopati associerad med Hashitoxikos. Acta Neurol. Belg. 115, 811–813.
Google Scholar
han är en av de mest kända och mest kända i världen. (2013). Hashimotos encefalopati: identifiering och långsiktigt resultat hos barn. EUR. J. Paediatr. Neurol. 17, 280–287. doi: 10.1016/j.ejpn.2012.11.003
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Menon, V., Subramanian, K. och Thamizh, J. S. (2017). Psykiatriska presentationer förebådar Hashimotos encefalopati: en systematisk genomgång och analys av fall som rapporterats i litteraturen. J. Neurosci. Landsbygd. Pract. 8, 261–267. doi: 10.4103/jnrp.jnrp_440_16
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Oz Tuncer, G., Teber, S., Kutluk, M. G., Albayrak, P. och Deda, G. (2018). Hashimotos encefalopati presenteras som pseudobulbar pares. Childs Nerv. Syst. 34, 1251–1254. doi: 10.1007 / s00381-018-3720-2
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Paterson, RW, Takada, Lt och Geschwind, MD (2012). Diagnos och behandling av snabbt progressiva demens. Neurol Clin. Pract. 2, 187–200.
PubMed Abstrakt / Google Scholar
Salazar, R., Mehta, C., Zaher, N. och Miller, D. (2012). Opsoclonus som en manifestation av Hashimotos encefalopati. J. Clin. Neurovetenskap. 19, 1465–1466. doi: 10.1016 / j. jocn.2012.02.012
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Sharan, A., Sengupta, S., Mukhopadhyay, S. och Ghosh, B. (2015). Hashimotos encefalopati presenterar med Chorea. J. Assoc. Läkare Indien 63, 83-84.
PubMed Abstrakt / Google Scholar
Tran, M. H., Mkhikian, H., Sy, M., Perez-Alvarez, I. och Demetriou, M. (2018). Långtidsplasmautbyte som underhållsbehandling för Hashimotos encefalopati av cerebellär Typ, en fallrapport. Transfus. Afer. Sci. 57, 418–420. doi: 10.1016 / j. transci.2018.05.027
PubMed Abstrakt / CrossRef fulltext / Google Scholar
Ueno, H., Nishizato, C., Shimazu, T., Watanabe, H., Mizukami, T., Kosuge, H., et al. (2016). Hashimotos encefalopati med svindel och muskelsvaghet hos en manlig pediatrisk patient. Ingen Hattatsu 48, 45-47.
PubMed Abstrakt / Google Scholar
uwatoko, H., Yabe, I., Sato, S., Abe, M., Shirai, S., Takahashi, I., et al. (2018). Hashimotos encefalopati efterliknar en hjärntumör och dess patologiska fynd: en fallrapport. J. Neurol. Sci. 394, 141–143. doi: 10.1016/j.jns.2018.09.008
PubMed Abstrakt / CrossRef Fulltext / Google Scholar
Yoneda, M. (2018). Hashimotos encefalopati och autoantikroppar. Hjärnnerven 70, 305-314. doi: 10.11477/mf.1416201004
PubMed Abstrakt / CrossRef Fulltext / Google Scholar