tumörmarkörer är serumåtgärder som är värdefulla vid diskriminering av en adnexal massa. Men med tanke på den långa listan att välja mellan kan det vara förvirrande att veta exakt vilka som bäst kan tjäna dina diagnostiska behov. Jag är vanligtvis frågad av obstetrikare/gynekologer och primärvårdsläkare för vägledning om detta ämne. I den här kolumnen kommer jag att undersöka några av de beslutsfattande som jag använder när jag bestämmer vilka markörer som kan vara mest användbara för enskilda patienter.
tumörmarkörer beställs vanligtvis för att uppskatta sannolikheten för malignitet och behovet av hänvisning till en onkologisk subspecialist.
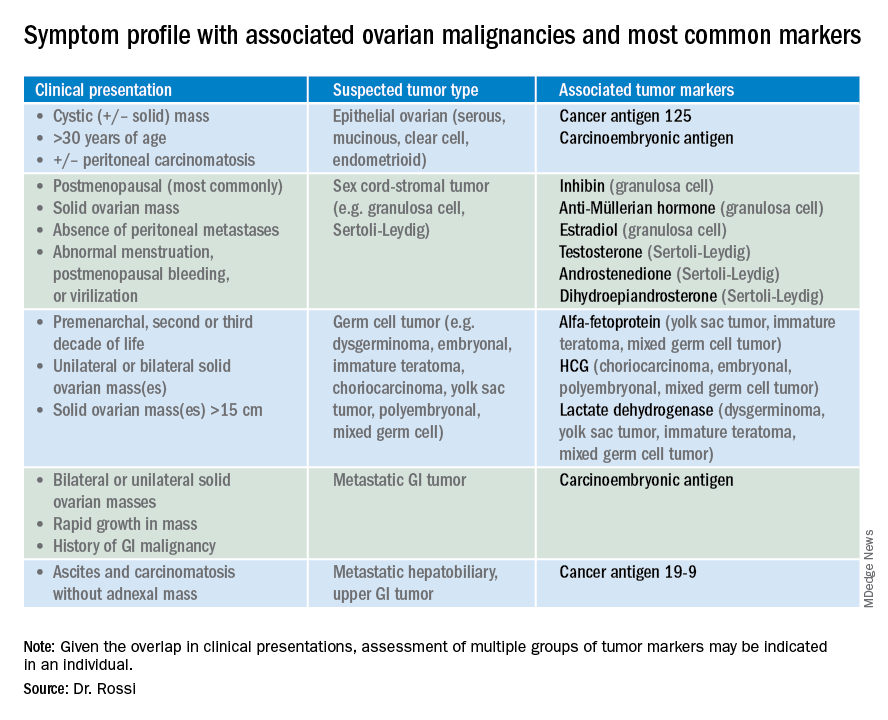
så vilka tumörmarkörer ska du beställa när du har diagnostiserat en adnexal massa? Eftersom tumörmarkörprofiler kan skilja sig dramatiskt baserat på neoplasmens celltyp, kanske den första frågan att ställa är vad som är den mest troliga kategorin av neoplasma baserat på andra kliniska data? Äggstocksneoplasmer passar in i följande undergrupper: epitel (inklusive den vanligaste celltypen, serös äggstockscancer, men också de mindre vanliga mucinösa och låga maligna potentiella tumörerna), könsstromala tumörer, bakteriecelltumörer och metastatiska tumörer. Tabell 1 sammanfattar vilka tumörmarkörer som bör övervägas baserat på den kliniska inställningen.
du bör misstänka en epiteltumör om det finns en adnexal massa med signifikanta cystiska komponenter hos äldre, postmenopausala patienter eller närvaron av peritoneal karcinomatos vid avbildning. Tumörmarkörerna som oftast höjs i denna kliniska miljö är cancerantigen 125 (CA 125), karcinoembryoniskt antigen (CEA) och eventuellt CA 19-9. CA 125-antigenet är ett glykoprotein härrörande från epitelet av peritoneum, pleura, perikardium och M-vävnader. De många ursprungsställena för detta glykoprotein talar om den dåliga specificiteten associerad med dess höjd, eftersom det är välkänt att vara förhöjt i både godartade tillstånd såsom endometrios, fibroider, graviditet, ägglossning, cirros och perikardit såväl som i icke-gynekologiska maligniteter, särskilt de metastatiska till bukhålan. Flera olika analyser är tillgängliga för att mäta CA 125, och var och en är associerad med ett något annat referensområde. Om man mäter seriella värden är det därför bäst att få dessa bedömda av samma laboratorium. På samma sätt, eftersom det kan vara fysiologiskt förhöjt under menstruationscykeln, bör premenopausala kvinnor ha seriella bedömningar vid samma punkt i menstruationscykeln eller helst inom de första 2 veckorna av sin cykel.
känsligheten hos CA 125 vid detektering av äggstockscancer är endast 78%, vilket begränsas av det faktum att inte alla epiteliala äggstockscancercelltyper (inklusive vissa klara celler, karcinosarkom och mucinösa) uttrycker höjningar i denna tumörmarkör, och eftersom CA 125 är förhöjd i mindre än hälften av stadium i äggstockscancer.1 med tanke på bristen på känslighet och specificitet för denna tumörmarkör bör du därför integrera andra kliniska data, såsom bildfynd, patientens ålder och tillhörande godartade medicinska tillstånd, när du utvärderar sannolikheten för cancer. American College of Obstetricians and Gynecologists (ACOG) rekommenderar att i samband med en adnexal massa rekommenderas hänvisning till gynekologisk onkologi när CA 125-värdet är större än 200 U/mL hos premenopausala kvinnor eller större än 35u/mL hos postmenopausala kvinnor.2
CEA är ett protein som kan uttryckas i tjocktarmen men inte i andra normala vävnader efter födseln, och därför är dess höjning vanligtvis associerad med metastatiska GI-tumörer till äggstocken och bukhinnan, eller mucinösa äggstockstumörer, inklusive gränstumörer. Metastatiska gi-tumörer misstänks vanligtvis när det finns bilaterala fasta äggstocksmassor. Högersidiga cystor av äggstockar kan också associeras med appendiceal patologi och kontroll av en CEA-nivå kan övervägas i dessa fall. Jag kommer vanligtvis att dra både CA 125 och CEA tumörmarkörer i inställningen av cystiska +/– fasta äggstocksmassor. Detta möjliggör erkännande av CA 125-negativa/CEA-positiva äggstockscancer, såsom mucinösa tumörer, vilket hjälper till vid senare övervakning eller ökar min misstanke om en ockult GI-tumör (särskilt om det finns en oproportionerligt högre höjd i CEA än CA 125).3 Om tumörmarkörprofiler tyder på en ockult gi-tumör, kommer jag ofta att överväga en preoperativ koloskopi och endoskopisk bedömning av övre GI.
CA 19-9 är en mycket mindre specifik tumörmarkör som kan förhöjas i en mängd solida organtumörer inklusive bukspottkörtel -, hepatobiliär -, mag-och äggstockstumörer. Jag reserverar vanligtvis att lägga till denna markör för atypiska kliniska presentationer av äggstockscancer, såsom karcinomatos i frånvaro av bäckenmassor.

Dr. Emma C. Rossi
Ovarian sex sladd-stromala neoplasmer förekommer oftast som fasta tumörer i äggstocken. Äggstocksstroma inkluderar de intetsägande fibroblasterna och de hormonproducerande könsnordgranulosa -, Sertoli-och Leydig-cellerna. Därför sex sladd-stromala tumörer vanligen är associerade med förhöjningar i serum inhibin, Anti-m Obbllerian hormon, och potentiellt androstenedion och dehydroepiandrosteron.4 dessa tumörer har sällan avancerad sjukdom vid diagnos. Granulosa celltumörer bör misstänkas hos kvinnor med en fast äggstocksmassa och onormal livmoderblödning (inklusive postmenopausal blödning), och lämpliga tumörmarkörer (inhibin och anti-m Occullerian hormon) kan styra denna diagnos preoperativt.4 Androgenutsöndrande stromala tumörer som Sertoli-Leydig-tumörer förekommer ofta med virilisering eller menstruella oegentligheter. Intressant kan dessa patienter ha dramatiska kliniska symtom med motsvarande icke-synliga eller mycket små fasta adnexala lesioner som ses vid avbildning. I fallet med fibromas har dessa fasta tumörer normala hormonella tumörmarkörer men kan förekomma med ascites och pleurala effusioner som en del av Meigs syndrom, vilket kan förvirra kliniken som kan misstänka avancerad epitelcancer, särskilt eftersom detta tillstånd kan vara associerat med förhöjd CA 125.
Könscellstumörer utgör den andra huvudgruppen av primära äggstockstumörer och uttrycker vanligtvis starkt tumörmarkörer. Dessa tumörer är vanligtvis fasta och mycket vaskulariserade vid avbildning, kan vara bilaterala och kan vara mycket stora vid diagnostidpunkten.5 de är oftast ensidiga och uppstår bland yngre kvinnor (inklusive vanligtvis under andra och tredje årtionden av livet). Tabell 1 visar de olika tumörmarkörerna associerade med olika bakteriecelltumörer. Det är min praxis att beställa en panel av alla dessa könscellsmarkörer hos unga kvinnor med fasta adnexala massor i vilka könscellstumörer misstänks, men jag kommer inte rutinmässigt att dra denna expansiva panel för äldre kvinnor med cystiska lesioner.
Tumörmarkörpaneler (som OVA 1, Overa, risk för Malignitetsalgoritm eller ROMA) har blivit populära de senaste åren. Dessa paneler innefattar flera serummarkörer (såsom CA 125, beta-2 mikroglobulin, humant epididymis sekretoriskt protein 4, transferrin etc.) utvärderas i samförstånd med målet att vara en mer nyanserad bedömning av sannolikheten för malignitet.6,7 dessa analyser stratifieras vanligtvis efter ålder eller menopausal status med tanke på de fysiologiska skillnaderna i normala referensområden som uppstår mellan dessa grupper. Medan dessa studier förbättrar känsligheten och specificiteten för att identifiera malignitet, jämfört med singelanalystester, är de inte definitivt diagnostiska för detta ändamål. Därför rekommenderar jag vanligtvis dessa analyser om en hänvisande läkare behöver ytterligare riskstratifiering för att vägleda om man ska hänvisa till en onkolog för operation eller inte.
inte alla tumörmarkörer är av lika värde hos alla patienter med en adnexal massa. Jag rekommenderar noggrant övervägande av andra kliniska faktorer som ålder, menopausal status, ultraljudsfunktioner och tillhörande fynd som GI-symtom eller manifestationer av hormonella förändringar när man överväger vilka markörer som ska bedömas.
Dr. Rossi är biträdande professor i avdelningen för gynekologisk onkologi vid University of North Carolina i Chapel Hill. Hon sa att hon inte hade några relevanta ekonomiska upplysningar. Maila henne på .