Dentinové hypersenzitivity je jedním z nejčastějších stížností pacientů slyšel v zubní praxi.1 Postihuje až 57% pacientů, zdá se, že vrchol ve věku mezi 20 a 40.2 prevalence přecitlivělosti je mírně vyšší u žen,3 špičáky a premoláry obou oblouků nejčastěji podílejí.4 bolest je často chronická a vyznačuje se akutními epizodami.5
Podle Holland et al,6 dentinové hypersenzitivity je definována jako „krátká, ostrá bolest vyplývající z obnaženého dentinu v reakci na podněty, které jsou obvykle tepelně, odpařovací, hmatové, a osmotický nebo chemické látky, které obvykle nelze přičítat jakékoliv jiné formě, zubní vady nebo patologie.“Obvykle je bolest lokalizována a má krátké trvání. To se liší od pulpální bolesti, která je prodloužená, nudná, bolestivá, špatně lokalizovaná a trvá déle než aplikovaný podnět.
úzkost způsobená přecitlivělostí se může pohybovat od malých až po těžké. U pacientů s těžkou přecitlivělostí může být obtížné jíst a pít, zejména při konzumaci horkých nebo studených látek. Bolest, kterou zažívají jedinci s citlivostí, je však vysoce subjektivní a intenzita je epizodické povahy. Bohužel pacienti jsou zřídka schopni izolovat příslušný zub.7 s cílem izolovat příčiny citlivosti, lékaři obvykle spoléhají na odhalování podezření na zub do vzduchu, výbuch nebo horké nebo studené kapaliny, aby vyvolat reakci. V tomto procesu může být užitečné použití gumové přehrady k izolaci zubu.
hydrodynamická teorie
hydrodynamická teorie je nejčastěji dohodnutou příčinou přecitlivělosti dentinu. Kramer8 a Brännström9 potvrdil a rozšířil na teorii, že vytváří vztah mezi aplikovaným tlakem, vzduch výbuchy a chemické podněty k dentinu tekutiny posuny, které se vyskytují v reakci na tyto podněty.7 V původním výzkumu, Brännström zem skrz sklovinu do midcoronal dentinu třenových zubů u dětí, jejichž zuby byly extrahovány pro ortodontické účely. Dětské průřezové dentinové tubuly byly vystaveny slinám po dobu jednoho týdne, což vedlo ke zvýšené citlivosti. Zpočátku tyto zuby pokrývala vrstva nátěru, ale do konce týdne zmizela, čímž se dentin stal stále více hyperconductive.9 propustnost dentinu se mění a může se rychle snížit.10
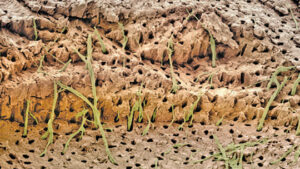
důkazy podporující hydrodynamickou teorii jsou založeny na studiích in vivo u lidí a zvířat. Distribuce nervů v dentinových tubulech se liší, přičemž přibližně 40% se vyskytuje přes rohy buničiny a menší procento se nachází v cervikálním dentinu. Zdá se, že otevřené dentinové tubuly jsou nezbytné pro to, aby se exponovaný dentin stal citlivým (Obrázek 1, strana 18); ve skutečnosti se citlivost pacienta zvýší úměrně počtu přítomných velkých otevřených tubulů. Otevřené tubuly vykazují vysokou hydraulickou vodivost; naopak, průtok tekutiny klesá, pokud jsou tubuly blokovány. To poskytuje prostředky pro různé možnosti léčby. Magloire et al11 stát, že vnější podněty v důsledku dentinové pohyb tekutiny, a to odontoblastů a/nebo nervu komplexní reakce mohou být charakteristické mechanosensory systém — poskytuje novou roli pro odontoblastů jako senzor buňky. Přenos informací mezi odontoblastů a axony mohou být výsledkem mediátorů v mezeře prostor mezi odontoblastů a axony, o čemž svědčí nocioceptive-receptorů, transdukce a trojklanného aferentní vlákna, a vyjádření renomovaných efektory od odontoblastů (Obrázek 2).11
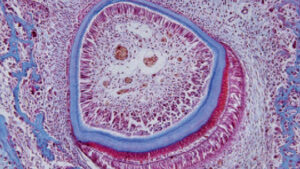
stanovit dentinu (tenkou vrstvu), která tvoří většinu zubu. Smalt (silnější modrá vrstva) je tvořen ameloblasty, vrstvou podlouhlých buněk kolem vnější strany skloviny.
MOŽNÉ PŘÍČINY
Parodontu, gingivální recese, popraskané zuby, eroze, abraze, abfraction a zlomeniny zubu může způsobit přecitlivělost. Všechny tyto podmínky výsledek v obnaženého dentinu, která vytváří prostředí, v němž podněty způsobit dentinových tubulární tekutiny, pohyb, který aktivuje nervových vláken, což způsobuje bolest. Exponovaný dentin může vyplývat z odstranění krční cementu při škálování a kořenové hoblování, dokončování a leštění výplní, nebo extrémní čištění zubů — a to zejména po požití kyselých potravin nebo nápojů. Regurgitace u pacientů s bulimií produkuje kyselinu expozice a následné kartáčování může vést až ke ztrátě zubu.1 Bolest může být lokalizována nebo obecná V přírodě a může ovlivnit různé povrchy zubů, buď společně, nebo jednotlivě.12
jak bylo uvedeno, pacienti s periodontálním onemocněním podléhají přecitlivělosti na dentinu.13 studií ukazuje, že incidence přecitlivělosti se zvyšuje jeden týden po parodontálním chirurgickém zákroku a odezní o osm týdnů.14,15 mladší pacienti vykazují větší citlivost ve srovnání se staršími dospělými, u nichž citlivost trvá déle. Škálování a hoblování kořenů může také způsobit citlivost několik dní po ošetření.
gingivální recese vede k expozici kořenových povrchů a možné citlivosti. Bukální kost poskytuje většinu krevního zásobení bukální gingivy a jakákoli ztráta bukální kosti povede ke snížení gingivy.14 tenká nebo fenestrovaná kost, anatomie zubu, poloha zubu nebo ortodontický pohyb mohou vést k recesi. Nadměrné čištění zubů pomocí zubní pasty může také způsobit recesi.15 známky a příznaky prasklých zubů se mohou lišit v závislosti na závažnosti. Pacienti obvykle zažijí akutní bolest s masticací, ale po odstranění podnětu bolest ustoupí. Pokud se bolest rozšíří na buničinu nebo parodontální VAZ, bude přetrvávat.16
eroze je definována jako ztráta skloviny chemickým rozpuštěním kyselinami, které nejsou bakteriálního původu. Existují tři typy eroze: vnější (např. strava, životní styl nebo životní prostředí), vnitřní (např. žaludeční kyselina) a idiopatická.17 unionizovaná kyselina difunduje do interprismatických oblastí skloviny a rozpouští minerál v podpovrchové oblasti.18 v počátečním stádiu je povrch zubu matný kvůli demineralizaci,ale zub není přecitlivělý, protože dentin s otevřenými tubuly není vystaven. Kompozit lze použít k utěsnění skloviny, aby se obnovil normální obrys a zabránilo se expozici dentinu.19 Obnova zubu zlepší ústní hygienu a sníží možné postižení pulpální tkáně, oděru zubního kartáčku/ zubního prostředku a erozi kyselinou.20
oděr je ztráta struktury zubů mechanickými silami z cizího prvku a může způsobit citlivost.21 opotřebení je kontakt zub-zub, který je výsledkem okluzní funkce nebo parafunkce-jako je bruxismus – a může způsobit ztrátu struktury zubů na okluzních površích a řezných okrajích.22
úloha abfrakce v etiologii přecitlivělosti dentinu je kontroverzní. Abfrakce může nastat, když nepřiměřené cyklické, neaxiální zatížení zubů vede k ohybu hrotu a koncentraci napětí v citlivé krční oblasti zubů. Tyto cervikálních lézí, způsobených okluzní zdůrazňuje, vést k oslabení děložního struktury zubu a může způsobit skloviny, cementu nebo dentinu čip od krční aspekt.23 Lee a Eakle24 poprvé popsali léze, které mohou vyplývat z tahových napětí. Oni zjistí, že abfraction léze je často umístěn na nebo v blízkosti opěry v oblasti s největší koncentrací napětí v tahu; to je obvykle ve tvaru klínu a zobrazí velikost úměrná stupni a výskyt aplikována tahová síla.
jiní však tvrdí, že existují omezené důkazy podporující abfrakci jako primární příčinu toho, co se nyní označuje jako nekariózní cervikální léze. Noncarious procesy, které vedou ke ztrátě tvrdé tkáně v cervikální oblasti, se zdají být multifaktoriální a mohou zahrnovat oděr, kyselé výzvy a případně abfraction.23 Zatímco k dispozici důkazy naznačují, že tyto léze mohou vyvinout ze síly, včetně žvýkací síly, působící samostatně, nebo v kombinaci,23 další studie jsou oprávněné k určení přesné role abfraction v noncarious lézí a všechny související citlivost.
kromě těchto zdrojů způsobuje bělení zubů často přecitlivělost dentinu. Použití peroxidu vodíku nebo peroxidu karbamidu může infiltrovat sklovinu a dentin do buničiny. Glutathionperoxidáza a kataláza v buničině nemají dostatek času na inaktivaci peroxidu vodíku, což může způsobit citlivost. Je třeba také poznamenat, že všechny bělící gely jsou hypertonické a osmoticky čerpat vodu z dužiny přes dentin a sklovinu bělící činidlo. To může potenciálně stimulovat intradentální nervy.25
MOŽNOSTI LÉČBY
Lékaři mohou doporučit řadu procedur pro domácí použití nebo v aplikaci sady office (viz Tabulka 1 pro možnost léčby vývojový diagram).26 mechanismem účinku je typicky nervová desenzibilizace, srážení bílkovin, ucpávání dentinových tubulů, utěsnění dentinu nebo ablace dentinu laserem. Mezi nejčastěji používané terapie patří protizánětlivé látky, proteinové srážecí látky, činidla zabraňující tubulům a tmely tubulů. Nejkonzervativnější přístup by měl být zaveden zpočátku, s agresivnějšími léčbami navrženými, pokud není dosaženo úlevy.27
tabulka 1. Strategie pro Léčbu Kostní Hypersensitivity26 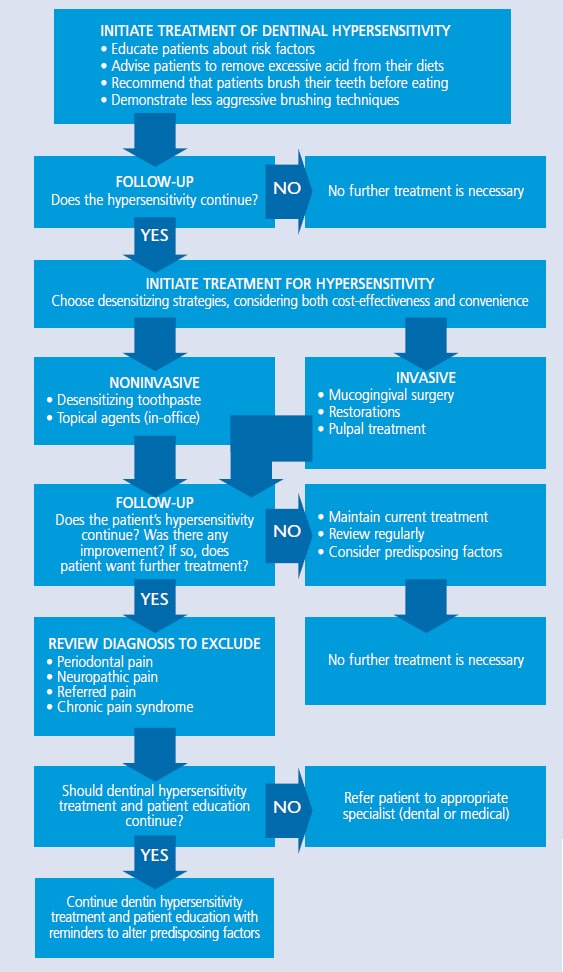 Jako první linie obrany proti citlivosti, lékaři mohou chtít doporučují čištění zubů s draselných solí (např. dusičnan draselný, sodný nebo draselný, citrát sodný), soli stroncia (např. stroncium chlorid nebo octan strontnatý), nebo fluoridů. Ionty draslíku difundují podél dentinových tubulů, které blokují nervové působení a otupují bolest spojenou s přecitlivělostí. Zubní pasty draselné soli jsou účinné, ale mohou vyžadovat dva týdny konzistentního používání, aby pacienti pocítili účinky.28 pro srovnání, způsob účinku nalezený v zubech soli stroncia nebo fluoridu je okluze tubulů. Fluorid v různých formách je účinnou strategií pro domácí úlevu od citlivosti. Fluorid sodný, fluorid kamenitý a monofluorofsofát sodný blokují dentinální tubuly, což snižuje citlivost. Mohou být také užitečné zubní pasty na předpis a aplikace zásobníku.29technologie fosforečnanu vápenatého jsou další možností léčby přecitlivělosti. Amorfní fosforečnan vápenatý zpřístupňuje ionty vápníku a fosfátů ve slinách k urychlení remineralizace a může pomoci minimalizovat citlivost vyvolanou bělením. Je k dispozici v gelových a bělících produktech.29 kromě toho mohou být produkty obsahující kasein fosfopeptid-amorfní fosforečnan vápenatý (CPP-ACP) použity k částečnému uzavření dentinových tubulů. I když předčištění s znecitlivující agent bude někdy v rozporu s regenerační lepení, studie Borges et al30 zjistil, že pasta s CPP-ACP neměl negativně ovlivnit pevnost a v některých případech zlepšila. Fosforečnan vápenatý sodný může také pomoci při infiltraci a remineralizaci tubulů. Oxid křemičitý v materiálu funguje jako nukleační poloha pro srážení vápníku a fosfátu.31 fosforečnan vápenatý (TCP) je nejnovějším přírůstkem do rodiny technologií fosforečnanu vápenatého. Poskytuje pomalé uvolňování vápníku na povrchu zubu, TCP je navržen tak, aby zvýšit remineralizaci účinky fluoridu, což může také snížit citlivost. Je k dispozici v předepsané zubní pastě a fluoridovém laku.32
Jako první linie obrany proti citlivosti, lékaři mohou chtít doporučují čištění zubů s draselných solí (např. dusičnan draselný, sodný nebo draselný, citrát sodný), soli stroncia (např. stroncium chlorid nebo octan strontnatý), nebo fluoridů. Ionty draslíku difundují podél dentinových tubulů, které blokují nervové působení a otupují bolest spojenou s přecitlivělostí. Zubní pasty draselné soli jsou účinné, ale mohou vyžadovat dva týdny konzistentního používání, aby pacienti pocítili účinky.28 pro srovnání, způsob účinku nalezený v zubech soli stroncia nebo fluoridu je okluze tubulů. Fluorid v různých formách je účinnou strategií pro domácí úlevu od citlivosti. Fluorid sodný, fluorid kamenitý a monofluorofsofát sodný blokují dentinální tubuly, což snižuje citlivost. Mohou být také užitečné zubní pasty na předpis a aplikace zásobníku.29technologie fosforečnanu vápenatého jsou další možností léčby přecitlivělosti. Amorfní fosforečnan vápenatý zpřístupňuje ionty vápníku a fosfátů ve slinách k urychlení remineralizace a může pomoci minimalizovat citlivost vyvolanou bělením. Je k dispozici v gelových a bělících produktech.29 kromě toho mohou být produkty obsahující kasein fosfopeptid-amorfní fosforečnan vápenatý (CPP-ACP) použity k částečnému uzavření dentinových tubulů. I když předčištění s znecitlivující agent bude někdy v rozporu s regenerační lepení, studie Borges et al30 zjistil, že pasta s CPP-ACP neměl negativně ovlivnit pevnost a v některých případech zlepšila. Fosforečnan vápenatý sodný může také pomoci při infiltraci a remineralizaci tubulů. Oxid křemičitý v materiálu funguje jako nukleační poloha pro srážení vápníku a fosfátu.31 fosforečnan vápenatý (TCP) je nejnovějším přírůstkem do rodiny technologií fosforečnanu vápenatého. Poskytuje pomalé uvolňování vápníku na povrchu zubu, TCP je navržen tak, aby zvýšit remineralizaci účinky fluoridu, což může také snížit citlivost. Je k dispozici v předepsané zubní pastě a fluoridovém laku.32
in-OFFICE aplikace
jednoduché in-office terapie mohou být užitečné při řešení citlivosti. Lékaři mohou aplikovat desenzibilizující profylaktickou pastu formulovanou s 8% argininem a uhličitanem vápenatým k uzavření tubulů zátkami argininu, vápníku, fosfátu a uhličitanu. Bylo prokázáno, že vydržet normální pulpal tlaku a kyselých výzvy, úspěšně minimalizuje dentinových tubulů průtok kapaliny, a proto, citlivost,33 bez poškození pevnost.34
fluoridový lak umožňuje pomalé a kontinuální uvolňování fluoridu. Laky poskytují prostředek na bázi přírodní pryskyřice pro fluorid. Fluorid vápenatý se nanáší na povrch zubu, což vede k tvorbě fluorapatitu. Přidání oxalátu draselného způsobuje tvorbu kyselinovzdorného oxalátu vápenatého po reakci s vápníkem dentinu.35 lak s prodlouženým kontaktem je fotocurovaný fluoridový lak, který lze použít ke snížení přecitlivělosti dentinu. Skládá se z ionomeru skla modifikovaného pryskyřicí, který obsahuje glycerofosfát s uvolňováním fluoridů. Podporuje také tvorbu pryskyřičných značek, což umožňuje okamžitou a dlouhodobou okluzi tubulů. Další lak kombinuje 5% glutaraldehydu a 35% hydroxyethylmethakrylátu. Působí jako biologický fixační prostředek a vytváří koagulaci plazmatických proteinů v tubulech a blokuje otvory. Schopný snížit citlivost po dobu nejméně tří měsíců,, sup>36 může infiltrovat kyselinou leptaný a vlhký dentin. Tyto laky jsou kompatibilní s lepidly, cementy a regeneračními a jádrovými materiály.37
Chlorhexidin lak tvoří mechanickou bariéru, po sušení, což snižuje citlivost, a zároveň poskytuje antiplaque a antibakteriální účinek.38
bylo také prokázáno, že oxaláty snižují propustnost dentinu a blokují tubuly.39 oxalát reaguje s ionty vápníku v dentinu za vzniku krystalů oxalátu vápenatého v tubulech a na povrchu. Účinek se však časem snižuje, protože krystaly se odstraňují kartáčováním a dietními kyselinami. Leptání zlepšuje infiltraci krystalů oxalátu vápenatého do tubulů.39
Lékaři mohou také použít světlem tuhnoucí desensitizer, který snižuje citlivost prostřednictvím reakce monomeru s vápníkem v zubu a pryskyřice tag tvorbu, což v tubulu okluze. Vytvrzovací světlo následně polymeruje pryskyřičnou vrstvu. Může být použit pro okamžité dentinové utěsnění připravených zubů.
INVAZIVNÍ MOŽNOSTI LÉČBY
Když méně invazivní terapie nejsou účinné, lepení, roubování a ošetření laserem může poskytnout úlevu od dentinové hypersenzitivity. Pojiva mohou být použita k současnému znecitlivění a vazbě.40 v závislosti na použitém produktu je potenciální nevýhodou tohoto přístupu potřeba kyseliny fosforečné před umístěním pojiva, což může vyžadovat použití anestezie.
alternativou je použití samoleptacího lepidla. Další dostupné pojivo blokuje dentinální tubuly a obsahuje triclosan, aby se minimalizovala tvorba plaku.41 alternativním způsobem desenzibilizace je zakrytí exponovaných kořenových povrchů roubováním. To by mělo být zváženo před technikami lepení, nicméně, protože lepené výplně mohou zabránit úspěšnému štěpu.42 použití Nd:YAG lasery zajišťují absorpci tepelné energie na dentinu, což může mít za následek okluzi nebo zúžení dentinových tubulů.39,43
SHRNUTÍ
Dentinové hypersenzitivity je způsobeno tím, obnaženého dentinu, ve kterém podněty vyvolat dentinových tubulů plynulý pohyb, který aktivuje nervových vláken, aby způsobit bolest. Vztah mezi povrchem a intratubulární precipitace a mírou citlivosti není jednoduché. Není to množství sraženiny, ale spíše kvalita, hustota, pórovitost, Hloubka průniku a síla připojení k dentinu, která ovlivňuje výsledky.40 nakonec je účinnost léčby určena tím, jak dlouho trvá snížení nebo eliminace.
rozhodnutí o léčbě by měla být založena na závažnosti a etiologii dentinální přecitlivělosti. Některé in-office ošetření přinést okamžitou úlevu, která může být následován s řadou at-home opravné prostředky. Pro zajištění dlouhodobé úlevy může být zaručena kombinace technik.
KLÍČOVÉ TAKEAWAYS
-
- Hydrodynamické teorie je nejčastěji dohodnuta příčinou dentinové hypersenzitivity.
- otevřené dentinální tubuly vykazují vysokou hydraulickou vodivost, což přispívá k citlivosti; naopak průtok tekutiny klesá, pokud jsou tubuly blokovány. To poskytuje prostředky pro různé přístupy k léčbě.
- prevalence tohoto onemocnění je mírně vyšší u žen,3 špičáky a premoláry obou oblouků nejčastěji podílejí.4
- Typicky, bolest z přecitlivělosti je lokalizován a krátké trvání; tím se liší od pulpal bolest, což je zdlouhavé, nudné, bolesti, špatně lokalizované, a trvá déle, než aplikovaného stimulu.
- použití gumové přehrady může být užitečné při pokusu o izolaci zubu — nebo zubů-s přecitlivělostí.
- lékaři mohou doporučit různé terapie pro domácí použití nebo kancelářské aplikace. Mezi nejčastější léčby patří protizánětlivé látky, proteinové srážecí látky, činidla zabraňující tubulům a tmely tubulů.
- rozhodnutí o léčbě by měla být založena na závažnosti citlivosti a etiologii a může být zaručena kombinace technik, které poskytují účinnou úlevu.
-
-
- Addy M. přecitlivělost Dentinu: Nové pohledy na starý problém. Int Dent J. 2002; 52: 367-375.
- Addy m. etiologie a klinické důsledky přecitlivělosti na dentin. Dent Clin North Am. 1990;34:503–514.
- Flyn J, Galloway R, Orchardson R. výskyt přecitlivělých zubů na Západě Skotska. J Dent. 1985;13:230–236.
- Addy M, Mostafa P, Newcombe RG. Přecitlivělost dentinu: distribuce recese, citlivosti a plaku. J Dent. 1987;15:242–248.
- Dababneh RH, Khouri AT, Addy m. Dentine hypersenzitivita-záhada? Přehled terminologie, mechanismů, etiologie a řízení. Br Dent J. 1999; 187: 606-611.
- Holandsku GR, Narhi MN, Addy M, Gangarosa L, Orchardson R. Pokyny pro navrhování a provádění klinických hodnocení na dentin hypersensitivity. J Clin Periodontol. 1997;24:803–813.
- li y. inovace v boji proti přecitlivělosti na dentin: současný stav techniky. Compend Contin Educat Dent. 2012; 33 (Suppl): 10-16.
- Kramer IRH. Vztah mezi citlivostí dentinu a pohyby v obsahu dentinových tubulů. Br Dent J. 1955; 98: 391-392.
- Brännström m. vyvolání bolesti v lidském dentinu a buničině chemickými podněty. Arch Oral Biol. 1962;7:59–62.
- Pashley DH. Dentin-predentinový komplex a jeho propustnost: fyziologický přehled. J Dent Res. 1985;64(Suppl): 613-620.
- Magloire H, Maurin JC, Couble ML, et al. Aktuální přehled. Bolest zubů a odontoblasty: fakta a hypotézy. J Orofac Bolest. 2010;24:335–349.
- Camilotti V, Zilly J, Nassar CA, Nassar PO. Desenzibilizující léčba přecitlivělosti na dentin: randomizovaná klinická studie s dělenými ústy. Braz Oral Res. 2012; 26: 263-268.
- Chabanski MB, Gillam DG, Bulman JS, Newman HN. Prevalence citlivosti cervikálního dentinu v populaci pacientů odkázaných na specializované periodontologické oddělení. J Clin Periodontol. 1996;23:989–992.
- Uchida A, Wakano Y, Fukuyama O, Miki T, Iwayama Y, Okada H. Kontrolované klinické hodnocení 10% roztoku chloridu strontnatého při léčbě přecitlivělosti na dentin po parodontálním chirurgickém zákroku. J. Parodontol. 1980;51:578–581.
- Absi EG, Addy M, Adams D. dentin hypersenzitivita-účinek čištění zubů a dietních sloučenin na dentin in vitro: studie SEM. Jaromír Jágr. 1992;19:101–110.
- Kahler W. prasklý zubní hlavolam: terminologie, klasifikace, diagnostika a řízení. Jsem Dent. 2008;21:275–282.
- Bartlett DW. Úloha eroze při opotřebení zubů: etiologie, prevence a léčba. Int Dent J. 2005; 55 (Suppl): 277-284.
- Zero DT, Lussi a. eroze-chemické a biologické faktory důležité pro zubního lékaře. Int Dent J. 2005; 55: 285-290.
- Lambrechts P, Van Meerbeek B, Perdigão J, Gladys S, Braem M, Vanherle G. restorativní terapie erozivní léze. Eur Jen Oral Sci. 1996;104:229–240.
- Grippo JO. Noncarious cervikální léze: rozhodnutí ignorovat nebo obnovit. J Esthet Dent. 1992;4:55–64.
- Abrahamsen TC. Opotřebovaný chrup-patognomonické vzory oděru a eroze. Int Dent J. 2005; 55 (Suppl):268–276.
- McIntyre F. obnovení estetiky a předního vedení v opotřebovaných předních zubech. Konzervativní multidisciplinární přístup. J Am Dent Doc. 2000;131:1279–1283.
- Michael JA, Townsend GC, Greenwood LF, Kaidonis JA. Abfraction: oddělení skutečnosti od fikce. Austria J. 2009; 54: 2-8.
- Lee WC, Eakle WS. Možná úloha tahového napětí v etiologii cervikálních erozivních lézí zubů. J Prothet Dent. 1984;52:374–380.
- Swift EJ Jr. citlivost zubů a bělení. Compend Contin Dent Educat Dent.2005; 26 (Suppl): 4-10.
- Kanadský Poradní výbor pro přecitlivělost na Dentin. Doporučení založená na konsensu pro diagnostiku a léčbu přecitlivělosti na dentin. J Může Dent Doc. 2003;69:221–226.
- Al-Saud LM, Al-Nahedh HN. Okluzní účinek laseru Nd:YAG a různých dentinových desenzibilizujících činidel na lidských dentinových tubulech in vitro: vyšetřování skenovací elektronové mikroskopie. Oper Dent. 2012;37:340–355.
- Poulsen S, Errboe M, Hovgaard O, Worthington HW. Zubní pasta dusičnanu draselného pro přecitlivělost dentinu. Cochrane Database Syst Rev. 2001; 2: CD001476.
- Orchardson R, Gillam DG. Řízení přecitlivělosti na dentin. J Dent Doc. 2006;137:990–998.
- Borges BC, Souza-Junior EJ, da Costa Gde F, et al. Účinek předúpravy dentinu pastou kaseinového fosfopeptideamorfního fosforečnanu vápenatého (CPP-ACP) na pevnost vazby dentinu v trojrozměrných dutinách. Acta Odontol Scand. 2013;71:271–277.
- Forsback AP, Areva S, Salonen JI. Mineralizace dentinu indukovaná ošetřením bioaktivním sklem s53p4 in vitro. Acta Odontol Scand. 2004;62:14–20.
- Karlinsey RL, Mackey AC. Příprava v pevném stavu a zubní aplikace organicky modifikovaného fosforečnanu vápenatého. J Mater Sci. 2009;44:346–349.
- Panagakos F, Schiff T, Guignon a. přecitlivělost na Dentin: účinná léčba desenzibilizační pastou v kanceláři obsahující 8% argininu a uhličitanu vápenatého. Jsem Dent. 2009;22(Dod):3A–7A.
- García-Godoy, García-Godoy F. Vliv 8,0% arginin a uhličitanu vápenatého v kanceláři znecitlivující vložit na smyková pevnost kompozitů na lidské zubní sklovinu. Jsem Dent. 2010;23:324–326.
- Camilotti V, Zilly J, Busato Chop M, Nassar CA, Nassar PO. Desenzibilizující léčba přecitlivělosti na dentin: randomizovaná klinická studie s dělenými ústy. Braz Oral Res. 2012; 26: 263-268.
- Sethna GD, Prabhulji MLV, Karthikeyan BV. Srovnání dvou různých forem laků při léčbě přecitlivělosti dentinu: slepá randomizovaná klinická studie. Ústní Zdraví Předchozí Dent. 2011;9:143–150.
- Dijkman GE, Jongebloed WL, de Vries, J., Ogaard B, Arends J. Uzavření dentinových kanálků tím, glutaraldehyd léčby, rastrovací elektronové mikroskopie studie. Scand J Dent Res. 1994; 102: 144-150.
- Sköldové-Larsson K, Sollenius O., Petersson LG, Twetman S. Vliv lokální aplikace román chlorhexidin-thymol lak vzorec na mutans streptokoky a zubního kazu vývoj v okluzálních fisur stálých molárů. J Clin Dent. 2009;20:223–226.
- Lan WH, Lee BS, Liu HC, Lin CP. Morfologická studie ND: použití laseru YAG při léčbě přecitlivělosti dentinu. J.Endode. 2004;30:131–134.
- Ide M, Morel AD, Wilson RF, Ashley FP. Úloha dentinového pojiva při snižování citlivosti cervikálního dentinu. J Clin Periodontol. 1998;25:286–290.
- Yu X, Liang B, Jin X, Fu, B, Hannig M. Srovnávací studie in vivo na znecitlivění účinnost dentinu desensitizers a jednu láhev self-etching adheziv. Oper Dent. 2010;35:279–286.
- Douglas de Oliveira DW, Marques DP, Aguiar-Cantuária IC, Flecha od, Gonçalves PF. Vliv pokrytí chirurgických defektů na přecitlivělost cervikálního dentinu a kvalitu života. J. Parodontol. 2013;84:768–775.
- Orhan K, Aksoy U, Can-Karabulut DC, kalendář a. nízkoúrovňová laserová terapie přecitlivělosti dentinu: krátkodobá klinická studie. Lasery Med Sci. 2011;26:591–598.
-