Epoxidovou kroužek-zahájení reakce – SN1 vs. SN2, regioselectivity, a stereoselectivity
nonenzymatic kroužek-zahájení reakce epoxidy poskytuje pěkný přehled z mnoha konceptů, které jsme již viděli v této kapitole. Reakce otevírající prstenec mohou probíhat buď mechanismem SN2 nebo SN1, v závislosti na povaze epoxidu a reakčních podmínkách. Pokud je epoxid asymetrický, struktura produktu se bude lišit podle toho, který mechanismus dominuje. Když asymetrický epoxidovou prochází solvolysis v základní methanol, ring-otevření dochází k SN2 mechanismus a méně substituovaný uhlík je místo nucleophilic útok, což vede k tomu, co budeme označovat jako produkt B:

Naopak, když solvolysis se vyskytuje v kyselých methanolu, reakce probíhá mechanismem s podstatným SN1 charakter, a více substituovaný uhlík je web útoku. V důsledku toho převažuje produkt A.

to jsou oba dobré příklady regioselektivní reakce. V regioselektivní reakci jsou jako produkty možné dva (nebo více) různých ústavních izomerů, ale jeden je tvořen přednostně (nebo někdy výhradně).
podívejme se nejprve na základní případ SN2. Odcházející skupina je alkoxidový anion, protože není k dispozici žádná kyselina, která by protonovala kyslík před otevřením kruhu. Alkoxid je špatná odcházející skupina, a proto je nepravděpodobné, že by se kruh otevřel bez „tlačení“ z nukleofilu.

samotný nukleofil je silný: deprotonovaný záporně nabitý methoxidový iont. Pokud nukleofilní substituční reakce zahrnuje špatnou odcházející skupinu a silný nukleofil, je velmi pravděpodobné, že bude pokračovat mechanismem SN2.
a co elektrofil? Existují dva elektrofilní uhlík v epoxidových, ale nejlepší cíl pro nukleofil v SN2 reakce je uhlík, který je nejméně omezován. To odpovídá pozorovanému regiochemickému výsledku. Stejně jako u jiných SN2 reakcí probíhá nukleofilní útok ze zadní strany, což vede k inverzi na elektrofilní uhlík.
pravděpodobně nejlepší způsob, jak znázornit kyselinou katalyzovanou epoxidovou kruhovou reakci, je jako hybrid nebo kříž mezi SN2 a SN1 mechanismem. Za prvé, je kyslík protonované, vytváření dobrého opuštění skupiny (krok 1 níže) . Pak uhlík-kyslík dluhopisů začne break (krok 2) a pozitivní náboj, začne se stavět na více substituovaný uhlík (vzpomeňte si na diskusi z oddílu 8.4 B o karbokation stability).

na Rozdíl od v SN1 reakce, nukleofil napadá elektrofilní uhlík (krok 3) než kompletní karbokation intermediate má šanci tvořit.

Útok probíhá přednostně ze zadní strany (jako v SN2 reakce), protože uhlík-kyslík bond je stále do určité míry na místě, a kyslík, který blokuje útok z přední strany. Všimněte si však, jak se regiochemický výsledek liší od reakce katalyzované bází: v kyselé katalýzy proces, nukleofil napadá více substituovaný uhlík, protože je to uhlík, který má větší míře kladný náboj.
Cvičení 8.17:
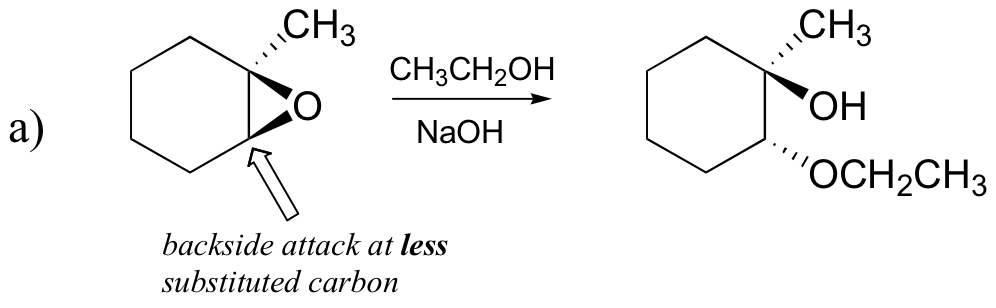
Předpovědět, hlavní produkt(y) kruhu zahájení reakce, která nastane, když epoxidovou na obrázku níže je zacházeno s:
) ethanolu a malého množství hydroxidu sodného
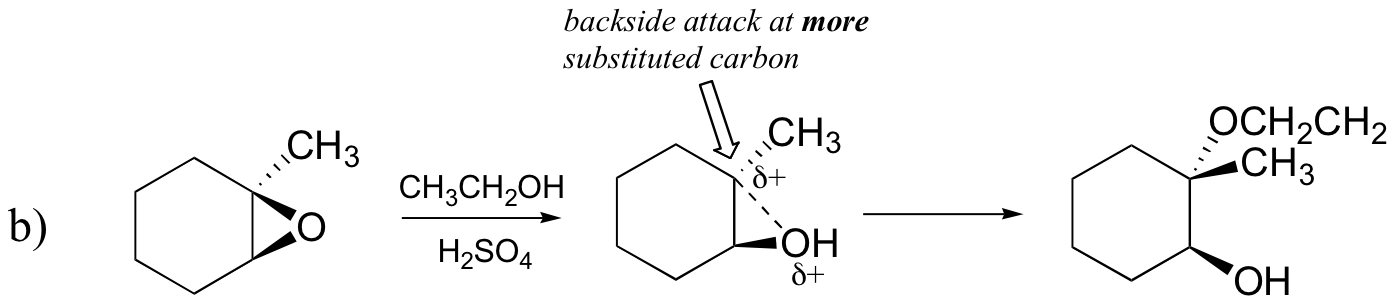
b) ethanolu a malého množství kyseliny sírové

tip: nezapomeňte zvážit jak regiochemii, tak stereochemii!
Khan academy videa

otevření Kruhu za kyselých podmínek: