Vitamin E Léčbu Pacientů s Nealkoholická Steatohepatitis
Jhonathan Ferney Vélez M. (1), Gustavo Amador Crespo H. (1), Juan Carlos Restrepo G. MD. Esp, MSc, PhD. (2)
(1) student medicíny na Lékařské fakultě Universidad de Antioquia v Medellínu v Kolumbii.
(2) docent na Katedře Vnitřního Lékařství a Gastrohepatology Skupiny na Universidad de Antioquia a Hepatolog v Nemocnici Pablo Tobón Uribe v Medellín, Kolumbie. [email protected]
Received: 12-02-14 Přijato: 05-11-14
Abstrakt
Nealkoholické Steatohepatitis (NASH) je charakterizována histologicky tím balonem hepatocytů, lobulárního zánětu a steatózy. Pokud je podezření na tuto diagnózu, je důležité vyloučit jiné příčiny poškození jater, zejména nadměrnou konzumaci alkoholu. K dnešnímu dni je však biopsie jedinou dostupnou metodou k potvrzení diagnózy. Vitamin E by měla být považována za terapii první linie pro léčbu tohoto onemocnění, protože několik klinických studií ukázaly, že dávka 800 UI/den zlepšuje histologie non-dospělých diabetiků, kteří trpí NASH, i když neexistuje žádný významný dopad na fibrózy. Tyto výsledky byly potvrzeny biopsiemi. Navzdory prokázaným přínosům užívání tohoto léku je důležité si uvědomit, že jeho použití nemůže nahradit změny ve stravě a cvičení, ale spíše by mělo být považováno za doplněk těchto opatření.
klíčová slova
nealkoholická steatohepatitida, vitamin E, oxidační stres.
ÚVOD
NASH je charakterizována histologicky tím balonem hepatocytů, lobulárního zánětu a steatózy (1, 2). V současné době může být NASH diagnostikována pouze biopsií jater, což je diagnostický zlatý standard. Poskytuje také informace týkající se přítomnosti a stupně zánětu, nekrózy a fibrózy, které jsou důležité pro stanovení prognózy pacienta (2-5). Rozdíly mezi NASH a alkoholickou steatohepatitidou jsou mikroskopicky malé, což ztěžuje histologické rozlišení mezi nimi. Z tohoto důvodu je důležité získat od pacienta informace o jeho pitných návycích (4).
NASH je součástí mnohem širší entity zvané NAFLD (nealkoholické tukové onemocnění jater), která zahrnuje časná stadia steatózy jater: steatózu bez zánětu a steatózu s mírným zánětem. Nakonec se NAFLD vyvine do charakteristického zánětlivého stavu NASH, který postupuje k fibróze a nakonec cirhóze (1, 2, 5). Dosud není zcela jasné, že jednotlivci postupují od jednoduché steatózy k zánětlivému stavu. Interakce mezi genetickou náchylností, metabolickými poruchami a oxidačním stresem jsou nejdůležitějšími faktory (6, 7).
NAFLD je celosvětově nejrozšířenějším onemocněním jater (2, 4, 6). Prevalence NAFLD se odhaduje na 20% až 30% a prevalence NASH je považována za 2% až 3% v běžné populaci západního světa (8).
vzhledem ke svým antioxidačním vlastnostem byl vitamin E doporučen v současných amerických pokynech pro léčbu NASH. „Vitamin E (α -tokoferol) podáván v denní dávce 800 IU / den zlepšuje jaterní histologie v non-dospělých diabetiků s biopsií prokázáno NASH“ To nezbavuje význam intervence v oblasti životního stylu a dieta jako součást základní léčby pro pacienty s NASH (9, 10). V tomto článku přezkoumáváme patofyziologii NASH s důrazem na roli vitaminu E při léčbě pacientů s tímto onemocněním.
PATOFYZIOLOGIE
Zatímco patogeneze NASH není ještě zcela jasné, nejlepší přijata hypotéza navrhuje, aby datum vysvětlit události, které vedly ke steatóza a následně steatohepatitis je „two-hit“ teorie. Prvním hitem při nástupu této nemoci je přetížení tukem (11, 12). Sedavý životní styl, genetické faktory a zvýšený příjem kalorií činí jedinci náchylnější k rozvoji inzulínové rezistence a hyperinzulinémie, která vede ke zvýšení jaterních lipidů, syntézu a uvolňování volných mastných kyselin z tukové tkáně. Pokud je játra udržována v tomto stavu, stává se neschopná metabolizovat všechny mastné kyseliny, které produkuje a které jsou odstraněny z oběhu. Tento stav nakonec vede k druhému zásahu, kterým je steatóza jater a oxidační stres (4, 5, 13).
oxidační stres je nerovnováha upřednostňující prooxidanty před antioxidanty (3). Během jaterní steatózy vstupují hepatocyty do hypermetabolického stavu, který vede ke zvýšené produkci volných radikálů v buněčných organelách (13). Zvýšení množství reaktivních forem kyslíku (ROS) v hepatocytech vést k peroxidaci lipidů, což je reakce, která poskytuje nepřetržitou dodávku dalších volných radikálů s potenciálně zničující účinky (14, 15).
jedním antioxidantem je vitamin E (tokoferol), který reaguje s peroxidy lipidů za účelem jejich snížení na mastné kyseliny. Tvoří relativně stabilní radikál tokoferoxyl, který přetrvává dostatečně dlouho na to, aby přešel zpět na tokoferol reakcí s vitamínem C na buněčném povrchu (12). Vzhledem k této vlastnosti byl vitamin E považován za léčbu pacientů s NASH (13, 16).
projevy a diagnóza
NAFLD je běžný syndrom, který se pohybuje od jednoduché steatózy po steatohepatitidu (NASH) s následnou fibrózou a cirhózou (5). Ačkoli při diagnóze je většina pacientů asymptomatická, někteří pacienti, zejména děti, si mohou stěžovat na únavu a nepohodlí. Nepohodlí v pravém horním kvadrantu břicha, podezření v důsledku zvýšených hladin aminotransferáz a břišní ultrazvuk s jasným onemocněním jater jsou všechny příznaky tohoto onemocnění. Obezita, diabetes a dyslipidemie by měly být také vzaty v úvahu při hodnocení stavů, které mohou být spojeny s NAFLD a NASH (5, 17).
během diagnostického hodnocení by měly být vyloučeny další běžné příčiny onemocnění jater, ale nakonec je jaterní biopsie jedinou dostupnou metodou k potvrzení diagnózy. Je také důležité pro definování prognózy pacienta (Tabulka 1) (3, 4). Navzdory své velké klinické hodnotě je biopsie drahá a vede k mírnému zvýšení morbidity a ve vzácných případech vede k úmrtnosti. Tento nástroj by měl být zvažována pouze u pacientů, pro které přítomnost nealkoholické steatózy je podezřelé, kteří jsou na vysoké riziko steatohepatitis a pokročilou fibrózou (obezita, diabetes typu II mellitus, dyslipidemie a metabolický syndrom) a v případech nejisté diagnózy (3, 9).

ROLE vitaminu E v léčbě nealkoholické steatohepatitidy
v současné době neexistuje účinná léčba NASH. Nicméně, s ohledem na důležitou úlohu vitamín E jako antioxidant faktor tam bylo několik klinických studií s cílem prokázat jeho přínos v klinické a histopatologické vývoj tohoto onemocnění (Tabulka 2).
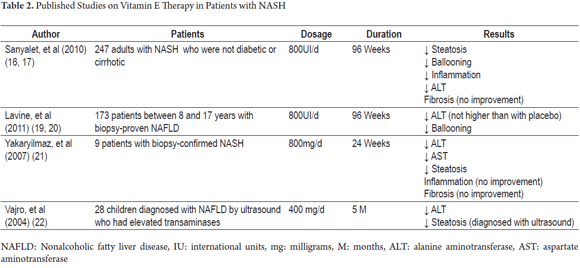
Mezi nimi je PIVENS trial (Pioglitazonem oproti vitaminu E v porovnání s placebem na léčbu non-diabetických pacientů s nealkoholická steatohepatitida). To byla multicentrická, dvojitě zaslepená, placebem kontrolovaná studie, ve které bylo histologické zlepšení byla hodnocena v 247 non-diabetické a non-cirhotických pacientů, kteří měli NASH. Pacienti byli náhodně zařazeni do denní dávky pioglitazonu (80 pacientů), vitaminu E(84 pacientů) nebo placeba (83 pacientů) po dobu devadesáti šesti týdnů (18). Denní dávky byly 30mg pro pioglitazon a 800U pro vitamin E. Tato studie zjistila, že 43% pacientů, kteří dostávali vitamin E (P = 0,001) zlepšení vs. 34% těch, kteří dostávali pioglitazon (P = 0.04) a 19% z těch, kteří dostávali placebo. Rozdíl v míře zlepšení mezi pioglitazonem a placebem nebyl statisticky významný, zatímco rozdíl mezi sazby zlepšení Vitaminu E a placebo. Nicméně obě léky byly spojeny se zlepšením hladin aminotransferázy, snížením steatózy a lobulárního zánětu, ale ani jeden nevedl ke zlepšení fibrózy. Stejná studie ukázala, že po ukončení léčby vitamínem E se hladiny aminotransferázy zvýšily, což naznačuje, že může být nezbytné neurčité podání léčby. Kromě toho nebyly zjištěny žádné významné rozdíly mezi nežádoucími účinky vitaminu E a nežádoucími účinky placeba (19).
přehodnocení PIVENSOVY studie Hoofnagle et al. zaměřuje se na reakce ALT v séru u pacientů, kteří užívali vitamín E nebo placebo a o přidružení tato reakce s počáteční klinické, histologické změny a interakce se změnami v tělesné hmotnosti. Zjistili, že změny ALT byly častější u těch, kteří dostávali vitamín E (48%) než u těch, kteří dostávali placebo (16%; p <0, 001). Ve skupině, která dostávala vitamín E, byly ALT odpovědi spojeny se sníženou aktivitou nealkoholického tukového jaterního onemocnění (NAFLD), ale po ukončení léčby po 96 týdnech nedošlo ke zlepšení fibrózy. ALT zvýšené hladiny vitaminu E skupiny po podání skončila, ale nedošlo k nárůstu ve skupině placeba po podání skončil. Obě léčebné skupiny měly ve 120. týdnu téměř identické hladiny ALT. Tyto výsledky jsou podobné těm, které jsou uvedeny v celé kohortě hlavní publikace PIVENSOVY studie. Navíc, výsledky ukázaly, že ztráta hmotnosti (2 kg nebo více), je také spojován s ALT odpověď, s lepší NAFLD (<0,001) a zlepšení fibrózy (p <0.02), ale vitamin E měl větší účinky na NAFLD nezávislé změny v tělesné hmotnosti. Konečně je třeba poznamenat, že účinky vitaminu E a hubnutí na ALT reakci a histologie jsou nezávislé, což znamená, že i ti pacienti, kteří zhubnout, by měli prospěch z terapie s vitamínem E (20).
další multicentrickou, dvojitě zaslepenou, placebem kontrolovanou studií byla studie s tonikem (léčba nealkoholického tukového jaterního onemocnění u dětí). Zahrnovalo 173 pacientů ve věku od osmi do sedmnácti let. Pacienti byli randomizováni k podávání vitaminu E (58 pacientů), metforminu (57 pacientů) nebo placeba (58 pacientů) po dobu 96 týdnů. Dávky byly 400 IU dvakrát denně pro vitamín E a 500 mg dvakrát denně pro metformin (21). Ani jeden z přípravků nebyl lepší než placebo pro dosažení buď trvalého snížení výchozích hladin ALT alespoň o 50% nebo trvalých hladin ALT 40 U / L nebo méně. Měření byla prováděna každých 12 týdnů od 48. týdne do 96. týdne. Tato studie také zjistila, že rozlišení NASH bylo významně vyšší ve skupině pacientů léčených vitamínem E než ve skupině s placebem. Tento výsledek byl přičítán významnému poklesu hepatocelulárního balonu, který byl zjištěn u pacientů léčených vitamínem E. To je podobné PIVENS výsledky i přesto, že TONIKUM soud nezkoumal snížil hepatocelulární balonem jako primární výsledek, protože histopatologického rozdíly mezi NALFD u dětských pacientů a dospělých. Tonická studie nezjistila žádné zlepšení fibrózy (22).
před těmito dvěma velkými studiemi byly provedeny další menší studie, které měly výsledky s významnými rozdíly v hodnocených primárních výsledcích. Kromě mnohem menších populací měly tyto studie kratší dobu sledování a některé z nich nebyly kontrolovány placebovými skupinami.
a 2007 study by Yakaryilmaz et al. podíval se na účinek vitaminu E na devět pacientů, jejichž diagnózy NASH byly ověřeny biopsií. Studie hodnotila účinek vitaminu E na receptor gama aktivovaný peroxizomovým proliferátorem (PPARG) a na inzulínovou rezistenci. Pacienti dostávali 800 mg vitaminu E denně po dobu 24 týdnů. Před zahájením léčby byla játra pacientů hodnocena biochemicky a histologicky. Tato hodnocení byla opakována po ukončení léčby. Na konci 24 týdnů bylo zjištěno statisticky významné snížení AST, ALT a steatózy, ale nebyly zjištěny žádné histologické změny v úrovni zánětu a fibrózy. Žádný pacient neměl při této dávce vitaminu E (23) nežádoucí účinky.
Vajro, et al. (2004) provedla studii skupiny 28 dětí s dysfunkcí jater související s obezitou. Pacienti byli rozděleni do dvou skupin. Průměrný věk skupiny byl 9.88 (+/- 3.97) let, a druhá skupina byla 10.7 (+/- 3.45). Pacienti byli hodnoceni, aby se zjistilo, zda existují nějaké příznivé účinky léčby vitamínem E na úbytek hmotnosti, hladiny transamináz a steatózu měřené ultrazvukem. Děti účastnící se této studie měli chronické hypertransaminasemia (AST nebo ALT úrovně 1,5 krát vyšší normální hodnoty pro více než 6 měsíců) a známky steatózy v ultrazvuku. Studie měla jeden-slepý design, ve které byli pacienti randomizováni do jedné ze dvou skupin: Skupina 1 (placebo plus strava) a Skupina 2 (vitamin E + strava). Později byla každá skupina rozdělena v závislosti na souladu pacienta s léčbou. Skupina 1 byla rozdělena do podskupiny 1A pro ty, kteří dodržovali dietu, a podskupiny 1B pro ty, kteří nedodrželi dietu. Skupina 2 byla rozdělena do Podskupin 2A pro ty, kteří v souladu s vitamínem E terapii a Podskupina 2B pro ty, kteří neměli splněny s vitamínem E terapii. Podskupina 2A byla dále rozdělena na podskupinu 2A1 pro ty, kteří nedodržovali dietu, a podskupinu 2A2 pro ty, kteří dietu dodržovali. Studie zjistila, že dávka vitaminu E 400 mg/den způsobila významné snížení hodnot ALT u pacientů v podskupině 2A, kteří se přiblížili normalizaci nezávisle na jakýchkoli změnách hmotnosti. Na druhé straně pacienti, kteří dosáhli vysokých hladin vitaminu E v séru a také zhubli, dosáhli normalizace ALT a remise steatózy. Dále, srovnání mezi Podskupina 1A, kdo splněny pouze s dietou a Podskupiny 2A1, kdo splněny pouze s vitaminem E terapie zjistili, že obě skupiny pacientů měly snížení hladin ALT na dva měsíce sledování, ale že to tam bylo větší snížení Podskupina 1A (splněny pouze s dietou) než v Podskupině 2A1 (splněny pouze s vitaminem E) na pět měsíců sledování. Všechny příznaky steatózy zmizely z ultrazvukových obrazů v podskupině 2A2 skupina, která zhubla během léčby 400 mg vitaminu E. Tyto výsledky poukazují na význam podpory zdravé výživy jako jeden z hlavních léčebných intervencí u pacientů s NASH, ale musíme si také uvědomit, že mnozí pacienti nedodržují dietní režimy vedou k selhání zásahu. To zdůrazňuje význam použití antioxidantů, jako je vitamin E, jako dobré alternativní terapie pro tyto pacienty (24).
pilotní studie kugelmas, et al. (2003) hodnotili účinky Krok 1 American Heart Association strava v kombinaci se zvýšenou aerobní cvičení s a bez denní podávání vitaminu E na profily cytokinů (TNF alfa, IL-8, IL -6) a hladiny jaterních enzymů v 16 pacientů mezi 18 a 65 let věku s biopsií prokázanou NASH. To byl single-blind studii, ve které byli pacienti náhodně zařazeni tak, aby dostávali 800 IU vitaminu E denně. Pacienti, kteří nedostávali vitamín E, dostávali placebo. Test byl proveden po dobu 12 týdnů. Hodnoty cytokinů se během studie významně nesnížily při úbytku hmotnosti s podáním vitaminu E nebo bez něj. Změny životního stylu byly spojeny se zlepšením jaterních enzymů a hladinu cholesterolu v plazmě u pacientů s NASH, zatímco dávka vitaminu E použitá v této studii neprokázaly žádné další výhody. Tento výsledek může být způsoben malou velikostí vzorku, krátkou dobou sledování nebo dávkou použitého vitaminu E (25, 26).
recenze publikované v listopadu 2013 o v současné době dostupných možností pro léčbu pacientů s NASH uznávané aktuální doporučení pro použití vitaminu E jako terapii první linie u pacientů s NASH potvrdila biopsií, kteří nejsou cirhózou a kteří nemají diabetes, ale také upozornil na skutečnost, že tato terapie má pouze prokázán významný přínos v méně než polovina pacientů. Z tohoto důvodu přezkum dospěl k závěru, že budoucí léčebné strategie by měly být založeny na patogenních onemocněních, pokud bude někdy vyvinuta účinná léčba pacientů s NASH (27).
Ji H-F et al. provedla metaanalýzu k vyhodnocení účinku vitaminu E na snížení aminotransferáz u pacientů s NAFLD, NASH a chronickou hepatitidou C (CHC). Čtyři studie, které zkoumali, zahrnovaly pacienty s NASH, kteří dostávali doplňky vitaminu E. Studie zahrnovaly studie TONIC a PIVENS. Zjistili, že vitamin E může optimalizovat hladiny AST a ALT u těchto pacientů. Nicméně, je třeba poznamenat, že tato meta-analýza byla omezena neschopnost vyloučit neschopnost vyloučit účinky intervencí zahrnující změny životního stylu, cvičení a použití jiných antioxidantů a neschopnost vyloučit vliv jiných rizikových faktorů pro chronická onemocnění jater, jako jsou alkohol a užívání drog, Přidal se k tomuto, heterogenita studií musí být vzaty v úvahu, jak to omezuje celkovou analýzu, stejně jako s nižší specificita pro hodnoty aminotransferáz než v biopsiích odebraných v době diagnózy a posouzení onemocnění jater (28).
i když mezi hlavní studie s cílem posoudit účinek použití vitaminu E u pacientů s NASH jsme nenašli statisticky významné rozdíly s použitím placeba a další terapeutické možnosti v krátkodobém horizontu, existují obavy o možných nepříznivých účincích dlouhodobé užívání Vitamínu E.
systematický přehled z devíti randomizovaných součástí nové randomizované placebem-kontrolované studie s cílem vyhodnotit účinky vitaminu E po dobu nejméně jednoho roku na celkové incidenci cévní mozkové příhody, stejně jako subtypů cévní mozkové příhody. Bylo zjištěno zvýšené riziko hemoragické mrtvice (RR = 1,22, 95% CI: 1,0 až 1,48, p = 0,045). Vzhledem k výsledkům získaných z jejich hodnocení, vědci doporučují vyhnout se bezohledné použití vitamínu E, protože vážné následky hemoragické mrtvice v nemocnosti a úmrtnosti (29).
randomizované, placebem kontrolované studii, která zahrnovala 35,533 u pacientů po minimálně sedmi let studoval rizika Vitaminu E souvisí s rakovinou prostaty. Srovnávala skupinu s placebem se skupinou, která dostávala vitamín E v denní dávce 400 IU. Došlo k výraznému zvýšení rizika rakoviny prostaty u těch, kteří užívali Vitamín E (H O 1,17; 99% CI, 1.004-1.360; p = 0.008). Absolutní nárůst rizika byl 1,6 na 1000 osob ročně (30).
další metaanalýza zkoumala vztah mezi dávkou a odpovědí suplementace vitamínem E a celkovou mortalitou u dospělých. Ukázalo se, že pacienti, kteří dostávají vysoké dávky vitaminu E (vyšší nebo rovno 400 IU / den), měli zvýšenou úmrtnost ze všech příčin. Tato meta-analýza omezena jeho hledání randomizovaných kontrolovaných studií, jejichž vzorcích pacientů se skládala z dospělých, kteří dostávali léčbu vitaminu E, samotného nebo v kombinaci s dalšími vitamíny nebo minerály, a které vyloučeny těhotné ženy a které měly nejméně 1 rok léčby a sledování. Výsledky poskytnuté touto metaanalýzou by měly být zváženy s opatrností, protože několik studií má malé velikosti vzorků a bylo provedeno u pacientů s několika chronickými onemocněními. To omezuje schopnost studie zobecnit výsledky na zdravou dospělou populaci (31).
ZÁVĚR
i když v současné době neexistuje účinná farmakoterapie u pacientů s NASH, důkazy ukazují PIVENS studie naznačuje, že řádná správa vitamin E zlepšuje jaterní histologie v dospělé non-cirhotických pacientů s NASH, kteří nemají diabetes. Nicméně je zapotřebí více studií, než bude toto doporučení rozšířeno na diabetické pacienty nebo na pacienty, kteří mají cirhózu s NASH. Studie provedené na dětské pacienty s NASH nebyly nalezeny dostatečné důkazy pro podporu užívání vitaminu E. kromě podávání Vitaminu E, bylo prokázáno, že ztráta hmotnosti snižuje steatózu jater a zánětu. U všech pacientů by měla být doporučena ztráta hmotnosti prostřednictvím nízkokalorické stravy v kombinaci se zvýšenou fyzickou aktivitou. Pokud jde o vedlejší účinky, nezjistili jsme statisticky významné rozdíly v krátkodobém užívání vitaminu E s placebem a dalšími možnostmi léčby. Přesto se nerozlišující užívání vitaminu E nedoporučuje po dlouhou dobu, protože existují důkazy naznačující zvýšené riziko rakoviny prostaty, hemoragické mrtvice a smrti ze všech příčin.
1. Abbas AK, Fausto N. Hígado, vesícula Biar y vías biliares. CS: Robbins SL, Mitchell RN, Kumar V, Abbas AK, Fausto N. Patología funcional y estructural. 8va ed. Barcelona: Elsevier; 2012. s. 645-687.
2. Brunt E, Neuschwander-Tetri B, Burt AD. Mastné onemocnění jater: alkoholické a nealkoholické. CS: Burt AD, Ferrell, L Portmann Bc. Macsweenova patologie jater. 6. vydání. Spojené království: Elservier; 2012. s. 293-359.
3. Corrado RL, Torres DM, Harrison SA. Přehled možností léčby nealkoholického tukového onemocnění jater. Med Clin N Am 2014; 98: 55-72.
4. Koek GH, Liedorp PR, Bast a. úloha oxidačního stresu při nealkoholické steatohepatitidě. Clinica Chimica Acta 2011; 412: 1297-1305.
5. Cortez-Pinto H, Ermelinda Camilo M. Nealkoholické mastné onemocnění jater / nealkoholická steatohepatitida (NAFLD / NASH): diagnóza a klinický průběh. Nejlepší Praxe & Výzkum Klinická Gastroenterologie 2004; 18 (6): 1089-104.
6. Mishra A, Younossi ZM. Epidemiologie a přirozená historie nealkoholického tukového onemocnění jater. Journal of Clinical and Experimental Hepatology 2012; 2 (2): 135-44.
7. Rolo AP, Teodoro JS, Palmeira CM. Role oxidačního stresu v patogenezi nealkoholické steatohepatitidy. Zdarma Radic Biol Med 2012; 52 (1): 59-69.
8. Machado MV, Cortez-Pinto h. Neinvazivní diagnostika nealkoholického tukového onemocnění jater. Kritické hodnocení. Journal of Hepatology 2013; 58 (5): 1007-19.
9. Chalasani N, et al. Diagnostiku a Řízení Tukové Non Alkoholické Jaterní Onemocnění: Praxe obecných Zásad podle Americké Asociace pro Studium Jaterních Chorob, American College of Gastroenterologie, a Americké Gastroenterologické Asociace. Hepatologie 2012; 55.
10. Mazzella N, Ricciardi LR, Mazzotti A, Marchesini G. Role léků pro léčbu pacientů s NAFLD. Clin Játra Dis 2014; 18: 73-89.
11. Chunga MY, Yeunga SF, Parka HJ, Volekb JS, Brunoa RS. Dietní α – a γ-tokoferol doplnění zmírňuje lipopolysacharidem indukované oxidačního stresu a zánětlivé reakce v obézní myši model nealkoholické steatohepatitis. Journal of Nutritional Biochemistry 2010; 21: 1200-1206.
12. Den CP, James z. Steatohepatitis: příběh dvou „hitů“? Gastroenterologie 1998; 114: 842-4.
13. Harper HA, Murray RK, Rodwell VW, Bender DA. Bioquímica ilustrada, 28 ed. México: McGraw-Hill Interamericana; 2010. s. 484-485.
14. Neuschwander-Tetri BA. Jaterní lipotoxicita a patogeneze nealkoholické steatohepatitidy: ústřední úloha metabolitů mastných kyselin netriglyceridů. Hepatologie 2010; 52 (2): 774-88.
15. Le T, Loomba R. léčba nealkoholického tukového onemocnění jater a steatohepatitidy. Journal of Clinical and Experimental Hepatology 2012; 2: 156-173.
16. Verdam FJ, Dallinga JW, Driessen, de Jonge C, Moonen, E, van Berkel J, Luijk J, Bouvy ND, Buurman AW, Rensen SS, Greve JW. Nealkoholická steatohepatitida: neinvazivní diagnóza analýzou vydechovaného dechu. Journal of Hepatology 2013; 58: 543-548.
17. Palmentieri B, de Sio I, La Mura V, et al. Úloha jasného vzoru ozvěny jater na ultrazvukovém vyšetření B-mod v diagnostice steatózy jater. Digi, 38: 485-9.
18. Sanyal AJ, et al. Pioglitazon versus vitamin E versus placebo pro léčbu nediabetických pacientů s nealkoholickou steatohepatitidou: PIVENSŮV návrh studie. Contemp Clin Trials 2009; 30 (1): 88-96.
19. Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, Bass NM, et al. Pioglitazon, vitamin E nebo placebo pro nealkoholickou steatohepatitidu. N Engl J Med 2010; 362 (18): 1675-85.
20. Hoofnagle JH, Van Natta ML, Kleiner DE, Clark JM, Kowdley KV, Loomba R, et al. Vitamin E a změny hladin alaninaminotransferázy v séru u pacientů s nealkoholickou steatohepatitidou. Aliment Pharmacol Ther 2013; 38 (2): 134-43.
21. Lavine JE, Schwimmer JB, Molleston JP, Scheimann AO, Murray KF, Abrams SH, et al. Léčba nealkoholického tukového onemocnění jater u dětí: tonický zkušební design. Contemp Clin Zkoušky 2010; 31 (1): 62-70.
22. Lavine JE, Schwimmer JB, Van Natta ML, et al. Účinek vitaminu e nebo metforminu pro léčbu nealkoholické mastných onemocnění jater u dětí a dospívajících: tonikum randomizované kontrolované studii. JAMA 2011; 305 (16): 1659-68.
23. Yakaryilmaz F, Guliter S, Savas B, Erdem O, Ersoy R, Erden E, et al. Účinky vitaminu E na léčbu peroxisome tiazolidindionom-activated receptor-α projevu a inzulínové rezistence u pacientů s non-alkoholická steatohepatitida: výsledky pilotní studie. Stážista Med J 2007; 37 (4): 229-35.
24. Vajro P, Mandato C, Franzese A, Ciccimarra E, Lucariello S, Savoia M, et al. Léčba vitamínem E u pediatrických onemocnění jater souvisejících s obezitou: randomizovaná studie. J Pediatr Gastroenterol Nutr 2004; 38(1): 48-55
25. Papastergiou V, et al. Devět bodovacích modelů pro krátkodobou mortalitu u alkoholické hepatitidy: křížová validace v kohortě prokázané biopsií. Aliment Pharmacol Ther 2014; 39: 721-732.
26. Kugelmas M, Hill DB, Vivian B, Marsano L, McClain CJ. Cytokiny a NASH: pilotní studie účinků modifikace životního stylu a vitaminu E. hepatologie 2003; 38 (2): 413-9.
27. Younossi ZM, Reyes MJ, Mishra MA, Mehta R, Henry L. Systematický přehled s meta-analýzou: nealkoholická steatohepatitida – případ pro osobní léčbu na základě patogenních cíle. Aliment Pharmacol Ther2014; 39: 3-14.
28. Ji HF a kol. Účinek suplementace vitaminem E na hladiny aminotransferázy u pacientů s NAFLD, NASH a CHC: výsledky metaanalýzy. Výživa 2014; 1-6.
29. Markus S, Robert JG, Pamela MR, Christophe T, Tobias k. účinky vitaminu E na podtypy mrtvice: metaanalýza randomizovaných kontrolovaných studií. BMJ 2010; 341.
30. Klein EA, Thompson IM, Tangen CM, et al. Vitamin e a riziko rakoviny prostaty: studie prevence rakoviny selenu a vitaminu e (select). JAMA 2011; 306 (14): 1549-56.
31. Miller ER, 3., Pastor-Barriuso R, Dalal D, Riemersma RA, Appel LJ, Guallar e. metaanalýza: suplementace vysokým dávkováním vitaminu E může zvýšit úmrtnost ze všech příčin. Ann Intern Med 2005; 142 (1): 37-46.