El uso de un tinte azoico como indicador – naranja de metilo
Los compuestos azoicos contienen un sistema altamente deslocalizado de electrones que toma tanto los anillos de benceno como los dos átomos de nitrógeno que unen los anillos. La deslocalización también puede extenderse a cosas unidas a los anillos de benceno. Si la luz blanca cae sobre una de estas moléculas, algunas longitudes de onda son absorbidas por estos electrones deslocalizados. El color que ves es el resultado de las longitudes de onda no absorbidas. Los grupos que contribuyen a la deslocalización (y por lo tanto a la absorción de la luz) se conocen como cromóforo.
Modificar los grupos presentes en la molécula puede tener un efecto en la luz absorbida, y así sucesivamente en el color que se ve. Puede aprovechar esto en los indicadores. La naranja de metilo es un tinte azoico que existe en dos formas dependiendo del pH:
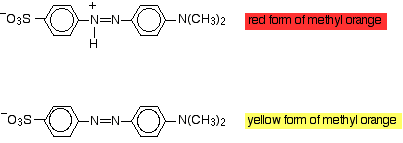
A medida que el ion hidrógeno se pierde o se gana, se produce un cambio en la naturaleza exacta de la deslocalización en la molécula, y eso causa un cambio en la longitud de onda de la luz absorbida. Obviamente, eso significa que ves un color diferente. Cuando se agrega naranja de metilo, se une un ion hidrógeno para dar la forma roja. El naranja de metilo es rojo en soluciones ácidas (de hecho, soluciones de pH inferior a 3,1). Si se agrega un álcali o se eliminan iones de hidrógeno, entonces se genera la forma amarilla. El naranja de metilo es amarillo a un pH superior a 4,4.
En el medio, en algún momento habrá cantidades iguales de las formas roja y amarilla, por lo que el metil naranja se ve naranja.