het gebruik van een azokleurstof als indicator – methyloranje
Azoverbindingen bevatten een sterk gedelokaliseerd systeem van elektronen dat zowel benzeenringen als de twee stikstofatomen opneemt die de ringen overbruggen. De delokalisatie kan zich ook uitstrekken tot dingen die aan de benzeenringen zijn bevestigd. Als wit licht op een van deze moleculen valt, worden sommige golflengten geabsorbeerd door deze gedelokaliseerde elektronen. De kleur die je ziet is het resultaat van de niet-geabsorbeerde golflengten. De groepen die tot de delokalisatie (en zo tot de absorptie van licht) bijdragen zijn genoemd geworden chromophore.
het wijzigen van de groepen die aanwezig zijn in het molecuul kan een effect hebben op het geabsorbeerde licht, en zo op de kleur die je ziet. U kunt hiervan profiteren in indicatoren. Methyloranje is een azokleurstof die in twee vormen bestaat, afhankelijk van de pH:
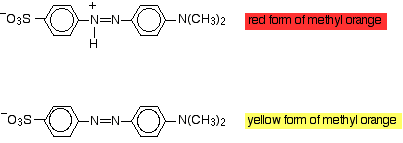
aangezien het waterstofion wordt verloren of bereikt is er een verschuiving in de nauwkeurige aard van de delokalisatie in het molecuul, en dat veroorzaakt een verschuiving in de golflengte van geabsorbeerd licht. Dat betekent natuurlijk dat je een andere kleur ziet. Wanneer methyloranje wordt toegevoegd, hecht een waterstofion zich om de rode vorm te geven. Methyloranje is rood in zure oplossingen (in feite oplossingen met een pH lager dan 3,1). Als een alkali wordt toegevoegd of waterstofionen worden verwijderd, dan is de gele vorm indien gegenereerd. Methyloranje is geel bij pH hoger dan 4,4.
tussen, op een gegeven moment zullen er gelijke hoeveelheden van de rode en gele vormen en dus methyloranje lijkt oranje.