katalysoimattomat reaktiot liuoksessa ovat hitaita, koska varauksen kehitys ja erottaminen tapahtuu siirtymätilassa. Sidosten muodostuessa tai katketessa muodostuu usein varattuja välituotteita, joiden energia on suurempi kuin reaktanttien. Koska välitila on suurempi energialtaan kuin reaktantit, siirtymätila olisi vielä suurempi energialtaan ja muistuttaisi näin ollen tarkemmin varautunutta välituotetta. Kaikki, mikä voi vakauttaa välivaiheen varauksia ja siten kehittyviä varauksia siirtymätiloissa, alentaa siirtymätilan energiaa ja katalysoi reaktiota. Tässä osassa tutkimme mekanismia, joka on katalyysin taustalla pienten molekyylien kemiallisissa reaktioissa. Oletettavasti biologinen makromolekyylikatalyytti (kuten proteiinientsyymit) käyttää samanlaisia mekanismeja katalyyttisissä vaikutuksissaan (joita käsitellään seuraavassa jaksossa).
katalyytit, mukaan lukien entsyymit, voivat käyttää ainakin 5 eri tapaa vakauttaa siirtymätiloja.
VARAUSKEHITYSTÄ TS: ssä voidaan vähentää joko luovuttamalla protoni yleisistä hapoista (kuten etikkahaposta tai protonoidusta indolirenkaasta) karbonyyli-O: n kaltaiselle atomille, joka kehittää osittaisen negatiivisen varauksen TS: ssä nukleofiilin kiinnittyessä siihen. Protonin luovutus vähentää TS: n kehitysnegatiivia. Vaihtoehtoisesti nukleofiili, kuten vesi, joka kehittää osittaisen positiivisen varauksen TS: ssä, kun se alkaa muodostaa sidoksen elektrofiiliseen C: hen karbonyylissä, voidaan stabiloida yleisen emäksen (kuten asetaatin tai deprotonoidun indolirenkaan) läsnäololla. Protonin abstraktio vähentää kehittyvää positiivista varausta
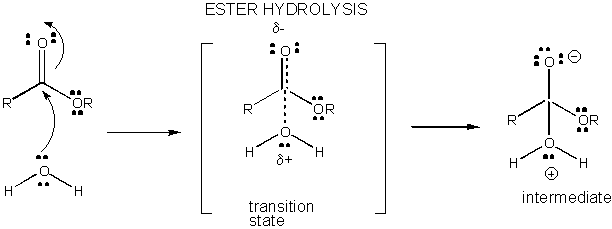
Kuva: varauksen kehitys SIIRTYMÄTILASSA Esterin hydrolyysissä
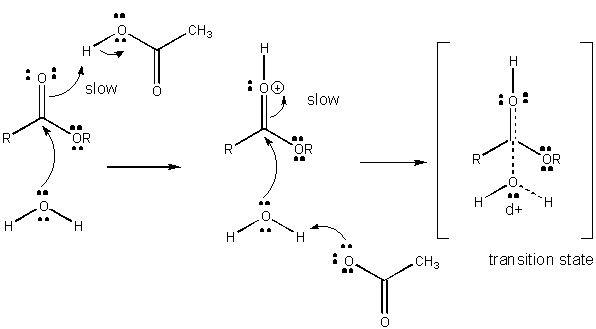
Kuva: yleisen HAPPOKATALYYSIN mekanismi
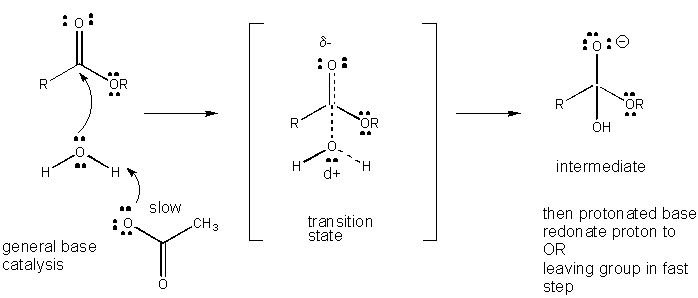
Kuva: yleisen emäksen katalyysin mekanismi
avustajat ja attribuutit
- Prof. Henry Jakubowski (College of St. Benedict/St. John ’ s University)