huonompi petrosal sinus-näytteenotto (IPSS) on invasiivinen toimenpide, jossa adrenokortikotrooppisen hormonin (ACTH) tasot otetaan aivolisäkettä tyhjentävistä laskimoista; näitä tasoja verrataan ääreisveren ACTH-tasoihin sen määrittämiseksi, onko aivolisäkkeen kasvain (toisin kuin kohdunulkoinen ACTH-lähde) vastuussa ACTH-riippuvaisesta Cushingin oireyhtymästä. IPSS: n avulla voidaan myös määrittää, kummalla puolella aivolisäkettä kasvain sijaitsee.
Cushingin tauti johtuu aivolisäkkeen kasvaimen aiheuttamasta liiallisesta kortisolin tuotannosta, joka johtuu kohonneista ACTH-tasoista. Sen sijaan Cushingin oireyhtymä sisältää kaikki hyperkortisolismin olosuhteet, jotka johtuvat joko ACTH-riippuvaisista syistä (esim.Cushingin tauti tai kohdunulkoinen ACTH-eritys ei-pituiteettisen kasvaimen avulla) tai ACTH-riippumattomista syistä (esim. kortisolin liiallinen autonominen eritys hyperfunktionoivasta lisämunuaiskuoren kasvaimesta).
muita ja harvinaisempia tiloja, jotka voivat johtaa Cushingin oireyhtymään, ovat kohdunulkoinen kortikotrofiinia vapauttavan hormonin (CRH) eritys, primaarinen molemminpuolinen pigmentoitunut nodulaarinen lisämunuaisen hyperplasia, makronodulaarinen lisämunuaisen hyperplasia, mahalaukun estävien peptidien kohdunulkoinen vaikutus ja muut oireyhtymät, kuten McCune-Albrightin oireyhtymä ja Carneyn oireyhtymä. Pseudo-Cushing-tiloja, joilla on samanlaisia kliinisiä esityksiä, voidaan löytää masennuksesta ja alkoholiriippuvuudesta. Cushingoid-piirteitä voi olla myös lihavuudessa.
ACTH-riippuvaisen ja ACTH-riippumattomasta Cushingin taudista erottaminen on usein suoraviivaista, mutta Cushingin tautia voi olla vaikea erottaa ektooppisen ACTH: n erityksen aiheuttamasta hyperkortisolismista (ts.epityitaarisesta lähteestä) johtuen ACTH: ta erittävien kasvainten aiheuttamasta syklisestä ja ajoittaisesta erityksestä sekä eri biokemiallisten testien vaihtelevista herkkyyksistä ja erityispiirteistä. Mukaan Prabhu et al (2002), arvo poikkileikkauksen kuvantaminen ACTH-riippuvainen Cushing oireyhtymä on myös rajoitettu, koska pieni toimimaton aivolisäkkeen satunnaisoomia esiintyy jopa 10% MRI suoritetaan terveillä nuorilla.
aivolisäkkeen mikroadenoomien kuvantamisen heikko herkkyys on toinen ongelma. ACTH: ta erittäviä aivolisäkkeen adenoomia on vaikea tunnistaa normaalilla 1, 5 T-tai 3T-magneettikuvauksella sekä dynaamisella varjoainekuvauksella. Useimmissa tapauksissa rutiininomainen thin slice-varjoainetehostettu T1-painotettu MRI pystyy tarjoamaan anatomisia yksityiskohtia ja auttamaan IPS-salaojituskuvion tunnistamisessa. Joissakin tapauksissa, kun salaojakuviota ei voida tunnistaa, edes spatiaalinen resoluutio ei auta kuvaamaan monimutkaista anatomiaa. Tällaisessa tilanteessa IPSS yksin auttaa erottamaan Cushingin taudin Cushingin oireyhtymästä, joka johtuu kohdunulkoisista ACTH: ta erittävistä kasvaimista, ja on siksi edelleen kultakanta ACTH: ta erittävien aivolisäkkeen adenoomien diagnosoinnissa. On hyvin osoitettu, että IPSS voi diagnosoida tarkasti Cushingin taudin, ja on myös tunnettua, että MRI tarjoaa paremman tarkkuuden adenooman paikan paikallistamisessa. Kakade ym. ovat ehdottaneet, että jos magneettikuvauksessa havaitaan epäselviä aivolisäkkeen löydöksiä, aiempi IPSS voi välttää tarpeettomat transfenoidiset leikkaukset. Erään tutkimuksen mukaan 7T MRI voi auttaa havaitsemaan normaalin 1,5 T: n ja 3T MK: n negatiivisen Cushingin taudin ja saattaa ehkäistä IPSS: ää tulevaisuudessa.
aiempi petrosal sinus-näytteenotto
IPSS otettiin käyttöön vuonna 1977 Corrigan et al: ssa, joka raportoi yksipuolisen selektiivisen katetroinnin ja laskimonäytteen käyttämisestä ACTH: n erityksen paikallistamiseen potilaalla, jolla oli hämmentävä kliininen ja laboratoriokuva, joka oli yhteensopiva joko kohdunulkoisen ACTH: n erityksen tai aivolisäkkeestä riippuvan Cushingin oireyhtymän kanssa. Myöhemmin todettiin, että aivolisäkkeen laskimoverenvuodon ACTH-tasot voivat olla epäsymmetrisiä joko kortikotrophin adenooman sijainnin tai laskimoiden anatomian epäsymmetristen vaihtelujen vuoksi.
aivolisäkkeen laskimovuoto on yleensä ipsilateraalinen, joten kontralateraalisen puolen laskimovuoto adenomaan nähden ei useinkaan ole suuri ACTH-pitoisuus. Doppman et al (1984) ehdotti samanaikaista näytteenottoa molemmista huonommista petrosal-sivuonteloista (IPSs), jotta vältettäisiin vääriä negatiivisia tuloksia aivolisäkkeen kortikotroph-adenooman läsnä ollessa. Tämä menettely oli nimeltään bilateral inferior petrosal sinus näytteenotto (BIPSS).
monet kortikotroph adenoomat ovat alttiita stimulaatiolle eksogeenisesti annetulla CRH: lla, kuten Oldfield et al kuvasi ensimmäisen kerran vuonna 1991 bipss: n herkkyyden lisäämiseksi. Raportoiduissa tutkimuksissa on käytetty kahta eri CRH-muotoa: lampaan CRH (oCRH) ja ihmisen CRH (hCRH). Nieman et al (1989) ovat raportoineet, että perifeerinen ACTH ja kortisoli vasteet oCRH olivat merkittävästi korkeammat kuin ihmisen CRH.
Future and controversies
jotkut keskukset ovat raportoineet parantuneesta tarkkuudesta ja tähtienvälisestä paikantamisesta kahdenvälisellä ontelonäytteellä, mutta kallon hermovaurion riski on suurentunut, joten tämä tekniikka ei ole vielä saavuttanut suosiota.
sisäistä kaulalaskimonäytettä (IJVS) on myös kokeiltu teknisesti helpommaksi vaihtoehdoksi BIPSS: lle. Radvany ym. verrattiin IJVS: ää IPSS: ään 30: llä peräkkäisellä potilaalla, joilla oli MRI-negatiivinen ACTH-riippuvainen Cushingin oireyhtymä. Heidän tuloksensa osoittavat, että IJVS ei ole yhtä hyödyllinen aivolisäkkeen diagnosoinnissa kuin IPSS liiallisen ACTH: n lähteenä. Vaikka IJVS on spesifisyys samanlainen kuin BIPSS, se on pienempi herkkyys (83% vs. 94%), mukaan Ilias et al.
IPSS: stä otettujen näytteiden avulla Oklu et al ovat tunnistaneet 3 pientä yhdistepotentiaalista Cushingin taudin biomarkkeria (pyridoksaatti, deoksikolihappo ja trimetyyliadipaatti). Nämä voivat valaista kasvainbiologiaa ja ehdottaa tulevaisuudessa mahdollisia diagnostisia molekyylikuvauskokeita ja terapeuttisia tavoitteita potilailla, joilla on toistuva sairaus leikkauksen jälkeen.
relevantti anatomia
Miller ja Doppman (1991) ovat toimittaneet yksityiskohtaisen kuvauksen IPS: n anatomiasta (KS.kuva alla).
 Inferior Petrosal Sinus Anatomy
Inferior Petrosal Sinus Anatomy useimmilla yksilöillä IPS kapenee yhdeksi suoneksi, jolloin ipsilateraalinen sisäinen jugulaarilaskimo (IJV) tyhjenee. Noin 25%: lla yksilöistä IPS-salaojitus muodostaa pleksin kanavia, jotka tyhjenevät IJV: hen. 0,6% -7%: lla yksilöistä IJV: n ja IPS: n välillä ei ole yhteyttä, mikä tekee normaalinäytteenoton mahdottomaksi.
noin 60%: lla yksilöistä aivolisäkkeen laskimovuoto on symmetrinen siten, että suurin osa aivolisäkkeen molemmilta puolilta valuvasta laskimovirrasta valuu ipsilateraaliseen IPS: ään. Tämän seurauksena, useimmat ihmiset, BIPSS voi olla tehokas työkalu lateralisoida kortikotroph adenoomat ja välttää vääriä negatiivisia tuloksia.
Doppman et al (1999) antoi arvoksi 0.8% väärien negatiivisten tulosten esiintyvyys HYPOPLASTISEEN tai anomaaliseen IPS: ään. Shiu et al (1968) kuvasi ensimmäisen kerran luokittelujärjestelmän IPS-anatomisille muunnoksille. Bonelli et al (2000) ovat kuvanneet Shiu et al: n luokittelujärjestelmän muutosta seuraavasti:
-
tyyppi I (KS. kuva alla): IPS-liitos IJV: n kanssa; anteriorinen kondylaarilaskimo puuttuu tai yhtyy IPS: ään määritellystä alkulähteestä; suonen lyhyttä segmenttiä tämän anastomoosin pisteestä IJV: hen kutsutaan huonommaksi kondylaariseksi yhtymäkohdaksi
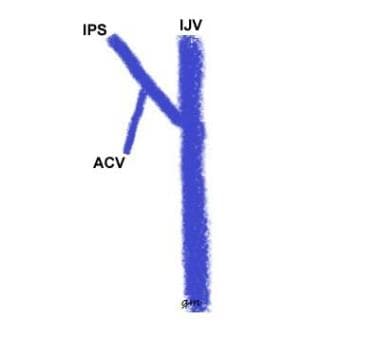 IPS-muunnostyyppi 1
IPS-muunnostyyppi 1 -
tyyppi II (KS. kuva alla): IPS: n ja anteriorisen kondylaarilaskimon yhteinen alkuperä IJV: n kanssa
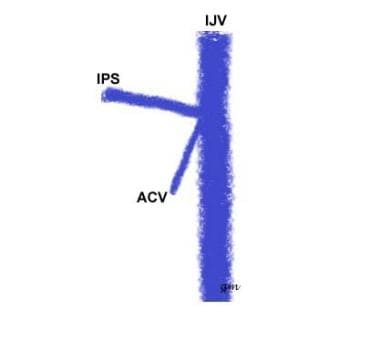 IPS variant type 2
IPS variant type 2 -
tyyppi III (KS. kuva alla): IP-osoite, joka koostuu useista pienistä kanavista, jotka viestivät IJV: n kanssa
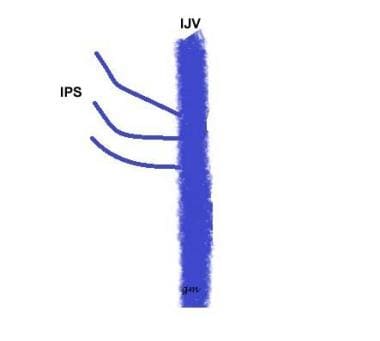 IPS-variantityyppi 3
IPS-variantityyppi 3 -
Tyyppi IV (KS. kuva alla): IPS, joka kommunikoi anteriorisen kondylaarilaskimon kanssa eikä IJV: n
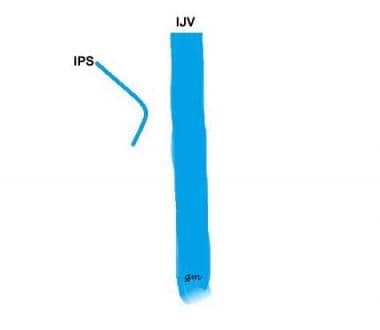 IPS-variantityyppi 4
IPS-variantityyppi 4
 IPS-muunnostyyppi 1
IPS-muunnostyyppi 1  IPS variant type 2
IPS variant type 2  IPS-variantityyppi 3
IPS-variantityyppi 3  IPS-variantityyppi 4
IPS-variantityyppi 4