L’utilisation d’un colorant azoïque comme indicateur – orange de méthyle
Les composés azoïques contiennent un système d’électrons fortement délocalisé qui absorbe à la fois les cycles benzéniques et les deux atomes d’azote qui les pontent. La délocalisation peut également s’étendre aux objets attachés aux cycles benzéniques. Si la lumière blanche tombe sur l’une de ces molécules, certaines longueurs d’onde sont absorbées par ces électrons délocalisés. La couleur que vous voyez est le résultat des longueurs d’onde non absorbées. Les groupes qui contribuent à la délocalisation (et donc à l’absorption de la lumière) sont appelés chromophores.
La modification des groupes présents dans la molécule peut avoir un effet sur la lumière absorbée, et ainsi de suite sur la couleur que vous voyez. Vous pouvez en profiter dans les indicateurs. L’orange de méthyle est un colorant azoïque qui existe sous deux formes en fonction du pH:
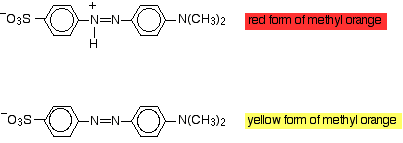
Lorsque l’ion hydrogène est perdu ou gagné, il y a un changement dans la nature exacte de la délocalisation dans la molécule, ce qui provoque un changement dans la longueur d’onde de la lumière absorbée. Évidemment, cela signifie que vous voyez une couleur différente. Lorsque de l’orange méthylique est ajouté, un ion hydrogène se fixe pour donner la forme rouge. L’orange méthylique est rouge dans les solutions acides (en fait des solutions de pH inférieur à 3,1). Si un alcali est ajouté ou si des ions hydrogène sont éliminés, la forme jaune s’il est généré. L’orange méthylique est jaune à un pH supérieur à 4,4.
Entre les deux, à un moment donné, il y aura des quantités égales de formes rouge et jaune et donc l’orange méthylique semble orange.