I marcatori tumorali sono misure sieriche che sono preziose nella discriminazione di una massa annessiale. Tuttavia, data la lunga lista da cui scegliere, può essere fonte di confusione per sapere esattamente quale potrebbe servire meglio le vostre esigenze diagnostiche. Mi viene comunemente chiesto da ostetrici / ginecologi e medici di assistenza primaria per una guida su questo argomento. In questa colonna esplorerò alcuni dei processi decisionali che uso per determinare quali marcatori potrebbero essere più utili per i singoli pazienti.
I marcatori tumorali in genere sono ordinati per stimare la probabilità di malignità e la necessità di un rinvio a un sottospecialista oncologico.
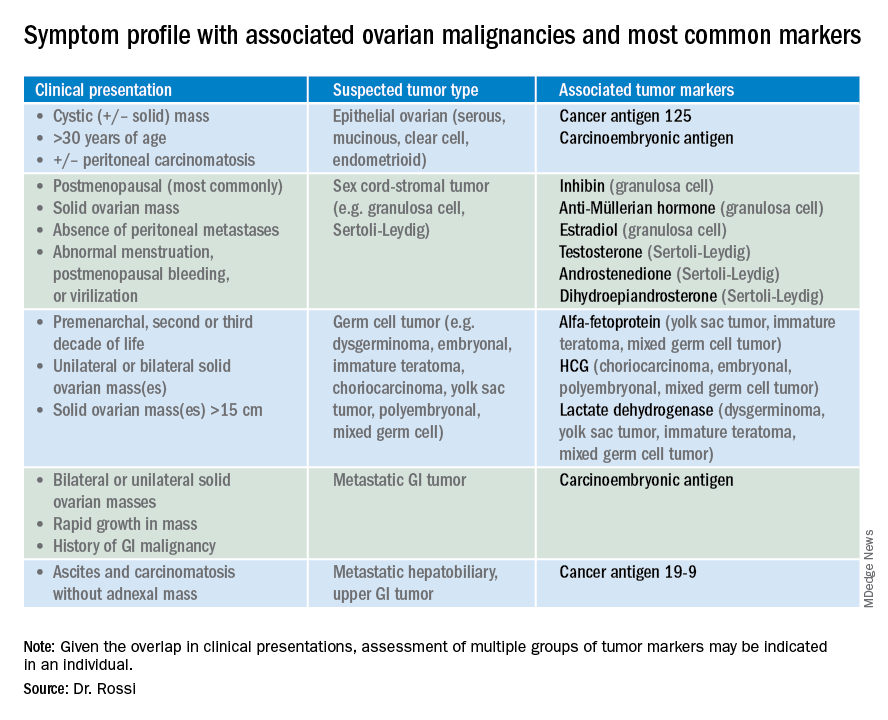
Quindi quali marcatori tumorali dovresti ordinare quando hai diagnosticato una massa annessiale? Poiché i profili dei marcatori tumorali possono differire notevolmente in base al tipo di cellula della neoplasia, forse la prima domanda da porsi è qual è la categoria più probabile di neoplasia basata su altri dati clinici? Le neoplasie ovariche si inseriscono nei seguenti sottogruppi: epiteliale (incluso il tipo di cellula più comune, il cancro ovarico sieroso, ma anche i tumori potenziali mucinosi e maligne meno comuni), tumori del cordone-stromale del sesso, tumori a cellule germinali e tumori metastatici. La tabella 1 riassume quali marcatori tumorali devono essere considerati in base all’impostazione clinica.
Si dovrebbe sospettare un tumore epiteliale se c’è una massa annessiale con componenti cistiche significative in pazienti anziani, in postmenopausa, o la presenza di carcinomatosi peritoneale sull’imaging. I marcatori tumorali più comunemente elevati in questo ambiente clinico sono l’antigene del cancro 125 (CA 125), l’antigene carcinoembrionico (CEA) e possibilmente CA 19-9. L’antigene CA 125 è una glicoproteina derivata dall’epitelio del peritoneo, della pleura, del pericardio e dei tessuti Mülleriani. I molteplici siti di origine di questa glicoproteina parla alla scarsa specificità associata alla sua elevazione, come è ben noto per essere elevata in entrambe le condizioni benigne come endometriosi, fibromi, gravidanza, ovulazione, cirrosi e pericardite, nonché in neoplasie non ginecologiche, in particolare quelle metastatiche alla cavità peritoneale. Sono disponibili più saggi diversi per misurare CA 125 e ciascuno è associato a un intervallo di riferimento leggermente diverso. Pertanto, se si misurano i valori seriali, è meglio farli valutare dallo stesso laboratorio. Allo stesso modo, poiché può essere fisiologicamente elevata durante il ciclo mestruale, le donne in premenopausa dovrebbero avere valutazioni seriali nello stesso punto del loro ciclo mestruale o idealmente entro le prime 2 settimane del loro ciclo.
La sensibilità di CA 125 nel rilevare il cancro ovarico è solo del 78%, che è limitata dal fatto che non tutti i tipi di cellule epiteliali di cancro ovarico (tra cui alcune cellule chiare, carcinosarcoma e mucinoso) esprimono elevazioni in questo marcatore tumorale, e perché CA 125 è elevata in meno della metà dei tumori ovarici di stadio I.1 Pertanto, data la mancanza di sensibilità e specificità per questo marcatore tumorale, è necessario integrare altri dati clinici, come i risultati dell’imaging, l’età del paziente e le condizioni mediche benigne associate, quando si valuta la probabilità di cancro. L’American College of Obstetricians and Gynecologists (ACOG) raccomanda che nell’ambito di una massa annessiale, si raccomanda il rinvio all’oncologia ginecologica quando il valore di CA 125 è superiore a 200 U/mL nelle donne in premenopausa o superiore a 35U/mL nelle donne in postmenopausa.2
CEA è una proteina che può essere espressa nel colon ma non in altri tessuti normali dopo la nascita, e quindi la sua elevazione è comunemente associata a tumori GI metastatici all’ovaio e al peritoneo, o tumori ovarici mucinosi, compresi i tumori borderline. I tumori metastatici di GI sono sospettati tipicamente quando ci sono masse solide ovariche bilaterali. Le cisti ovariche del lato destro possono anche essere associate a patologia appendicea e il controllo di un livello di CEA può essere considerato in questi casi. Disegnerò comunemente sia i marcatori tumorali CA 125 che CEA nell’impostazione di masse ovariche solide + / – cistiche. Ciò consente il riconoscimento di tumori ovarici CA 125-negativi/CEA-positivi, come i tumori mucinosi, che aiutano nella sorveglianza successiva o aumentano il mio sospetto per un tumore occulto GI (in particolare se c’è un’elevazione sproporzionatamente maggiore in CEA rispetto a CA 125).3 Se i profili dei marcatori tumorali sono indicativi di un tumore occulto del GI, spesso prenderò in considerazione una colonscopia preoperatoria e una valutazione endoscopica del GI superiore.
CA 19-9 è un marcatore tumorale molto meno specifico che può essere elevato in una varietà di tumori di organi solidi tra cui tumori pancreatici, epatobiliari, gastrici e ovarici. In genere mi riservo di aggiungere questo marker per le presentazioni cliniche atipiche di cancro ovarico, come la carcinomatosi in assenza di masse pelviche.

Dott. ssa Emma C. Rossi
Neoplasie del cavo-stromale del sesso ovarico più comunemente presenti come tumori solidi nell’ovaio. Lo stroma ovarico comprende i fibroblasti blandi e le cellule di granulosa, Sertoli e Leydig che producono ormoni. Pertanto i tumori del cavo-stromale del sesso sono comunemente associati ad aumenti dell’inibina sierica, dell’ormone anti-mülleriano e potenzialmente dell’androstenedione e del deidroepiandrosterone.4 Questi tumori raramente hanno avanzato la malattia alla diagnosi. I tumori a cellule granulose dovrebbero essere sospettati nelle donne con una massa ovarica solida e sanguinamento uterino anormale (incluso sanguinamento postmenopausale) e gli appropriati marcatori tumorali (inibina e ormone anti-mülleriano) possono guidare questa diagnosi preoperatoria.4 Androgeni-secernenti tumori stromali come tumori Sertoli-Leydig spesso presenti con virilizzazione o irregolarità mestruali. È interessante notare che questi pazienti possono avere sintomi clinici drammatici con corrispondenti lesioni annessiali solide non visibili o molto piccole osservate nell’imaging. Nel caso dei fibromi, questi tumori solidi hanno marcatori tumorali ormonali normali, ma possono presentare con ascite e versamenti pleurici come parte della sindrome di Meigs, che può confondere il clinico che può sospettare il cancro epiteliale in stadio avanzato soprattutto perché questa condizione può essere associata a CA 125 elevata.
I tumori delle cellule germinali costituiscono l’altro gruppo principale di tumori ovarici primari e tipicamente esprimono fortemente i marcatori tumorali. Questi tumori in genere sono solidi e altamente vascolarizzati sull’imaging, possono essere bilaterali e possono essere molto grandi al momento della diagnosi.5 Sono più comunemente unilaterali e si presentano tra le donne più giovani (anche di solito nella seconda e terza decade di vita). La tabella 1 mostra i diversi marcatori tumorali associati a diversi tumori a cellule germinali. È mia pratica ordinare un pannello di tutti questi marcatori di cellule germinali in giovani donne con masse annessiali solide in cui si sospettano tumori a cellule germinali, ma non disegnerò abitualmente questo pannello espansivo per le donne anziane con lesioni cistiche.
I pannelli marcatori tumorali (come OVA 1, Overa, Risk of Malignancy Algorithm o ROMA) sono diventati popolari negli ultimi anni. Questi pannelli includono più marcatori sierici (come CA 125, microglobulina beta-2, proteina secretoria dell’epididimo umano 4, transferrina, ecc.) valutato in concerto con l’obiettivo di una valutazione più sfumata della probabilità di malignità.6,7 Questi saggi sono tipicamente stratificati per età o stato menopausale date le differenze fisiologiche nei normali intervalli di riferimento che si verificano tra questi gruppi. Mentre questi studi migliorano la sensibilità e la specificità per identificare la malignità, rispetto ai test di analisi singola, non sono definitivamente diagnostici per questo scopo. Pertanto, in genere raccomando questi saggi se un medico di riferimento ha bisogno di ulteriore stratificazione del rischio per guidare se fare riferimento o meno a un oncologo per un intervento chirurgico.
Non tutti i marcatori tumorali sono di uguale valore in tutti i pazienti con una massa annessiale. Raccomando un’attenta considerazione di altri fattori clinici come l’età, lo stato della menopausa, le caratteristiche ultrasonografiche e i risultati associati come i sintomi GI o le manifestazioni di alterazioni ormonali quando si considerano quali marcatori valutare.
Dott. Rossi è assistente professore nella divisione di oncologia ginecologica presso l’Università della Carolina del Nord a Chapel Hill. Ha detto che non aveva informazioni finanziarie rilevanti. Email lei a .