Nel Marzo 2017, una mini-simposio al 11 ° Congresso di Controversie in Neurologia (CONy), Atene, Grecia, era dedicato alla neuro-Behçet (NBD). Un’introduzione alle caratteristiche cliniche chiave della malattia di Behçet (BD) è stata seguita da una revisione delle sue manifestazioni neurologiche e una presentazione mirata delle sfide della diagnosi differenziale. Questa recensione rappresenta una relazione del mini-simposio sotto forma di una sintesi aggiornata degli argomenti che sono stati presentati. Segue la struttura del mini-simposio e in parte espande le informazioni presentate lì. Tuttavia, una revisione sistematica non rientra nell’ambito di applicazione della presente relazione. L’introduzione generale a BD sarà succinta, in quanto il focus di questa recensione è NBD. I dettagli di BD in generale possono essere trovati in recensioni recenti, ad esempio, Yazici et al.1
Malattia di Behçet
Storia ed epidemiologia
La BD è una malattia cronica, multisistemica e polisintomatica con esacerbazioni e remissioni imprevedibili. Tutti i sistemi possono essere interessati contemporaneamente o consecutivamente.1 Esistono diversi sottoinsiemi clinici e vi è una variazione geografica che indica diversi meccanismi di malattia. In considerazione di ciò, alcuni autori preferiscono usare il termine sindrome di Behçet piuttosto che la malattia di Behçet. Ai fini della coerenza e dell’armonizzazione, e per seguire la terminologia delle discussioni del mini-simposio, questa revisione userà il termine Malattia di Behçet. Nel 1930, l’oftalmologo Adamantiades descrisse la coesistenza di lesioni oculari, cutanee e mucose in un paziente.2 Nel 1937, Hulusi Behçet identificò la BD in due pazienti, che soffrivano di ulcere orali e genitali, oltre alla malattia degli occhi e la descrisse come una malattia separata che si riteneva fosse causata da un virus.3
Gli studi epidemiologici hanno mostrato un’ampia variabilità nella prevalenza di BD a seconda delle origini geografiche ed etniche della popolazione. L’evidenza mostra che la prevalenza di BD è più alta nelle aree in cui la popolazione ha un’alta incidenza di allele HLA-B51.4 È spesso chiamata “malattia della via della seta” a causa della sua prevalenza relativamente alta nei paesi del Mediterraneo, del Medio Oriente e dell’Estremo Oriente lungo l’antica via commerciale della seta. La Turchia ha la più alta prevalenza, a 119,8 per 100.000.4
Fisiopatologia
I patomeccanismi di BD non sono completamente noti; tuttavia, può essere visto come una condizione associata a risposte autoimmuni, autoinfiammazione e lesioni vascolari. La suscettibilità sembra essere determinata da un’interazione tra fattori genetici e ambientali. Tra i geni di suscettibilità, quelli per citochine come interleuchina (IL)-17, IL-12, IL-23, IL-21, IL-23, fattore di necrosi tumorale (TNF)-α, IL-1β e IL-8 sono stati implicati.5 La disregolazione di queste citochine proinfiammatorie può riflettere un’attivazione incontrollata del sistema immunitario innato con o senza attivazione delle risposte immunitarie adattive che sembrano essere responsabili delle caratteristiche patologiche. L’elevata produzione di citochine proinfiammatorie, come TNF-α, IL-1β e IL-8, provoca l’attivazione dei neutrofili e l’aumento delle interazioni cellulari tra neutrofili e cellule endoteliali.6 Questi neutrofili attivati producono eccessivi superossidi ed enzimi lisosomiali che provocano lesioni tissutali. Le lesioni risultanti sono caratterizzate istologicamente da infiltrati angiocentrici neutrofili con vasculite leucocitoclastica (precoce) o linfocitica (tardiva) con o senza trombosi murale e necrosi.7 Inoltre, la funzione dei linfociti B è stata segnalata come anormale in alcuni pazienti.8
Tra i fattori ambientali responsabili della suscettibilità alla BD, gli agenti infettivi che sono stati implicati più frequentemente includono batteri come Streptococcus sanguinisand virus, principalmente herpesvirus. In effetti, l’interazione gene-ambiente in BD è indicata da studi di genotipizzazione densi che collegano la risposta immunitaria ospite disregolata agli antigeni batterici alla suscettibilità BD.9
Manifestazioni cliniche e diagnosi
BD ha una vasta gamma di manifestazioni cliniche. Le ulcere orali sono di solito il primo sintomo; possono comparire anni prima della diagnosi e sono presenti durante il decorso della malattia a quasi il 100% di frequenza. Nel 75% dei pazienti si osservano afte anogenitali, principalmente sullo scroto e sul pene negli uomini e sulla vulva nelle donne. In circa il 60% dei pazienti, sono state riportate varie lesioni cutanee, che includono eritema nodoso, lesioni papullopustulari, pseudofolliculite, piodermite gangrenoso e vasculite cutanea.1,10
Inoltre, numerose altre aree sono comunemente colpite da BD. Le presentazioni oculari di BD si verificano nel 30-80% dei pazienti (prevalentemente negli uomini) e sono una delle principali cause di morbilità in quanto possono causare cecità, in particolare nell’ambito della vasculite retinica.1 Il coinvolgimento articolare è anche comunemente riportato in BD. Mono / poliartrite in BD è corsivonon erosivo e le articolazioni più colpite sono ginocchia, caviglie, piedi e corsivomani. Il coinvolgimento gastrointestinale è caratterizzato da dolore, emorragia, ulcerazioni della mucosa intestinale o perforazione intestinale. Corsivopuò verificarsi anche coinvolgimento vascolare, più comunemente trombosi venosa periferica profonda/superficiale e anche arteriopatia aneurismatica / occlusiva. Il coinvolgimento cardiaco comprende arterite coronarica, malattia vascolare, trombi intracardiaci o trombosi dei vasi collaterali venosi e vena cava superiore, miocardite e aritmie ventricolari ricorrenti.1 Il coinvolgimento neurologico è anche una manifestazione comune di BD e sarà discusso ulteriormente nella sezione seguente.
I criteri diagnostici per BD sono stati pubblicati 28 anni fa.11 Il criterio principale sono le ulcerazioni orali ricorrenti (aftose o erpetiformi) osservate dal medico o segnalate in modo affidabile dal paziente almeno tre volte in un periodo di 12 mesi. Inoltre, due dei quattro criteri minori devono essere soddisfatti:
- ulcerazione genitale ricorrente;
- lesioni oculari: uveite anteriore, posteriore uveite, le cellule del corpo vitreo con lampada a fessura esame o vasculite retinica osservato da un oculista;
- lesioni della cute: eritema nodoso, pseudofolliculitis, papulopustolosa di lesioni acneiformi noduli post-adolescenziale pazienti che non assumono corticosteroidi; e
- positivo pathergy test (skin prick test): non specifici pelle Italicshyper-reattività in risposta a traumi minori di lettura da parte di un medico a 24-48 ore (>2 mm pustule, dopo avambraccio pelle (5 mm di profondità), bucherellare con 20-22 g ago).
Opzioni di trattamento
L’obiettivo del trattamento BD è quello di sopprimere tempestivamente le esacerbazioni infiammatorie e le recidive per prevenire danni irreversibili agli organi e un approccio multidisciplinare è necessario. La gestione della BD dipende dal fatto che vi siano manifestazioni autolimitanti o da un serio coinvolgimento degli organi e deve essere individualizzata in base all’età, al sesso e al tipo.12,13 Nella malattia sistemica grave, possono essere scelti corticosteroidi per impulso endovenoso seguiti da dosi orali giornaliere, azatioprina, ciclofosfamide, ciclosporina-A, metotrexato, micofenolato mofetile, tacrolimus, interferone (IFN)-α o inibitori del TNF-α (etanercept, infliximab).Un nuovo inibitore orale della fosfodiesterasi-4, apremilast, è stato studiato in pazienti senza coinvolgimento maggiore di organi e ha dimostrato una risposta completa in un numero significativamente maggiore di pazienti.14
Altri trattamenti mirano a controllare i sintomi specifici della BD. Gli inibitori del TNF-α sono altamente efficaci nella BD, in particolare nel coinvolgimento oculare.15,16,17 La somministrazione a lungo termine dell ‘ inibitore del TNF-α infliximab può ridurre la frequenza delle recidive oculari, anche in casi resistenti. Come trattamento di prima linea, infliximab deve essere iniziato in combinazione con un farmaco immunosoppressivo (azatioprina, corticosteroidi o Italicsmetotrexato) e al verificarsi della remissione, i corticosteroidi concomitanti devono essere ridotti. Molti studi hanno dimostrato l’efficacia di infliximab nella BD.15-17 Nei pazienti con interessamento oculare del segmento posteriore, si deve iniziare la terapia con azatioprina, ciclosporina-A, IFN-α o anti-TNF-α, spesso in associazione con corticosteroidi sistemici. Nei pazienti con coinvolgimento oculare del segmento posteriore, si deve iniziare la terapia con azatioprina, ciclosporina-A, IFN-α o anti-TNF-α, spesso associati a corticosteroidi sistemici.12,13
Per la gestione della malattia vascolare maggiore con eventi trombotici nella BD, sono raccomandati corticosteroidi e immunosoppressori come azatioprina, ciclofosfamide o ciclosporina-A,12 e Italicianti-TNF-α potrebbe essere preso in considerazione in pazienti refrattari. Gli anticoagulanti sono considerati quando il rischio di sanguinamento, in generale, è basso e gli aneurismi dell’arteria polmonare coesistenti sono esclusi.12,13 Per i sintomi gastrointestinali, possono essere utilizzati derivati dell’acido 5-aminosalicilico, tra cui sulfasalazina o mesalamina, corticosteroidi sistemici, azatioprina, anti-TNF-α e talidomide. Il coinvolgimento del sistema nervoso centrale, compresi gli attacchi acuti di coinvolgimento parenchimale cerebrale, sono trattati con corticosteroidi ad alte dosi seguiti da assottigliamento, insieme a immunosoppressori. La ciclosporina, sebbene poco costosa, dovrebbe essere evitata a causa del rischio di neurotossicità. L’anti-TNF-α deve essere considerato nella malattia grave o refrattaria come prima linea in corsivo. Il primo episodio di trombosi venosa cerebrale (CVT) deve essere trattato con corticosteroidi ad alte dosi, seguito da assottigliamento. Gli anticoagulanti possono essere aggiunti per una breve durata.
Coinvolgimento neurologico nella malattia di Behçet
Come con la malattia sistemica, le manifestazioni neurologiche della BD sono varie.18-22 Il coinvolgimento neurologico in BD può essere classificato come; 1) primario, in cui il coinvolgimento neurologico è direttamente dovuto a BD ed è chiamato come NBD o sindrome di neuro-Behçet (NBS); e 2) secondario, in cui le manifestazioni neurologiche sono il risultato di complicanze neurologiche secondarie al coinvolgimento sistemico di BD (cioè emboli cerebrali da complicanze cardiache di BD, aumento della pressione intracranica secondaria alla sindrome della vena cava superiore) o a causa delle terapie utilizzate per le manifestazioni sistemiche di BD (cioè neurotossicità del sistema nervoso centrale con ciclosporina; neuropatia periferica secondaria a talidomide o colchicina). Queste sono cause indirette di problemi neurologici in pazienti con BD e non sono definite come NBD.
Il coinvolgimento neurologico primario con NBD si verifica fino al 10% di tutti i pazienti.18-22 NBD si presenta normalmente entro la quarta decade e circa 5 anni dopo l’insorgenza della malattia sistemica. Sebbene alcuni pazienti possano presentare un coinvolgimento neurologico senza soddisfare i criteri di classificazione del Gruppo di studio internazionale (ISG) per BD,11 e una diagnosi di NBD non può essere fatta in genere a meno che non ci siano almeno la storia o le sequele di alcune delle manifestazioni sistemiche di BD. Anche se BD è visto quasi allo stesso modo in entrambi i sessi, NBD è più comune nei maschi (3:1).23 BD e NBD sono rari nella popolazione pediatrica; tuttavia, quando il coinvolgimento neurologico si verifica nei bambini è spesso subito dopo l’insorgenza della malattia sistemica.20.21
I risultati clinici e neuroimaging indicano che ci sono due forme principali di NBD: 1) Malattia parenchimale infiammatoria del SNC (p-NBD); e, meno comunemente, 2) una forma extra-parenchimale (ep-NBD) che coinvolge grandi strutture vascolari extra-parenchimali, principalmente seni durali venosi, causando trombosi del seno venoso cerebrale (CVST). A differenza della p-NBD, la CVST è più comunemente osservata nei pazienti pediatrici con NBD e questi due tipi di coinvolgimento si verificano molto raramente nello stesso individuo e, quindi, è probabile che abbiano diverse patogenesi. Raramente, una meningite asettica può essere la presentazione di NBD extra-parenchimale. Durante il trattamento con NBD si possono osservare sintomi comportamentali e psicotici, definiti “neuro-psico-Behçet”. È anche probabile che le funzioni cognitive siano influenzate in un sottogruppo di pazienti con BD e la disfunzione frontale (esecutiva) è il modello più comune osservato. Il coinvolgimento primario del sistema nervoso periferico è stato riportato in BD, ma è estremamente raro.18,19
Il sintomo neurologico più comune osservato in NBD è il mal di testa, che si verifica sia in NBD parenchimale (p-NBD) che in NBD extra-parenchimale (ep-NBD, CVST). Tuttavia, il mal di testa può anche essere un sintomo di grave infiammazione oculare; può essere associato a esacerbazioni di sintomi sistemici di BD, con alcune caratteristiche simili all’emicrania, ed è indicato come “mal di testa non strutturale di BD”; o può essere indipendente da BD e può coesistere come mal di testa primario a tassi simili con la popolazione generale. Altri sintomi comuni sono debolezza (emiparesi), disturbi dell’andatura (atassia), difficoltà di parola (disartria) e, meno comunemente, alterazioni comportamentali e cognitive. La perdita visiva dovuta a neurite ottica, sintomi sensoriali ed extrapiramidali e convulsioni sono rari.18-22
I criteri della raccomandazione di consenso internazionale (ICR) sono suggeriti per essere utilizzati nella diagnosi di NBD.24 Questi criteri possono essere riassunte come ‘l’insorgenza di sintomi e segni neurologici in un paziente che incontra l’ISG Criteri Diagnostici per il BD non altrimenti spiegata da qualsiasi altra sistemica o di malattie neurologiche o di trattamento e in quale obiettivo anomalie coerente con NBD sono rilevati su esame neurologico, studi di neuroimaging, risonanza magnetica, o anormale del liquido cerebrospinale (CSF) esami’.24 I criteri ICR includono anche un criterio “probabile NBD”, ma si dovrebbe essere più prudenti nel fare una tale diagnosi.
Malattia di neuro-Behçet parenchimale
Circa il 75-80% dei pazienti con NBD presenta un coinvolgimento parenchimale. I principali sintomi e segni di p-NBS includono mal di testa, disartria, atassia, emiparesi e neuropatie craniche (principalmente coinvolgimento dei nervi motore-oculari e facciali) e questi di solito si sviluppano in modo subacuto. p-NBD è una delle principali cause di morbilità e mortalità in NBD. Simile alla sclerosi multipla (SM), il decorso clinico della p-NBD può rimanere con un singolo attacco, può avere una forma recidivante o può essere progressivo. Tuttavia, i pazienti con p-NBD di solito sono lasciati con deficit neurologici. Le lesioni delle lesioni p-NBD coinvolgono comunemente la giunzione telencefalica / diencefalica e il tronco cerebrale, che di solito sono grandi, senza confini distinti. Nella fase acuta queste lesioni sono suscettibili di migliorare e generalmente appaiono in un modello eterogeneo. Le lesioni cerebrali tumefattive possono essere viste e le lesioni del midollo spinale, sebbene non comuni, quando accadono sono probabili essere longitudinalmente estese. In questi pazienti, gli anticorpi anti-MOG e AQP4 sono tipicamente assenti. Il coinvolgimento focale cerebellare è raro, ma è stata riportata atrofia cerebellare isolata.25 Le lesioni nei territori arteriosi principali intra-parenchimali sono insolite e il coinvolgimento di grandi arterie extra-parenchimali o intra-parenchimali più piccole, sebbene siano state riportate estremamente rare, suggerendo che potrebbe esistere un sottogruppo di p-NBD arterioso.26 Sulla base dei risultati radiologici e istopatologici, una patogenesi venosa è la probabile spiegazione delle lesioni p-NBS.17-19, 26
I risultati del CSF possono rivelare una pleocitosi prominente e un livello proteico elevato durante l’episodio acuto di p-NBD. La predominanza neutrofila è tipica durante la fase acuta, ma in seguito viene sostituita da una forma linfocitica. Le bande oligoclonali sono raramente rilevate.
Malattia di neuro-Behçet extra-parenchimale/trombosi del seno venoso cerebrale
Fino al 20% dei pazienti con NBD ha CVST. Questi pazienti presentano un forte mal di testa, che di solito si sviluppa in poche settimane. Tipicamente, l’esame fundoscopico e neurologico mostra papilledema e occasionalmente una paralisi del sesto nervo. Rispetto ad altre cause di trombosi del seno durale, la compromissione della coscienza, i deficit neurologici focali come l’emiparesi e le crisi epilettiche sono rari nella NBD extra-parenchimale e gli infarti venosi sono improbabili. Una venografia a risonanza magnetica confermerà la diagnosi e mostrerà l’estensione del CVST. Ad eccezione di una pressione di apertura elevata, i risultati del CSF sono generalmente normali, tranne che nella rara presentazione meningitica in cui è possibile trovare un numero elevato di neutrofili. Come già accennato, questa forma di NBD si verifica più comunemente nella popolazione pediatrica suggerendo che l’età può influenzare la forma di coinvolgimento neurologico.
Malattia di Neuro-Behçet-diagnosi differenziale
La diagnosi differenziale di NBD rimane una sfida importante. Particolarmente difficili sono le situazioni in cui un paziente senza BD in piena regola presenta manifestazioni neurologiche. È importante sapere che le manifestazioni neurologiche di BD riflettono la malattia più grave e sono raramente osservate in isolamento. Pertanto, i medici che sospettano NBD devono essere vigili per cercare il probabile sviluppo di sintomi e segni al di fuori del SNC. Questo è importante anche nei pazienti con BD noto, poiché le manifestazioni neurologiche tendono ad apparire durante gravi riacutizzazioni e devono essere ricercate manifestazioni sistemiche di BD. Nelle presentazioni meningitiche, la diagnosi differenziale dalla meningite batterica acuta è essenziale. La meningite batterica acuta è un’emergenza medica ed il trattamento antibiotico è iniziato spesso nelle regolazioni di emergenza prima della conferma microbiologica. Sebbene il CSF in NBD meningitico abbia spesso meno leucociti, a volte può raggiungere i numeri incontrati nella meningite batterica e il fallimento del riconoscimento può avere gravi conseguenze. Un miglioramento clinico transitorio può essere visto dopo l’istituzione delle misure di sostegno e degli antibiotici, che possono ritardare il trattamento aggressivo di BD.
Le sindromi uveomeningee sono un gruppo eterogeneo di disturbi infiammatori caratterizzati da infiammazione meningea e coinvolgimento oculare (uveite).27 La diagnosi differenziale include molte entità e le caratteristiche sistemiche associate, il coinvolgimento specifico degli organi (ad esempio polmone nella sarcoidosi) e le caratteristiche di imaging e biomarcatori possono aiutare a distinguere la NBD dalle altre condizioni. Oltre alla NBD, le sindromi uveomeningee includono:
- sarcoidosi;
- granulomatosi con poliangiite;
- sifilide;
- Malattia di Vogt-Koyanagi-Harada; e
- epiteliopatia acuta del pigmento placoide multifocale posteriore.
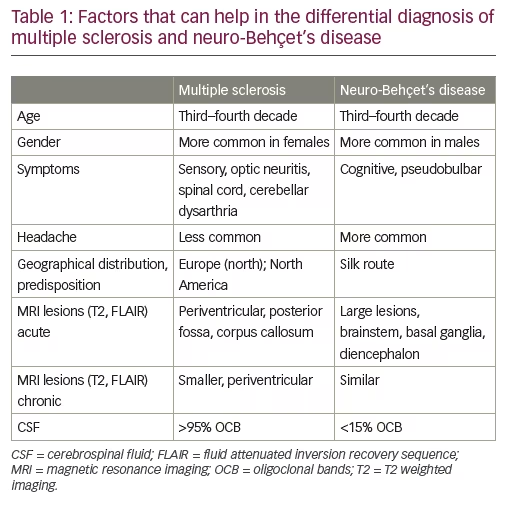
Una delle considerazioni più importanti e stimolanti nella diagnosi differenziale di NBD è MS. 18,28 Quando la diagnosi per entrambe le entità è ben stabilita, la distinzione è relativamente facile; tuttavia, nelle fasi iniziali, la distinzione può essere difficile. Le lesioni parenchimali di NBD possono imitare quelle di MS su MRI nella maggior parte degli aspetti, compreso la forma ovoidale delle “dita di Dawson” callose e la presenza di una vena centrale. A causa della distribuzione perivenulare delle lesioni in entrambe le condizioni, l’utilità del segno centrale e il suo ruolo nella diagnosi differenziale della SM rispetto alla NBD rimangono oggetto di dibattito nelle discussioni di consenso degli esperti.28,29 Mentre questo è particolarmente rilevante all’inizio della malattia e recenti evidenze mostrano che più MS rispetto alle lesioni di sostanza bianca NBD hanno vene centrali, bisogna tenere presente che generalmente i pazienti con NBD hanno meno lesioni di sostanza bianca rispetto ai pazienti con SM, quindi l’uso della vena centrale per la distinzione può rimanere difficile. Altri problemi che sono stati utili per distinguere le due entità possono essere visti nella Tabella 1. È importante notare che la manifestazione iniziale di NBD può essere una lesione cerebrale tumefattiva, che può essere quasi indistinguibile sia da una presentazione tumefattiva della SM che da un tumore cerebrale, quest’ultimo essendo una considerazione essenziale della diagnosi differenziale.30,31 I medici devono essere consapevoli che NBD e SM non devono escludersi a vicenda. In effetti, un gruppo di pazienti con NBD consolidata soddisfa anche i criteri diagnostici per la SM e ha caratteristiche cliniche, di imaging e di laboratorio (bande oligoclonali nel CSF) della SM.32
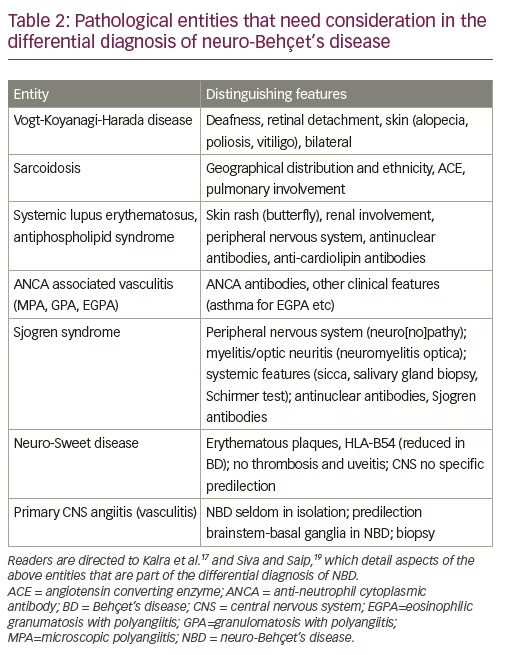
Un altro aspetto importante della diagnosi differenziale è la vasculite sistemica, che può essere primaria o secondaria ad altre malattie infiammatorie sistemiche con manifestazioni neurologiche. La tabella 2 presenta un elenco di malattie infiammatorie sistemiche con o senza vasculite secondaria che possono essere mal diagnosticate come NBD e le loro caratteristiche distintive che possono aiutare nella diagnostica differenziale di NBD. Questi sono discussi in modo più dettagliato in Kalra et al. e Siva e Saip.18,24
Nei pazienti che presentano ictus acuto, la variante vascolare di NBD a volte rappresenta parte della diagnosi differenziale. Per distinguere dall’ictus aterosclerotico non vasculite, è utile tenere presente la maggiore frequenza di trombosi venosa rispetto all’ictus arterioso del territorio in NBD. D’altra parte, alcuni tratti in NBD coinvolgono territori arteriosi, quindi un ictus arterioso può essere una manifestazione di NBD. È anche importante ricordare che i pazienti con BD sono a più alto rischio di eventi cardiovascolari incluso l’ictus, indipendentemente dal fatto che abbiano NBD.33 Dissezioni arteriose e sanguinamenti, anche se relativamente rari in NBD, dovrebbero innescare il sospetto di esso nel contesto clinico appropriato.
La NBD psichiatrica è una manifestazione rara, di solito con una presentazione subacuta e progressiva, e ha manifestazioni molto diverse, imitando la demenza degenerativa primaria, la depressione o la psicosi franca. È molto importante considerare NBD in tali pazienti.34
Un aspetto importante della diagnosi differenziale è lo sviluppo di un problema neurologico in un paziente con BD stabilito. I medici devono stabilire se il problema è correlato o meno alla NBD. Oltre all’ictus, il mal di testa è una lamentela molto comune nelle persone con BD e generalmente non rappresenta una manifestazione di NBD. La vigilanza è necessaria, tuttavia, poiché il mal di testa spesso annuncia altre manifestazioni di NBD.
La neuropatia periferica si verifica raramente come manifestazione clinica di NBD e quando diagnosticata in una persona con BD e senza altre manifestazioni neurologiche, è giustificata una ricerca di eziologie alternative.35
Infine, un aspetto emergente della diagnosi differenziale riguarda le complicanze neurologiche del trattamento con BD. È fondamentale non confondere tali complicazioni per lo sviluppo di NBD. Il ruolo della ciclosporina in NBD è importante poichè è stato collegato coerente ad un’accelerazione e ad un peggioramento potenziali su NBD. Altri trattamenti possono anche avere complicazioni. Gli agenti immunosoppressivi possono occasionalmente facilitare la meningite, che può essere confusa per NBD. L’uso di agenti anti-TNF come infliximab, che ha dimostrato di avere successo nella NBD,36 dovrebbe richiedere vigilanza, poiché con questi agenti sono state riportate demielinizzazione e altre complicanze neurologiche, sebbene nessuna sia stata ancora riportata con l’uso nella BD.
La talidomide, che viene occasionalmente utilizzata per la BD, provoca prevedibilmente una neuropatia non correlata alla NBD. La sindrome da encefalopatia reversibile posteriore è stata riportata come complicazione di diverse terapie immunitarie tra cui agenti anti-TNF, e al simposio CONy 2017, un caso interessante in BD è stato riportato dal Dr George Vavougios dalla Grecia (Comunicazione orale, Congresso CONy, Atene 2017).
In conclusione, NBD è una condizione neuroinfiammatoria grave che pone importanti sfide diagnostiche, diagnostiche differenziali e terapeutiche. La consapevolezza delle sue caratteristiche cliniche e possibilità terapeutiche insieme alla diagnosi precoce sono essenziali nella gestione di NBD.