Riconoscere la normale muscolatura liscia è solitamente semplice; è caratterizzato da fasci intrecciati di cellule fusi uniformi con lunghi nuclei ovali con estremità smussate e processi citoplasmatici bipolari affusolati. A causa delle disposizioni fascicolari, i nuclei appaiono piccoli e rotondi quando tagliati in sezione trasversale, ma lunghi e ovali quando tagliati longitudinalmente (vedi immagine seguente).
 Normali fascicoli della muscolatura liscia.
Normali fascicoli della muscolatura liscia. I leiomiomi presentano occasionalmente nucleoli piccoli ma cospicui e lievi irregolarità del confine nucleare. Occasionalmente, un leiomioma ha componenti amartomatose come grasso, cartilagine e ossa; tali tumori sono nominati in accordo con le caratteristiche dei componenti (ad esempio, lipoleiomioma, leiomioma condroide) e non hanno alcun rapporto con il potenziale maligno.
Raramente, le cellule muscolari lisce appaiono basaloidi e meno fascicolari e assomigliano allo stroma endometriale, aumentando la possibilità di un nodulo stromale o, di maggiore importanza clinica, sarcoma stromale endometriale. In questi casi, gli indizi istologici che la neoplasia è muscolo liscio includono la crescita fascicolare e vasi di grosso calibro. La differenziazione mediante immunoistochimica può essere utile, ma sfortunatamente non è sempre illuminante (vedi Immunoistochimica). La valutazione per i bordi infiltrativi caratteristici del sarcoma stromale endometriale è utile.
Sebbene benigna, leiomyomata può crescere a dimensioni estremamente grandi (20-30 cm). Sebbene nei tessuti molli un tale tumore sarebbe per definizione considerato un tumore maligno, questo non è vero per i tumori che si verificano nell’utero. A causa di influenze ormonali, i leiomiomi possono essere molto ipertrofici e mitoticamente attivi.
È comune che si verifichino infarti. Questi sono di solito facilmente riconoscibili dalla formazione di cicatrici lungo la periferia dell’infarto (classificato come necrosi ialina) (vedi l’immagine sotto). Inoltre, in un infarto, la muscolatura liscia e i vasi sono necrotici.
 Necrosi ialinizzata caratterizzata da formazione di cicatrici.
Necrosi ialinizzata caratterizzata da formazione di cicatrici. Dopo un infarto, il leiomioma a volte subisce un cambiamento idropico. La matrice allentata diventa edematosa, dando un aspetto mixoide alla lesione. Un indizio per il cambiamento idropico è la presenza di grandi vasi che galleggiano nello spazio vuoto, con le cellule muscolari lisce spinte verso la periferia. L’atipia reattiva e le mitosi aumentate sono viste frequentemente adiacente ad un’area di infarto; pertanto, l’atipia citologica deve essere valutata lontano dalle regioni di necrosi o infarto.
I leiomiosarcomi sono rari e di solito sono facili da diagnosticare. La valutazione delle seguenti 3 caratteristiche continua ad essere il mezzo più affidabile per valutare la malignità: attività mitotica, necrosi delle cellule tumorali e atipia citologica. Data l’importanza di queste caratteristiche, ciascuna è discussa di seguito.
Attività mitotica
Di per sé, l’indice mitotico non è un predittore indipendente di malignità. I leiomiomi mitoticamente attivi sono ben studiati e riportati. Questi sono definiti come tumori muscolari lisci con fino a 20 mitosi / 10 campi ad alta potenza (HPF), ma sono privi di atipia e necrosi delle cellule tumorali. Sebbene questa caratteristica da sola non denoti la malignità, quando altre caratteristiche preoccupanti sono presenti, l’attività mitotica diventa estremamente importante nella valutazione del potenziale maligno.
Per misurare l’indice mitotico, trovare l’area più mitoticamente attiva del tumore (ma evitare le aree adiacenti alla necrosi ialinizzata) e contare 10 HPF (40×).
I corpi apoptotici, le cellule muscolari lisce degeneranti e i linfociti infiltranti possono talvolta simulare figure mitotiche; pertanto, i conteggi mitotici dovrebbero includere solo mitosi definitive. Se si trova più di una singola figura mitotica atipica, è necessaria una valutazione vigile; il tumore non deve essere categoricamente classificato come benigno. Possono essere prese in considerazione diagnosi multiple, tra cui neoplasia atipica della muscolatura liscia, neoplasia della muscolatura liscia di basso grado e leiomiosarcoma.
Atipia citologica
Il miometrio non neoplastico adiacente può essere utilizzato come controllo interno per l’istologia basale della muscolatura liscia del paziente. Tipicamente, i leiomiomi hanno solo cellule leggermente più grandi e irregolarità focali della membrana nucleare. L’atipia citologica viene valutata mediante la determinazione della dimensione nucleare, l’esame dei contorni della membrana e la valutazione della prominenza e del numero di nucleoli (vedere l’immagine sotto).
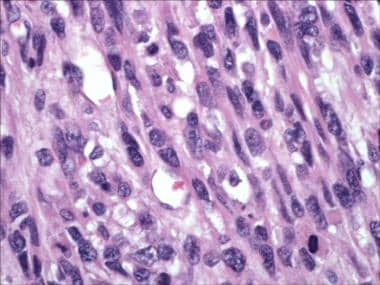 Leiomiosarcoma con atypia citologica marcata.
Leiomiosarcoma con atypia citologica marcata. È ben noto che in assenza di altre caratteristiche, l’atipia citologica grave focale è solitamente benigna (forse simile a cambiamenti antichi in altri tumori, come gli schwannomi). Questi tumori erano chiamati leiomiomi simplastici e ora sono classificati come leiomioma con atipia (vedere l’immagine seguente). L’atipia grave diffusa non è una caratteristica tipica dei tumori benigni e deve essere valutata con grande cura. In questi casi, l’indice mitotico aiuta a classificare il tumore.
 Leiomioma con atipia (precedentemente chiamato simplastico leiomioma). Si noti la natura focale dell’atipia grave. Per definizione, i tumori di questo tipo sono privi di necrosi delle cellule tumorali e mitosi superiori a 10 mitosi per 10 campi ad alta potenza (HPF).
Leiomioma con atipia (precedentemente chiamato simplastico leiomioma). Si noti la natura focale dell’atipia grave. Per definizione, i tumori di questo tipo sono privi di necrosi delle cellule tumorali e mitosi superiori a 10 mitosi per 10 campi ad alta potenza (HPF). Necrosi coagulativa delle cellule tumorali
Delle 3 caratteristiche discusse, la necrosi coagulativa delle cellule tumorali sembra essere la caratteristica istologica più predittiva della malignità. Il problema più grande è riconoscerlo e non classificarlo come necrosi infartuale / ialinizzata. La necrosi coagulativa delle cellule tumorali è caratterizzata da un brusco cambiamento di miociti vitali adiacenti ai miociti necrotici senza un bordo sclerotico intermedio (che è caratteristico degli infarti) (vedere l’immagine seguente). Le singole cellule tumorali necrotiche (cellule fantasma) sono solitamente distinguibili e le navi sono solitamente ancora vitali.
 Leiomioma con atipia (precedentemente chiamato simplastico leiomioma). Si noti la natura focale dell’atipia grave. Per definizione, i tumori di questo tipo sono privi di necrosi delle cellule tumorali e mitosi superiori a 10 mitosi per 10 campi ad alta potenza (HPF).
Leiomioma con atipia (precedentemente chiamato simplastico leiomioma). Si noti la natura focale dell’atipia grave. Per definizione, i tumori di questo tipo sono privi di necrosi delle cellule tumorali e mitosi superiori a 10 mitosi per 10 campi ad alta potenza (HPF). Se ci sono ampie aree di necrosi ialinizzata e un’area focale sospetta di necrosi delle cellule tumorali, i livelli possono talvolta aiutare a identificare un bordo sclerotico e confermare infarti più giovani. Inoltre, se un mioma è stato embolizzato prima dell’intervento chirurgico per controllare il sanguinamento, le caratteristiche istologiche assomiglieranno alla necrosi delle cellule tumorali, anche se i vasi all’interno delle aree di necrosi saranno anche necrotici. Se la necrosi delle cellule tumorali è in questione, il campionamento aggiuntivo della massa miomatosa può aiutare a chiarire il tipo di necrosi, sia attraverso ulteriori focolai di necrosi delle cellule tumorali o altre caratteristiche caratteristiche del leiomiosarcoma.
Il termine “tumore della muscolatura liscia di potenziale maligno incerto” (MONCONE) viene talvolta applicato a casi in cui vi sono caratteristiche indeterminate di malignità o una combinazione di caratteristiche insolite e quindi non sono riportate estesamente in letteratura. Questo termine dovrebbe essere riservato ai casi in cui il potenziale maligno è realmente sconosciuto e dovrebbe essere usato con parsimonia.
STUMP è essenzialmente una non diagnosi ed è irto di frustrazione per medici e pazienti. La maggior parte degli studi sul MONCONE riporta risultati benigni, che probabilmente riflettono il fatto che il termine è sovra-utilizzato. Se il tumore ha caratteristiche che di solito sono benigne, ma se sono noti rari casi di recidiva, il termine “basso potenziale ricorrente” può essere preferibile a MONCONE, perché quel termine trasmette maggiori informazioni sul potenziale maligno previsto e noto.
Il leiomioma metastatico benigno è un tumore mitoticamente inattivo, citologicamente blando, non necrotico che si diffonde ai polmoni e ai linfonodi. Può essere trattato con resezione e terapia ormonale. Questi tumori hanno un profilo citogenetico distinto. Poiché l’istologia del leiomioma metastatico benigno è identica a quella del leiomioma, la diagnosi viene sempre fatta retrospettivamente (ad esempio, in una donna che presenta noduli polmonari). Non ci sono caratteristiche istologiche che aiutano a prevedere quale blando leiomyomata uterina sarà “metastatizzare.”
La leiomiomatosi intravascolare è una blanda proliferazione della muscolatura liscia all’interno dei canali vascolari. Può essere focale (dimostrando intrusione vascolare) o multifocale e grossolanamente visibile. L’intrusione vascolare focale è solitamente auto-limitata. Occasionalmente, leiomiomatosi vascolare prominente ricorre all’interno dei vasi pelvici o addominali; raramente, si estende nella vena cava inferiore e alla fine coinvolge il cuore. Poiché leiomiosarcomi possono coinvolgere i vasi sanguigni, il termine “leiomiomatosi intravascolare” è riservato a quei tumori che non hanno caratteristiche istologiche sospette (vedere l’immagine sotto).
 Invasione vascolare di un leiomiosarcoma.
Invasione vascolare di un leiomiosarcoma. Le neoplasie della muscolatura liscia uterina mixoide (MUSMN) sono rare; questi tumori sono stati riportati solo in pochi piccoli studi. I criteri istologici per predire una lesione mixoide aggressiva sono irti di difficoltà, perché leiomiosarcomi mixoidi possono essere paucicellulari e ingannevolmente blandi. La loro istologia varia da un abbondante stroma mixoide, che ricorda un mixoma (vedi la prima immagine sotto), a un modello di edema polmonare in cui le cellule tumorali hanno alveoli settali sottili (come mostrato nella seconda immagine sotto), a un aspetto più classico della muscolatura liscia simile alla fascite nodulare mixoide. Il pattern mixoide non sembra correlare con il potenziale maligno.
 Il modello di mixoma dei tumori muscolari lisci mixoidi. Questo tumore ha solo atipia minima.
Il modello di mixoma dei tumori muscolari lisci mixoidi. Questo tumore ha solo atipia minima.  Leiomioma mixoide con edema polmonare marcato.
Leiomioma mixoide con edema polmonare marcato. Alcune caratteristiche comuni delle lesioni benigne includono bordi ben circoscritti, citologia blanda e essenzialmente nessuna attività mitotica (meno di 2 per 10 HPF) (vedere l’immagine seguente). Caratteristiche predittivo di malignità includono necrosi delle cellule tumorali (indipendentemente da altre caratteristiche), bordi infiltrativi (riconosciuto dal miometrio normale adiacente strombato e separato dallo stroma mixoide), e mitosi maggiore di 2 per 10 HPF. A causa dell’effetto di diluizione dello stroma mixoide, alcuni ricercatori sostengono il conteggio di 50 HPF per ottenere una migliore rappresentazione dell’indice mitotico.
 Figura mitotica in un tumore della muscolatura liscia mixoide. In media, la maggior parte dei leiomiosarcomi ha almeno 2 mitosi per 10 campi ad alta potenza (HPF) (o superiore a 10 per 50 HPF).
Figura mitotica in un tumore della muscolatura liscia mixoide. In media, la maggior parte dei leiomiosarcomi ha almeno 2 mitosi per 10 campi ad alta potenza (HPF) (o superiore a 10 per 50 HPF). Alcune prime segnalazioni di tumori della muscolatura liscia mixoide hanno rilevato che tumori caratterizzati da un indice mitotico di 0 per 10 HPF, citologia blanda e confini infiltrativi erano associati a risultati scadenti. Sebbene questi risultati non siano stati riprodotti fino ad oggi, probabilmente dovrebbero essere diagnosticati con cura; una categoria di CEPPO può essere più appropriata.
L’edema può assomigliare allo stroma mixoide e può confondere la valutazione di un tumore della muscolatura liscia. L’edema secondario alla degenerazione idropica perinodulare può causare gonfiore del leiomioma (gli autori ne hanno visto uno che misurava 35 cm). La degenerazione idropica è solitamente caratterizzata da edema centrato attorno ai grandi vasi. Ciò si traduce in spostamento delle normali cellule muscolari lisce alla periferia dell’edema. Le navi sembrano galleggiare nello spazio libero. Di solito, in un blando tumore della muscolatura liscia mixoide, le cellule tumorali sono piccole, ma nella degenerazione idropica, le cellule tumorali hanno le dimensioni delle normali cellule muscolari lisce.
I tumori della muscolatura liscia uterina epitelioide sono caratterizzati da cellule poligonali con nuclei rotondi posizionati centralmente. Spesso, una matrice eosinofila acellulare si forma attorno alle cellule, dandole un aspetto osseo quando viene visualizzata sotto l’ingrandimento della scansione. Questi tumori sono stati classificati sotto numerosi nomi, tra cui XYZ. Come con i loro cugini mixoidi, la soglia per classificare i tumori della muscolatura liscia epitelioide come leiomiosarcoma è inferiore rispetto ai normali tumori della muscolatura liscia (vedere le 2 immagini sotto).
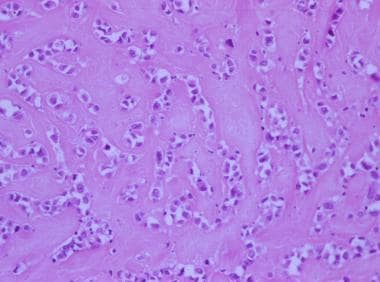 Matrice extracellulare marcata in un leiomioma epitelioide.
Matrice extracellulare marcata in un leiomioma epitelioide.  Tumore cellulare epitelioide della muscolatura liscia.
Tumore cellulare epitelioide della muscolatura liscia. I tumori della muscolatura liscia epitelioide si sovrappongono notevolmente ai tumori delle cellule epiteliali perivascolari (PECOMI). I pecomi sono tumori di differenziazione incerta che spesso si verificano nell’ambito della sclerosi tuberosa. Le cellule muscolari lisce di PEComa condividono l’immunofenotipo dispari di angiomiolipoma e linfangioleiomiomatosi e hanno liscia actina muscolare (SMA) positività così come perivascolare HMB 45 positività (vedere le 2 immagini sotto). Sebbene i pecomi uterini possano anche insorgere nell’ambito della sclerosi tuberosa, la maggior parte sono casi sporadici.
 Tumore a cellule epiteliali perivascolari (PEComa) che dimostra le caratteristiche delle cellule epitelioidi e chiare.
Tumore a cellule epiteliali perivascolari (PEComa) che dimostra le caratteristiche delle cellule epitelioidi e chiare.  HMB45 macchia immunoistochimica di un tumore a cellule epiteliali perivascolari (PEComa) che dimostra immunoreattività focale vicino ai vasi.
HMB45 macchia immunoistochimica di un tumore a cellule epiteliali perivascolari (PEComa) che dimostra immunoreattività focale vicino ai vasi. In 2 studi completi di Vang e Kempson e Folpe et al, la maggior parte dei PECOMI uterini ha avuto un risultato eccellente. Tuttavia, non sono state trovate caratteristiche affidabili per prevedere il potenziale aggressivo. Alcuni autori hanno affermato che la distinzione del PEComa dai tumori della muscolatura liscia epitelioide non è necessaria e la positività HMB45 può essere vista in tumori della muscolatura liscia epitelioide altrimenti usuali. Tuttavia, i geni della sclerosi tuberosa regolano la via Reb / mTOR / p70S6K, e anche casi sporadici di PEComa hanno aumentato i livelli di p70S6K. Questa è un’area potenziale per una terapia mirata come la rapamicina, che inibisce mTOR. Pertanto, anche se la nomenclatura potrebbe non avere importanza, la valutazione genetica potrebbe diventare più critica per possibili vie di trattamento.
Occasionalmente, leiomiosarcomi epitelioidi possono essere infiltrativi e simulare un tumore trofoblastico gestazionale epitelioide. L’età premenopausa, l’estensione delle cellule nel canale endocervicale o disperse in tutto l’endometrio sono modelli insoliti per il leiomiosarcoma. Sebbene la diagnosi differenziale possa essere difficile, la distinzione è facile con l’immunoistochimica.