reacties in oplossing die niet gekatalyseerd worden, zijn traag omdat ladingsontwikkeling en-scheiding optreedt in de overgangstoestand. Wanneer bindingen worden gemaakt of gebroken, worden vaak geladen tussenproducten gevormd die hoger in energie zijn dan de reagentia. Aangezien het tussenproduct hoger in energie is dan de reagentia, zou de overgangstoestand nog hoger in energie zijn, en dus meer lijken op het geladen tussenproduct. Alles wat de ladingen op de tussenliggende en dus de zich ontwikkelende ladingen in de transitiestaten kan stabiliseren, zal de energie van de transitiestaat verlagen en de reactie katalyseren. In deze sectie zullen we het mechanisme onderzoeken dat ten grondslag ligt aan de katalyse door kleine moleculen van chemische reacties. Vermoedelijk zullen biologische macromoleculaire katalysatoren (zoals eiwitenzymen) vergelijkbare mechanismen gebruiken in hun katalytische effecten (die in de volgende sectie zullen worden besproken).
katalysatoren, waaronder enzymen, kunnen ten minste 5 verschillende manieren gebruiken om overgangstoestanden te stabiliseren.
Ladingsontwikkeling in de TS kan worden verminderd door ofwel een proton van algemene zuren (zoals azijnzuur of een geprotoneerde indoolring) te doneren aan een atoom zoals een carbonyl O dat een gedeeltelijk negatieve lading in de TS ontwikkelt wanneer het door een nucleofiel is bevestigd. Protondonatie vermindert het zich ontwikkelende negatief in de TS. Als alternatief kan een nucleofiel zoals water dat een gedeeltelijke positieve lading in de TS ontwikkelt als het een binding begint te vormen aan een elektrofiele C in een carbonyl worden gestabiliseerd door de aanwezigheid van een algemene base (zoals acetaat of de gedeprotoneerde indoolring). Proton abstractie vermindert de ontwikkeling van positieve lading
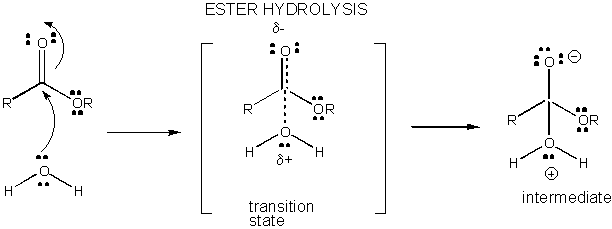
figuur: LADINGSONTWIKKELING in de overgangstoestand voor ESTERHYDROLYSE
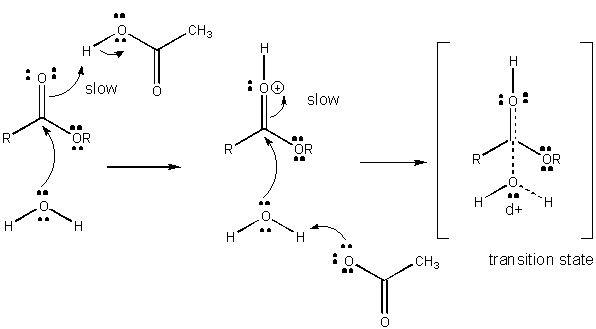
figuur: mechanisme van algemene zure katalyse
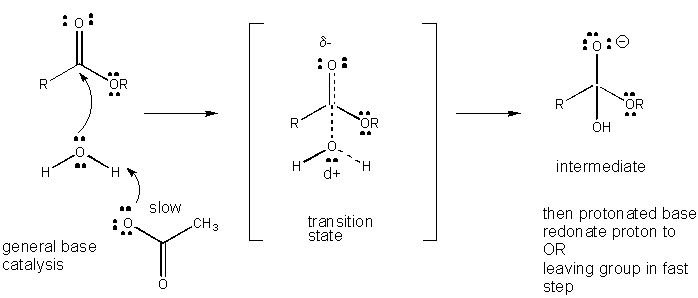
figuur: mechanisme van algemene BASISKATALYSE
bijdragen en toeschrijvingen
- Prof. Henry Jakubowski (College Of St. Benedict/St. John ‘ s University)