vitamine E behandeling voor patiënten met niet-alcoholische Steatohepatitis
Jhonathan Ferney Vélez M. (1), Gustavo Amador Crespo H. (1), Juan Carlos Restrepo G. MD. Esp, MSc, PhD. (2)
(1) medisch Student aan de Faculteit Geneeskunde aan de Universidad de Antioquia in Medellín, Colombia.
(2) universitair hoofddocent bij de afdeling Interne Geneeskunde en de groep Gastrohepatologie aan de Universidad de Antioquia en hepatoloog bij het ziekenhuis Pablo Tobón Uribe in Medellín, Colombia. [email protected]
ontvangen: 12-02-14 aanvaard: 05-11-14
Abstract
non-alcoholische Steatohepatitis (NASH) wordt histologisch gekarakteriseerd door het ballonvaren van hepatocyten, lobulaire ontsteking en steatose. Als deze diagnose wordt vermoed, is het belangrijk om andere oorzaken van leverbeschadiging uit te sluiten, vooral overmatige consumptie van alcohol. Niettemin, tot op heden, een biopsie is de enige beschikbare methode om de diagnose te bevestigen. Vitamine E moet worden beschouwd als een eerstelijnstherapie voor de behandeling van deze ziekte, omdat verschillende klinische studies hebben aangetoond dat een dosis van 800 UI/dag de histologie van niet-diabetische volwassenen die lijden aan NASH verbetert, zelfs wanneer er geen significante invloed is op fibrose. Deze resultaten werden bevestigd door biopsieën. Ondanks de bewezen voordelen van het gebruik van dit medicijn, is het belangrijk om zich ervan bewust te zijn dat het gebruik ervan veranderingen in dieet en lichaamsbeweging niet kan vervangen, maar eerder moet worden gezien als een aanvulling op deze maatregelen.
trefwoorden
niet-alcoholische steatohepatitis, vitamine E, oxidatieve stress.
inleiding
NASH wordt histologisch gekarakteriseerd door het ballonvaren van hepatocyten, lobulaire ontsteking en steatose (1, 2). Op dit moment kan NASH alleen gediagnosticeerd worden door middel van een leverbiopsie, wat de diagnostische gouden standaard is. Het geeft ook informatie over de aanwezigheid en de mate van ontsteking, necrose en fibrose die allemaal belangrijk zijn voor het vaststellen van de prognose van de patiënt (2-5). De verschillen tussen NASH en alcoholische steatohepatitis zijn microscopisch klein waardoor het moeilijk is om histologisch onderscheid tussen hen te maken. Daarom is het belangrijk om bij de patiënt informatie te verkrijgen over zijn of haar drinkgewoonten (4).
NASH maakt deel uit van een veel bredere entiteit genaamd NAFLD (nonalcoholic fatty liver disease) die de vroege stadia van hepatische steatose omvat: steatose zonder ontsteking, en steatose met milde ontsteking. Uiteindelijk ontwikkelt NAFLD zich tot de karakteristieke inflammatoire aandoening van NASH die zich ontwikkelt tot fibrose en uiteindelijk cirrose (1, 2, 5). Het is nog niet helemaal duidelijk dat individuen vooruitgang van eenvoudige steatose naar de inflammatoire toestand. Interacties tussen genetische gevoeligheid, metabole stoornissen en oxidatieve stress zijn de belangrijkste factoren (6, 7).
NAFLD is wereldwijd de meest voorkomende leverziekte (2, 4, 6). De prevalentie van NAFLD wordt geschat op 20% tot 30%, en de prevalentie van NASH wordt geschat op 2% tot 3% in de algemene bevolking van de westerse wereld (8).
vanwege zijn antioxiderende eigenschappen is vitamine E aanbevolen in de huidige Amerikaanse richtlijnen voor de behandeling van NASH. “Vitamine E (α-tocoferol) toegediend in een dagelijkse dosis van 800 IE / dag verbetert de leverhistologie bij niet-diabetische volwassenen met door biopsie bewezen NASH” dit doet niets af aan het belang van interventie in de levensstijl en het dieet van de patiënt als onderdeel van de basisbehandeling voor patiënten met NASH (9, 10). In dit artikel bespreken we de pathofysiologie van NASH met de nadruk op de rol van vitamine E bij de behandeling van patiënten met deze ziekte.
pathofysiologie
hoewel de pathogenese van NASH nog niet helemaal duidelijk is, is de “two-hit” – theorie de beste geaccepteerde hypothese die tot op heden wordt voorgesteld om de gebeurtenissen die leiden tot steatose en vervolgens tot steatohepatitis te verklaren. De eerste hit in het begin van deze ziekte is vetoverbelasting (11, 12). Een sedentaire levensstijl, genetische factoren en verhoogde calorie-inname maakt individuen vatbaarder voor de ontwikkeling van insulineresistentie en hyperinsulinemie die tot een verhoging van leverlipidesynthese en versie van vrije vetzuren uit vetweefsel leidt. Als de lever in deze toestand wordt gehouden, wordt het onbekwaam om alle vetzuren die het produceert en die uit de circulatie worden verwijderd te metaboliseren. Deze aandoening leidt uiteindelijk tot de tweede hit die hepatische steatose en oxidatieve stress (4, 5, 13).
oxidatieve stress is een onbalans die pro-oxidanten bevoordeelt boven antioxidanten (3). Tijdens hepatische steatose komen hepatocyten in een hypermetabole staat die leidt tot verhoogde productie van vrije radicalen in celorganellen (13). Toenemende hoeveelheden reactieve zuurstofsoorten (ROS) in hepatocyten leiden tot lipideperoxidatie, een reactie die een continue toevoer van extra vrije radicalen met potentieel verwoestende effecten biedt (14, 15).
een antioxidant is vitamine E (tocoferol) dat reageert met lipideperoxiden om deze te reduceren tot vetzuren. Ze vormen het relatief stabiele radicale tocoferoxyl dat lang genoeg aanhoudt om door middel van een reactie met vitamine C op het celoppervlak terug te keren naar tocoferol (12). Vanwege deze eigenschap is vitamine E overwogen voor gebruik als een behandeling voor patiënten met NASH (13, 16).
manifestaties en diagnose
NAFLD is een vaak voorkomend syndroom dat varieert van eenvoudige steatose tot steatohepatitis (NASH) met daaropvolgende fibrose en cirrose (5). Hoewel bij de diagnose de meeste patiënten asymptomatisch zijn, kunnen sommige patiënten, vooral kinderen, klagen over vermoeidheid en ongemak. Ongemak in het rechterbovenkwadrant van de buik, verdenking door verhoogde aminotransferasen en een abdominale echografie met een heldere leverziekte zijn allemaal tekenen van deze ziekte. Obesitas, diabetes en dyslipidemie moeten ook in aanmerking worden genomen bij de evaluatie van aandoeningen die geassocieerd kunnen worden met NAFLD en NASH (5, 17).
tijdens de diagnostische evaluatie moeten andere veel voorkomende oorzaken van leverziekte worden uitgesloten, maar uiteindelijk is een leverbiopsie de enige beschikbare methode om de diagnose te bevestigen. Het is ook belangrijk voor het bepalen van de prognose van de patiënt (Tabel 1) (3, 4). Ondanks zijn grote klinische waarde, een biopsie is duur en leidt tot een lichte toename van de morbiditeit en, in zeldzame gevallen, resulteert in mortaliteit. Deze tool mag alleen worden overwogen voor patiënten bij wie de aanwezigheid van niet-alcoholische hepatische steatose wordt vermoed en die een hoog risico hebben op steatohepatitis en gevorderde fibrose (obesitas, type II diabetes mellitus, dyslipidemie en metabool syndroom) en in gevallen van onzekere diagnose (3, 9).

rol van vitamine E bij de behandeling van niet-alcoholische STEATOHEPATITIS
momenteel is er geen effectieve behandeling voor NASH. Niettemin zijn er, gezien de belangrijke rol van vitamine E als antioxidantfactor, verscheidene klinische studies uitgevoerd om de voordelen ervan in de klinische en histopathologische evolutie van deze ziekte aan te tonen (Tabel 2).
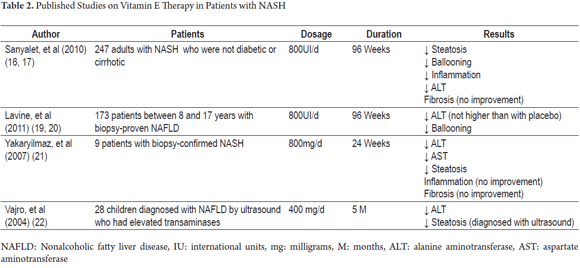
Hieronder valt de studie Pivens (pioglitazon versus vitamine E versus placebo voor de behandeling van niet-diabetische patiënten met niet-alcoholische steatohepatitis). Dit was een multicenter, dubbelblinde, placebogecontroleerde studie waarin histologische verbetering werd geëvalueerd bij 247 niet-diabetische en niet-cirrotische patiënten die NASH hadden. De patiënten kregen na willekeurige selectie een dagelijkse dosis pioglitazon (80 patiënten), vitamine E (84 patiënten) of placebo (83 patiënten) gedurende zesennegentig weken (18). De dagelijkse doseringen waren 30 mg pioglitazon en 800 E voor vitamine E. uit dit onderzoek bleek dat 43% van de patiënten die vitamine E kregen (P = 0,001) verbeterde ten opzichte van 34% van degenen die pioglitazon kregen (P = 0,04) en 19% van degenen die placebo ‘ s kregen. Het verschil in de mate van verbetering tussen pioglitazon en placebo ’s was niet statistisch significant, terwijl het verschil tussen de mate van verbetering van vitamine E en placebo’ s wel significant was. Niettemin werden beide geneesmiddelen geassocieerd met verbetering van aminotransferasespiegels, vermindering van steatose en lobulaire ontsteking, maar geen van beide resulteerde in een verbetering van fibrose. Dezelfde studie toonde aan dat na behandeling met vitamine E gesuspendeerde aminotransferasespiegels waren verhoogd, wat erop wijst dat onbepaalde toediening van de behandeling noodzakelijk kan zijn. Bovendien werden geen significante verschillen gevonden tussen de nadelige effecten van vitamine E en de negatieve effecten van placebo ‘ s (19).
een herbeoordeling van het PIVENS-onderzoek door Hoofdnagle et al. gericht op de respons van serum ALT bij patiënten die vitamine E of placebo ‘ s kregen en op de associatie van deze respons met de initiële klinische, histologische veranderingen en interacties met veranderingen in lichaamsgewicht. Zij stelden vast dat veranderingen in ALT vaker voorkwamen bij degenen die vitamine E kregen (48%) dan bij degenen die placebo ‘ s kregen (16%; p <0,001). Bij de groep die vitamine E kreeg, werden alat-responsen geassocieerd met een verminderde activiteit van niet-alcoholische leververvetting (NAFLD), maar er was geen verbetering in fibrose na het einde van de behandeling na 96 weken. De ALT-spiegels namen toe in de vitamine E-groep na beëindiging van de toediening, maar Namen niet toe in de placebogroep na beëindiging van de toediening. Beide behandelingsgroepen hadden bijna identieke ALT-spiegels in week 120. Deze resultaten zijn vergelijkbaar met die in de volledige cohort van de hoofdpublicatie van de pivens-studie. Bovendien toonden de resultaten aan dat gewichtsverlies (2 kg of meer) ook geassocieerd is met ALT-respons, met verbeterde NAFLD (<0,001) en verbeterde fibrose (p <0,02), maar vitamine E had grotere effecten op NAFLD onafhankelijk van veranderingen in lichaamsgewicht. Tot slot moet worden opgemerkt dat de effecten van vitamine E en gewichtsverlies op de ALAT-respons en histologie onafhankelijk zijn, wat betekent dat zelfs die patiënten die afvallen zouden profiteren van therapie met vitamine E (20).
het TONIC-onderzoek (Treatment of nonalcoholic fatty liver disease in children) was een ander multicenter, dubbelblind, placebogecontroleerd onderzoek. Het omvatte 173 patiënten tussen de leeftijd van acht en zeventien jaar. De patiënten kregen na willekeurige selectie gedurende 96 weken vitamine E (58 patiënten), metformine (57 patiënten) of placebo ‘ s (58 patiënten) toegediend. Doseringen waren 400 IE tweemaal daags voor vitamine E en 500 mg tweemaal daags voor metformine (21). Geen van beide middelen was superieur aan placebo ‘ s voor het bereiken van ofwel aanhoudende verlagingen van ten minste 50% in baseline ALT-spiegels of aanhoudende ALT-spiegels van 40 E/L of minder. De metingen werden om de 12 weken uitgevoerd van week 48 tot week 96. Uit deze studie bleek ook dat de resolutie van NASH significant hoger was in de groep van patiënten behandeld met vitamine E dan in de placebogroep. Dit resultaat werd toegeschreven aan de significante afname van hepatocellulair ballonvaren die werd gevonden bij patiënten behandeld met vitamine E. Dit is vergelijkbaar met de resultaten van PIVENS, hoewel in het TONIC-onderzoek niet werd gekeken naar verminderde hepatocellulaire ballonvaren als primaire uitkomst vanwege de histopathologische verschillen tussen NALFD bij pediatrische patiënten en volwassenen. In het TONIC-onderzoek werd geen verbetering van fibrose vastgesteld (22).
voorafgaand aan deze twee grote studies waren er andere kleinere studies geweest met resultaten met grote verschillen in de beoordeelde primaire resultaten. Naast veel kleinere populaties hadden deze studies minder controletijd en sommige werden niet gecontroleerd met placebogroepen.
een studie uit 2007 van Yakaryilmaz et al. er werd gekeken naar het effect van vitamine E op negen patiënten bij wie de diagnose van NASH door biopsie was geverifieerd. De studie evalueerde het effect van vitamine E op de peroxisome proliferator-activated receptor gamma (PPARG) en op insulineresistentie. De patiënten kregen gedurende 24 weken dagelijks 800 mg vitamine E. Voordat met de behandeling werd begonnen, werden de levers van de patiënten biochemisch en histologisch geëvalueerd. Deze evaluaties werden herhaald na beëindiging van de behandeling. Aan het einde van de 24 weken werden statistisch significante dalingen van ASAT, ALAT en steatose gevonden, maar er werden geen histologische veranderingen gevonden in het niveau van ontsteking en fibrose. Geen enkele patiënt ondervond bijwerkingen bij deze dosering van vitamine E (23).
Vajro, et al. (2004) een studie uitgevoerd bij een groep van 28 kinderen met obesitas gerelateerde leverdisfunctie. De patiënten werden in twee groepen verdeeld. De gemiddelde leeftijd van groep één was 9,88 (+/- 3,97) jaar, en van groep twee was 10,7 (+/- 3,45). De patiënten werden geëvalueerd om vast te stellen of de behandeling met vitamine E gunstige effecten had op gewichtsverlies, transaminasespiegels en steatose gemeten door middel van echografie. De kinderen in deze studie hadden allemaal chronische hypertransaminasemie (ASAT-of ALAT-waarden 1,5 keer boven de normale waarde gedurende meer dan 6 maanden) en tekenen van steatose bij echografie. De studie had een enkelblind ontwerp waarbij patiënten werden gerandomiseerd in een van de twee groepen: Groep 1 (placebo plus dieet) en groep 2 (vitamine E + dieet). Later werd elke groep onderverdeeld afhankelijk van de therapietrouw van de patiënt. Groep 1 werd onderverdeeld in subgroep 1A voor degenen die aan het dieet voldeden en subgroep 1B voor degenen die niet voldeden. Groep 2 werd onderverdeeld in subgroep 2A voor degenen die aan vitamine E therapie hadden voldaan en subgroep 2B voor degenen die niet aan vitamine E therapie hadden voldaan. Subgroep 2A werd verder onderverdeeld in subgroep 2A1 voor degenen die niet aan het dieet voldeden en subgroep 2A2 voor degenen die wel aan het dieet voldeden. De studie toonde aan dat de 400 mg/dag dosering van vitamine E significante dalingen in ALT-waarden voor patiënten in subgroep 2A veroorzaakte die normalisatie naderden onafhankelijk van veranderingen in gewicht. Aan de andere kant bereikten die patiënten die hoge serumspiegels van vitamine E bereikten en ook gewicht verloren, ALT-normalisatie en remissie van steatose. Verder bleek uit een vergelijking tussen subgroep 1A die alleen aan dieet voldeed en subgroep 2A1 die alleen aan vitamine E-therapie voldeed, dat beide groepen patiënten na twee maanden monitoring verlaagde ALT-spiegels hadden, maar dat er een grotere afname was in subgroep 1A (die alleen aan dieet voldeed) dan in subgroep 2A1 (die alleen aan vitamine E voldeed) na vijf maanden monitoring. Alle tekenen van steatose verdwenen uit ultrasone beelden in subgroep 2A2 die gewicht verloren tijdens de behandeling met 400 mg vitamine E. Deze resultaten benadrukken het belang van het bevorderen van gezond eten als een van de belangrijkste behandelingsinterventies voor patiënten met NASH, maar we moeten ook opmerken dat veel patiënten niet voldoen aan dieetregimes die leiden tot het falen van de interventie. Dit onderstreept het belang van het gebruik van antioxidanten zoals vitamine E als een goede alternatieve therapie voor deze patiënten (24).
a pilot study by Kugelmas, et al. (2003) evalueerde de effecten van Stap 1 van de American Heart Association dieet gecombineerd met verhoogde aërobe oefening met en zonder dagelijkse toediening van vitamine E op de profielen van cytokines (TNF alfa, IL-8, IL-6) en niveaus van leverenzymen bij 16 patiënten tussen 18 en 65 jaar met biopsie bewezen NASH. Dit was een enkelblind onderzoek waarbij patiënten na willekeurige selectie 800 IE vitamine E per dag kregen toegewezen. Patiënten die geen vitamine E kregen, kregen placebo ‘ s. De test werd uitgevoerd over een periode van 12 weken. Cytokinewaarden daalden niet significant bij gewichtsverlies met of zonder toediening van vitamine E tijdens de studie. De veranderingen in levensstijl werden geassocieerd met verbeteringen in leverenzymen en plasmacholesterol bij patiënten met NASH, terwijl de dosering van vitamine E die in deze studie werd gebruikt geen extra voordeel toonde. Dit resultaat kan te wijten zijn aan de kleine steekproefgrootte, de korte follow-up tijd, of de dosering van de gebruikte vitamine E (25, 26).
een review gepubliceerd in November 2013 over de momenteel beschikbare opties voor de behandeling van patiënten met NASH erkende de huidige aanbeveling voor het gebruik van vitamine E als eerstelijnsbehandeling bij patiënten met NASH bevestigd door biopsie die niet cirrotisch zijn en die geen diabetes hebben, maar benadrukte ook het feit dat deze therapie slechts een significant voordeel heeft aangetoond bij minder dan de helft van de patiënten. Daarom werd in het onderzoek geconcludeerd dat toekomstige behandelingsstrategieën gebaseerd moeten zijn op pathways van pathogene ziekten als er ooit een effectieve behandeling voor patiënten met NASH zal worden ontwikkeld (27).
Ji H-F et al. een meta-analyse uitgevoerd om het effect van vitamine E op het verminderen van aminotransferasen te evalueren bij patiënten met NAFLD, NASH en chronische hepatitis C (CHC). In de vier studies die zij onderzochten, waren patiënten met NASH opgenomen die vitamine E-supplementen kregen. De studies omvatten de onderzoeken TONIC en PIVENS. Ze vonden dat vitamine E de AST-en ALT-spiegels bij deze patiënten kon optimaliseren. Er zij echter op gewezen dat deze meta-analyse werd beperkt door het onvermogen om het onvermogen uit te sluiten om effecten uit te sluiten van interventies met veranderingen in levensstijl, lichaamsbeweging en het gebruik van andere antioxidanten en het onvermogen om de effecten van andere risicofactoren voor chronische leverziekte zoals alcohol-en drugsgebruik uit te sluiten, daarbij moet rekening worden gehouden met de heterogeniteit van de onderzoeken, aangezien deze de algemene analyse beperkt en minder specificiteit voor aminotransferasespiegels heeft dan biopsieën genomen op het moment van diagnose en beoordeling van leverziekte (28).
hoewel we bij de belangrijkste studies om het effect van het gebruik van vitamine E bij patiënten met NASH te beoordelen geen statistisch significante verschillen hebben gevonden met het gebruik van placebo ‘ s en andere therapeutische opties op korte termijn, bestaat er bezorgdheid over mogelijke nadelige effecten van langdurig gebruik van vitamine E.
een systematische beoordeling van negen gerandomiseerde onderzoeken omvatte nieuwe gerandomiseerde placebogecontroleerde onderzoeken om de effecten van vitamine E gedurende een periode van ten minste één jaar op de totale incidentie van cerebrovasculaire accidenten en subtypes van cerebrovasculaire accidenten te evalueren. Er werd een verhoogd risico op hemorragische beroerte vastgesteld (RR = 1,22, 95% BI: 1,0 tot 1,48, p = 0,045). Op grond van de resultaten van hun beoordeling raden de onderzoekers aan om willekeurig gebruik van vitamine E te vermijden vanwege de ernstige gevolgen van hemorragische beroertes in morbiditeit en mortaliteit (29).
in een gerandomiseerd placebogecontroleerd onderzoek met 35.533 patiënten die minimaal zeven jaar werden gevolgd, werden de risico ‘ s van vitamine E in verband met prostaatkanker bestudeerd. Het vergeleek een placebogroep met een groep die vitamine E kreeg in een dagelijkse dosis van 400 IE. Er was een significante toename van het risico op prostaatkanker bij degenen die vitamine E namen (HR 1,17; 99% BI, 1,004-1,360; p = 0,008). De absolute toename van het risico was 1,6 per 1000 persoonsjaren (30).
een andere meta-analyse heeft gekeken naar de dosis-respons relatie van vitamine E suppletie en totale mortaliteit bij volwassenen. Het toonde aan dat patiënten die hoge doses vitamine E kregen (meer dan of gelijk aan 400 IE/dag) een verhoogde mortaliteit hadden, ongeacht de oorzaak. Deze meta-analyse beperkte het onderzoek tot gerandomiseerde gecontroleerde studies waarbij de patiëntstalen bestonden uit volwassenen die behandeld werden met vitamine E alleen of in combinatie met andere vitaminen of mineralen en waarbij zwangere vrouwen werden uitgesloten en die minimaal 1 jaar behandeling en controle hadden. De resultaten van deze meta-analyse dienen met voorzichtigheid te worden overwogen, omdat verschillende van de onderzoeken een kleine steekproefomvang hebben en werden uitgevoerd bij patiënten met verschillende chronische ziekten. Dit beperkt het vermogen van de studie om resultaten te veralgemenen aan de gezonde volwassen bevolking (31).
conclusie
hoewel er op dit moment geen effectieve medicamenteuze behandeling is voor patiënten met NASH, wijst het bewijs uit de PIVENS-studie erop dat een juiste toediening van vitamine E de leverhistologie verbetert bij volwassen niet-cirrotische patiënten met NASH die geen diabetes hebben. Niettemin zijn er meer studies nodig voordat deze aanbeveling kan worden uitgebreid tot diabetespatiënten of patiënten met cirrose met NASH. Studies uitgevoerd bij pediatrische patiënten met NASH hebben niet voldoende bewijs gevonden om het gebruik van vitamine E te ondersteunen.naast de toediening van vitamine E is aangetoond dat gewichtsverlies steatose en leverontsteking vermindert. Gewichtsverlies door een caloriearm dieet in combinatie met verhoogde fysieke activiteit moet worden aanbevolen voor alle patiënten. Wat de bijwerkingen betreft, hebben we geen statistisch significante verschillen gevonden in kortdurend gebruik van vitamine E met placebo ‘ s en andere behandelingsopties. Toch wordt willekeurig gebruik van vitamine E niet aanbevolen voor lange perioden, omdat er aanwijzingen zijn voor verhoogde risico ‘ s van prostaatkanker, hemorragische beroerte en overlijden door alle oorzaken.
1. Abbas AK, Fausto N. Hígado, vesícula biliar y vías biliares. En: Robbins SL, Mitchell RN, Kumar V, Abbas AK, Fausto N. patología funcional y estructural. 8va Ed. Barcelona: Elsevier; 2012. blz. 645-687.
2. Brunt E, Neuschwander-Tetri B, Burt AD. Leververvetting: alcoholisch en niet-alcoholisch. En: Burt AD, Ferrell, l Portmann BC. MacSween ‘ s pathologie van de lever. 6e editie. UK: Elservier; 2012. p. 293-359.
3. Corrado RL, Torres DM, Harrison SA. Herziening van de behandelingsopties voor niet-alcoholische leververvetting. Med Clin N Am 2014; 98: 55-72.
4. Koek GH, Liedorp PR, Bast A. the role of oxidative stress in non-alcoholic steatohepatitis. Clinica Chimica Acta 2011; 412: 1297-1305.
5. Cortez-Pinto H, Ermelinda Camilo M. Niet-alcoholische leververvetting/niet-alcoholische steatohepatitis (NAFLD/NASH): diagnose en klinisch verloop. Best Practice & Research Clinical Gastroenterology 2004; 18 (6): 1089-104.
6. Mishra A, Younossi ZM. Epidemiologie en natuurlijke geschiedenis van niet-alcoholische leververvetting. Tijdschrift voor klinische en experimentele hepatologie 2012; 2 (2): 135-44.
7. Rolo AP, Teodoro JS, Palmeira CM. Rol van oxidatieve stress in de pathogenese van niet-alcoholische steatohepatitis. Kosteloos Radic Biol Med 2012; 52 (1): 59-69.
8. Machado MV, Cortez-Pinto H. Niet-invasieve diagnose van niet-alcoholische leververvetting. Een kritische beoordeling. Journal of Hepatology 2013; 58 (5): 1007-19.
9. Chalasani N, et al. De diagnose en het beheer van niet-alcoholische vette leverziekte: Praktijkrichtlijn door de American Association for the Study of Liver Diseases, American College Of Gastroenterology, en de American Gastroenterological Association. Hepatologie 2012; 55.
10. Mazzella N, Ricciardi LR, Mazzotti A, Marchesini G. De rol van medicijnen voor het beheer van patiënten met NAFLD. Clin Liver Dis 2014; 18: 73-89.
11. Chunga MY, Yeunga SF, Parka HJ, Volekb JS, Brunoa RS. Dieet α-En γ-tocoferolsuppletie verzwakt lipopolysaccharide-geïnduceerde oxidatieve stress en inflammatoire-gerelateerde responsen in een zwaarlijvig muismodel van niet-alcoholische steatohepatitis. Journal of Nutritional Biochemistry 2010; 21: 1200-1206.
12. Dag CP, James van. Steatohepatitis: een verhaal van twee ‘hits’? Gastroenterology 1998; 114: 842-4.
13. Harper HA, Murray RK, Rodwell VW, Bender DA. Bioquímica ilustrada, 28 ed. México: McGraw-Hill Interamericana; 2010. blz. 484-485.
14. Neuschwander-Tetri BA. Hepatische lipotoxiciteit en de pathogenese van niet-alcoholische steatohepatitis: de centrale rol van nontriglyceride vetzuurmetabolieten. Hepatologie 2010; 52 (2): 774-88.
15. Le T, Loomba R. Management of Non-alcoholic Fatty Liver Disease and Steatohepatitis. Journal of Clinical and Experimental Hepatology 2012; 2: 156-173.
16. Verdam FJ, Dallinga JW, Driessen, de Jonge C, Moonen E, Van Berkel J, Luijk J, Bouvy ND, Buurman AW, Rensen SS, Greve JW. Niet-alcoholische steatohepatitis: een niet-invasieve diagnose door analyse van uitgeademde adem. Journal of Hepatology 2013; 58: 543-548.
17. Palmentieri B, de Sio I, La Mura V, et al. De rol van helder leverecho patroon op echografie b-mod onderzoek in de diagnose van lever steatose. Dig Liver Dis 2006; 38: 485-9.
18. Sanyal AJ, et al. Pioglitazon versus vitamine E versus placebo voor de behandeling van niet-diabetische patiënten met niet-alcoholische steatohepatitis: pivens trial design. Contemp Clin Trials 2009; 30 (1): 88-96.
19. Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, Bass NM, et al. Pioglitazon, vitamine E of placebo voor niet-alcoholische steatohepatitis. N Engl J Med 2010; 362 (18): 1675-85.
20. Hoofdnagle JH, Van Natta ML, Kleiner de, Clark JM, Kowdley KV, Loomba R, et al. Vitamine E en veranderingen in serum alanineaminotransferasespiegels bij patiënten met niet-alcoholische steatohepatitis. Aliment Pharmacol Ther 2013; 38(2): 134-43.
21. Lavine je, Schwimmer JB, Molleston JP, Scheimann EA, Murray KF, Abrams SH, et al. Behandeling van niet-alcoholische leverziekte bij kinderen: TONIC trial design. Contemp Clin Trials 2010; 31( 1): 62-70.
22. Lavine JE, Schwimmer JB, Van Natta ML, et al. Effect van vitamine e of metformine voor de behandeling van niet-alcoholische leververvetting bij kinderen en adolescenten: de tonic gerandomiseerde gecontroleerde studie. JAMA 2011; 305 (16): 1659-68.
23. Yakaryilmaz F, Guliter S, Savas B, Erdem O, Ersoy R, Erden E, et al. Effecten van vitamine E behandeling op peroxisome proliferator-activated receptor-alpha expressie en insulineresistentie bij patiënten met niet-alcoholische steatohepatitis: resultaten van een pilot studie. Intern Med J 2007; 37 (4): 229-35.
24. Vajro P, Mandato C, Franzese A, Ciccimarra E, Lucariello S, Savoia M, et al. Vitamine E behandeling bij pediatrische obesitas gerelateerde leverziekte: een gerandomiseerde studie. J Pediatr Gastro-Enterol Nutr 2004; 38(1): 48-55
25. Papastergiou V, et al. Negen scoremodellen voor kortdurende mortaliteit bij alcoholische hepatitis: kruisvalidatie in een door biopsie bewezen cohort. Aliment Pharmacol Ther 2014; 39: 721-732.
26. Kugelmas M, Hill DB, Vivian B, Marsano L, McClain CJ. Cytokines and NASH: a pilot study of the effects of lifestyle modification and vitamin E. Hepatology 2003; 38 (2): 413-9.
27. Younossi ZM, Reyes MJ, Mishra MA, Mehta R, Henry L. Systematic review with meta-analysis: non-alcoholic steatohepatitis-a case for personalized treatment based on pathogenic targets. Aliment Pharmacol Ther2014; 39: 3-14.
28. Ji HF, et al. Effect van vitamine E-suppletie op aminotransferasespiegels bij patiënten met NAFLD, NASH en CHC: resultaten van een meta-analyse. Voeding 2014; 1-6.
29. Markus s, Robert JG, Pamela MR, Christophe T, Tobias K. effecten van vitamine E op beroerte subtypes: meta-analyse van gerandomiseerde gecontroleerde trials. BMJ 2010; 341.
30. Klein EA, Thompson IM, Tangen CM, et al. Vitamine e en het risico op prostaatkanker: de selenium en vitamine e kankerpreventie trial (select). JAMA 2011; 306 (14): 1549-56.
31. Miller ER, 3rd, Pastor-Barriuso R, Dalal D, Riemersma RA, Appel LJ, Guallar E. Meta-analyse: hoge dosering vitamine E suppletie kan verhogen all-cause mortality. Ann Intern Med 2005; 142( 1): 37-46.