Epóxidas anel de abertura de reações SN1 vs. SN2, regioselectivity, e stereoselectivity
O nonenzymatic anel-reações de abertura de epóxidos fornecer uma boa visão geral de muitos dos conceitos já vimos neste capítulo. As reações de abertura do anel podem prosseguir por mecanismos SN2 ou SN1, dependendo da natureza do epóxido e das condições de reação. Se o epóxido for assimétrico, a estrutura do produto variará de acordo com o mecanismo dominante. Quando um epóxido assimétrico sofre solvólise em metanol básico, a abertura do anel ocorre por um mecanismo SN2, e o carbono menos substituído é o local de ataque nucleofílico, levando ao que nos referiremos como produto B:

inversamente, quando a solvólise ocorre em metanol ácido, a reação ocorre por um mecanismo com caráter substancial de SN1, e o carbono mais substituído é o local de ataque. Como resultado, o produto a predomina.

estes são ambos bons exemplos de reacções regiosselectivas. Em uma reação regiosseletiva, dois (ou mais) isômeros constitucionais diferentes são possíveis como produtos, mas um é formado preferencialmente (ou às vezes exclusivamente).
examinemos primeiro o caso básico, SN2. O grupo de saída é um anião alcóxido, porque não há ácido disponível para protonar o oxigênio antes da abertura do anel. Um alcóxido é um grupo pobre de saída, e assim o anel é improvável de abrir sem um “empurrão” do nucleófilo.

o nucleófilo em si é potente: um ião metoxídeo desprotonado, carregado negativamente. Quando uma reação de substituição nucleofílica envolve um grupo de saída pobre e um poderoso nucleófilo, é muito provável que se proceda por um mecanismo SN2.E o electrófilo? Existem dois carbonos eletrofílicos no epóxido, mas o melhor alvo para o nucleófilo em uma reação SN2 é o carbono que é menos prejudicado. Isto explica o resultado regioquímico observado. Como em outras reações SN2, o ataque nucleofílico ocorre a partir do lado de trás, resultando em inversão no carbono eletrofílico.
provavelmente a melhor maneira de descrever a reação de abertura do anel epóxido catalisada pelo ácido é como um híbrido, ou cruzamento, entre um mecanismo SN2 e SN1. Primeiro, o oxigênio é protonado, criando um bom grupo de saída (Passo 1 abaixo) . Em seguida, a ligação carbono-oxigênio começa a quebrar (Passo 2) e a carga positiva começa a acumular-se sobre o carbono mais substituído (recordar a discussão da seção 8.4 B sobre a estabilidade de carbocação).

ao contrário de uma reação SN1, o nucleófilo ataca o carbono eletrofílico (Passo 3) antes que um intermediário de carbocação completo Tenha a chance de se formar.

o ataque ocorre preferencialmente a partir do lado de trás (como em uma reação SN2), porque a ligação carbono-oxigênio ainda está em algum grau no lugar, e os blocos de oxigênio atacam do lado frontal. Notice, however, how the regiochemical outcome is different from the base-catalyzed reaction: no processo catalisado pelo ácido, o nucleófilo ataca o carbono mais substituído porque é este carbono que detém um maior grau de carga positiva.
exercício 8.17:
prever o(S) produto (s) principal (Is) da reacção de abertura do anel que ocorre quando o epóxido mostrado abaixo é tratado com:
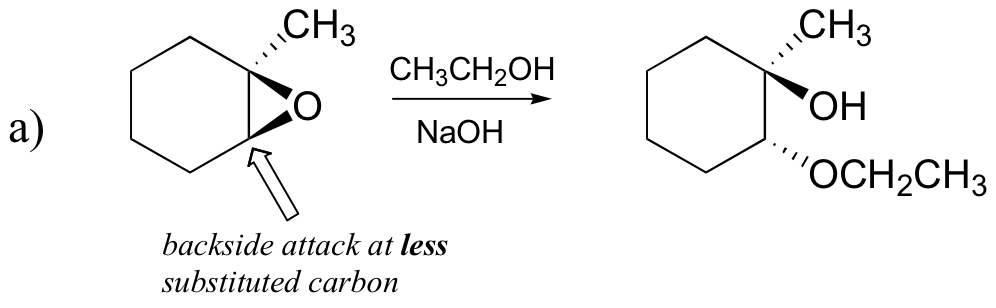
a) etanol e uma pequena quantidade de hidróxido de sódio
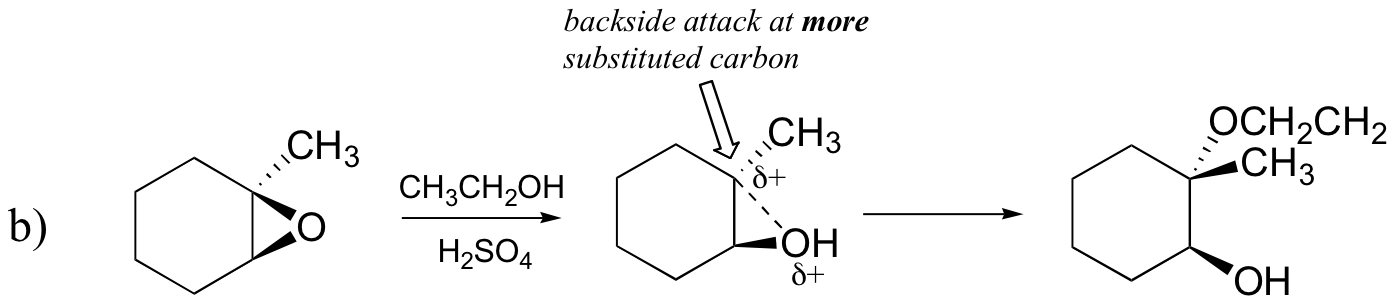
B) etanol e uma pequena quantidade de ácido sulfúrico

sugestão: não se esqueça de considerar tanto a regioquímica quanto a estereoquímica!
vídeos da Khan academy

Anel de abertura sob condições ácidas: