hipersensibilitatea Dentinală este una dintre cele mai frecvente plângeri ale pacienților auzite în practica dentară.1 afectând până la 57% dintre pacienți, se pare că atinge un vârf între 20 și 40.2 prevalența hipersensibilității este ușor mai mare în rândul femeilor,3 cu canini și premolari ai ambelor arcuri cel mai frecvent implicați.4 durerea este adesea cronică și marcată de episoade acute.5
conform Holland et al,6 hipersensibilitatea dentinală este definită ca o „durere scurtă și ascuțită care rezultă din dentina expusă ca răspuns la stimuli, care sunt de obicei termici, evaporativi, tactili și osmotici sau chimici care, de obicei, nu pot fi atribuite niciunei alte forme, defecte dentare sau patologii.”De obicei, durerea este localizată și de scurtă durată. Aceasta diferă de durerea pulpară, care este prelungită, plictisitoare, dureroasă, slab localizată și durează mai mult decât stimulul aplicat.
stresul cauzat de hipersensibilitate poate varia de la minor la sever. Pacienții care suferă de hipersensibilitate severă pot considera că mâncarea și băutul sunt dificile, mai ales atunci când consumă substanțe calde sau reci. Durerea experimentată de persoanele cu sensibilitate este însă extrem de subiectivă, iar intensitatea este de natură episodică. Din păcate, pacienții sunt rareori capabili să izoleze dintele relevant.7 pentru a izola cauzele sensibilității, clinicienii se bazează de obicei pe expunerea dintelui suspectat la o explozie de aer sau lichid fierbinte sau rece pentru a provoca un răspuns. Utilizarea unui baraj de cauciuc pentru izolarea dintelui poate fi utilă în acest proces.
teoria hidrodinamică
teoria hidrodinamică este cea mai comună cauză a hipersensibilității dentinale. Kramer8 și Brännström9 confirmat și extins pe această teorie care stabilește o relație între presiunea aplicată, aer explozii și stimuli chimici pentru dentina lichid schimburi care au loc ca răspuns la acești stimuli.7 În original de cercetare, Brännström sol prin email în midcoronal dentina de premolari la copiii ai căror dinți au fost de gând să fie extrași în scop ortodontic. Tubulii dentinici transversali ai copiilor au fost expuși la salivă timp de o săptămână, ceea ce a dus la creșterea sensibilității. Inițial, un strat de frotiu acoperea acești dinți, dar, până la sfârșitul săptămânii, dispăruse, făcând astfel dentina din ce în ce mai hiperconductoare.9 permeabilitatea dentinei variază și poate scădea rapid.10
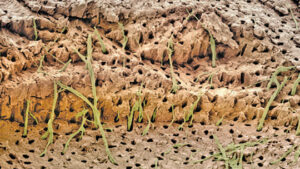
dovezile care susțin teoria hidrodinamică se bazează pe studii in vivo la subiecți umani și animale. Distribuția nervilor în tubulii dentinali variază, aproximativ 40% apărând peste coarnele pulpei și un procent mai mic situat în dentina cervicală. Se pare că tubulii dentinali deschiși sunt necesari pentru ca dentina expusă să devină sensibilă (Figura 1, pagina 18); de fapt, sensibilitatea unui pacient va crește proporțional cu numărul de tubuli mari, deschiși prezenți. Tubulii deschisi demonstrează o conductanță hidraulică ridicată; dimpotrivă, fluxul de fluid scade dacă tubulii sunt blocați. Aceasta oferă un mijloc pentru diferite opțiuni de tratament. Magloire și colab. 11 afirmă că stimulii externi au ca rezultat mișcarea lichidului dentinal și că odontoblastele și/sau reacția complexului nervos pot fi un sistem mecanosenzorial distinctiv — oferind un nou rol odontoblastelor ca celule senzoriale. Transferul de informații între odontoblaste și axoni poate fi rezultatul mediatorilor în spațiul dintre odontoblaste și axoni, după cum reiese din receptorii nocioceptivi-transductori și fibrele aferente trigeminale și exprimarea efectorilor reputați de către odontoblaste (Figura 2).11
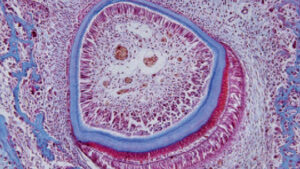
care stabilesc dentina (strat albastru subțire), care constituie cea mai mare parte a dintelui. Smalțul (stratul albastru mai gros) este format din ameloblaste, un strat de celule alungite în jurul exteriorului smalțului.
cauze posibile
boala parodontală, recesiunea gingivală, dinții crăpați, eroziunea, abraziunea, abfracția și fractura dinților pot provoca hipersensibilitate. Toate aceste condiții au ca rezultat dentina expusă, care creează un mediu în care stimulii provoacă mișcarea fluidului tubular dentinal care activează fibrele nervoase, provocând durere. Dentina expusă poate rezulta din îndepărtarea cimentului cervical în timpul scalării și rindeluirii rădăcinilor, finisarea și lustruirea restaurărilor sau spălarea extremă a dinților — în special după ingestia de alimente sau băuturi acide. Regurgitarea de către pacienții cu bulimie produce expunere acidă, iar periajul ulterior poate duce la pierderea structurii dinților.1 durerea poate fi localizată sau de natură generală și poate afecta o varietate de suprafețe dentare, fie împreună, fie individual.12
după cum sa menționat, pacienții cu boală parodontală sunt supuși hipersensibilității dentinale.13 studii arată că incidența hipersensibilității crește la o săptămână după intervenția chirurgicală parodontală și se remite cu opt săptămâni.14,15 pacienți mai tineri demonstrează o sensibilitate mai mare comparativ cu adulții mai în vârstă, la care sensibilitatea durează mai mult pentru a se rezolva. Scalarea și rindeluirea rădăcinilor pot provoca, de asemenea, sensibilitate timp de câteva zile după tratament.
recesiunea gingivală are ca rezultat expunerea suprafețelor rădăcinii și posibila sensibilitate. Osul bucal asigură cea mai mare parte a alimentării cu sânge a gingiei bucale, iar orice pierdere a osului bucal va duce la o scădere a gingiei.14 oasele subțiri sau fenestrate, anatomia dinților, poziția dinților sau mișcarea ortodontică pot duce la recesiune. Spălarea excesivă a dinților cu pastă de dinți poate provoca, de asemenea, recesiune.15 semnele și simptomele dinților crăpați pot varia în funcție de severitate. De obicei, pacienții vor suferi dureri acute cu masticare, dar, la îndepărtarea stimulului, durerea dispare. Dacă durerea se extinde la pulpa sau ligamentul parodontal, aceasta va persista.16
eroziunea este definită ca o pierdere a smalțului prin dizolvarea chimică de către acizi care nu sunt de origine bacteriană. Există trei tipuri de eroziune: extrinsecă (de exemplu, dietă, stil de viață sau mediu), intrinsecă (de exemplu, acid gastric) și idiopatică.17 acidul sindicalizat se difuzează în zonele interprismatice ale smalțului și dizolvă mineralul în zona subterană.18 în stadiul inițial, suprafața dintelui este plictisitoare din cauza demineralizării, dar dintele nu este hipersensibil deoarece dentina cu tubuli deschisi nu este expusă. Compozitul poate fi utilizat pentru a sigila smalțul pentru a restabili conturul normal și pentru a preveni expunerea la dentină.19 restaurarea dintelui va îmbunătăți igiena orală și va reduce posibila implicare a pulpei, abraziunea periuței de dinți/ a dinților și eroziunea acidă.20
abraziunea este pierderea structurii dintelui prin forțe mecanice de la un element străin și poate provoca sensibilitate.21 uzura este contactul dinte-dinte, care rezultă din funcția ocluzală sau parafuncția — cum ar fi bruxismul — și poate provoca pierderea structurii dintelui pe suprafețele ocluzale și marginile incizale.22
rolul abfracției în etiologia hipersensibilității dentinale este controversat. Abfracția poate apărea atunci când încărcarea disproporționată ciclică, nonaxială a dinților duce la flexia vârfului și concentrarea tensiunilor în regiunea cervicală sensibilă a dinților. Aceste leziuni cervicale, cauzate de solicitări ocluzale, duc la slăbirea structurii dintelui cervical și pot determina smalt, Cement sau dentină să se desprindă de aspectul cervical.23 Lee și Eakle24 au descris mai întâi leziunile care pot rezulta din solicitări de tracțiune. Ei au stabilit că o leziune de abfracție este adesea localizată la sau în apropierea punctului de sprijin în zona cu cea mai mare concentrație de stres de tracțiune; este de obicei în formă de pană și prezintă o dimensiune proporțională cu gradul și incidența forței de tracțiune aplicate.
alții, totuși, susțin că există dovezi limitate care susțin abfracția ca o cauză principală a ceea ce acum sunt denumite leziuni cervicale necarioase. Procesele necarioase care duc la pierderea țesutului dur în zona cervicală par a fi multifactoriale și pot include abraziune, provocări acide și, eventual, abfracție.23 în timp ce dovezile disponibile sugerează că aceste leziuni se pot dezvolta din forțe, inclusiv forțe ocluzale, care acționează singure sau în combinație,23 de studii suplimentare sunt justificate pentru a determina rolul exact al abfracției în leziunile necarioase și orice sensibilitate asociată.
în plus față de aceste surse, albirea dinților cauzează adesea hipersensibilitate dentinală. Utilizarea peroxidului de hidrogen sau a peroxidului de carbamidă se poate infiltra prin smalț și dentină în pulpă. Peroxidaza de glutation și catalaza din pulpă nu au suficient timp pentru a inactiva peroxidul de hidrogen, ceea ce poate provoca sensibilitate. De asemenea, trebuie remarcat faptul că toate gelurile de albire sunt hipertonice și trag osmotic apă din pulpă prin dentină și smalț la agentul de albire. Acest lucru poate stimula nervii intradentari.25
Opțiuni de tratament
clinicienii pot recomanda o varietate de tratamente pentru uz casnic sau în aplicații de birou (vezi Tabelul 1 pentru o diagramă a opțiunilor de tratament).26 mecanismul de acțiune este de obicei desensibilizarea nervilor, precipitarea proteinelor, conectarea tubulilor dentinali, etanșarea dentinei sau ablarea dentinei cu un laser. Cele mai frecvent utilizate terapii includ agenți antiinflamatori, precipitanți proteici, agenți de ocluzie a tubulilor și agenți de etanșare a tubulilor. Abordarea cea mai conservatoare ar trebui implementată inițial, cu tratamente mai agresive sugerate dacă nu se obține o ușurare.27
tabelul 1. Strategii pentru tratamentul hipersensibilității Dentinale26 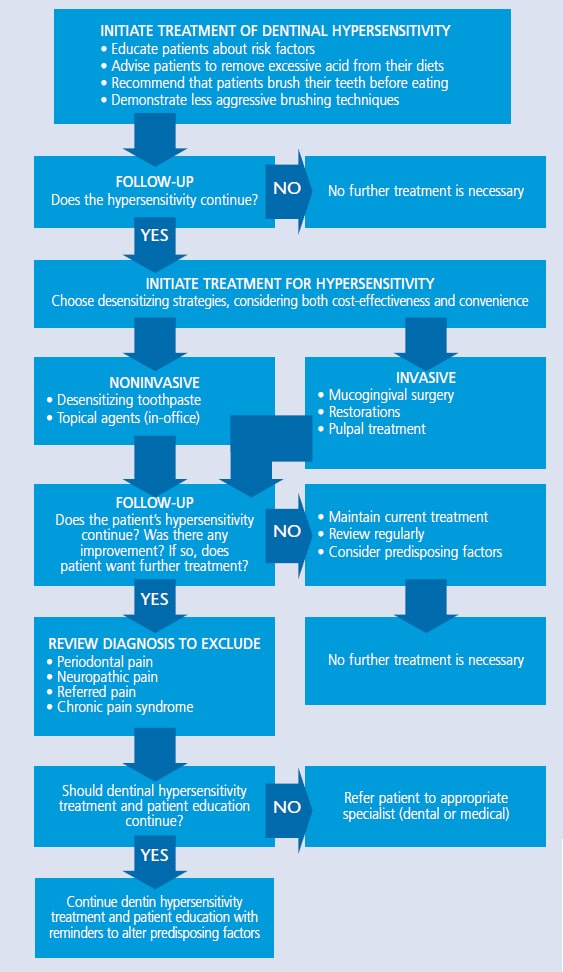 ca primă linie de apărare împotriva sensibilității, clinicienii ar putea dori să recomande o pastă de dinți cu săruri de potasiu (de exemplu, azotat de potasiu, clorură de potasiu sau citrat de potasiu), săruri de stronțiu (de exemplu, clorură de stronțiu sau acetat de stronțiu) sau fluorură. Ionii de potasiu difuzează de-a lungul tubulilor dentinali, care blochează acțiunea nervoasă și plictisesc durerea asociată cu hipersensibilitatea. Dentifricele cu sare de potasiu sunt eficiente, dar pot necesita două săptămâni de utilizare consecventă pentru ca pacienții să simtă efectele.28 prin comparație, metoda de acțiune Găsită în dentifricele de sare de stronțiu sau fluorură este ocluzia tubulară. Fluorul sub diferite forme este o strategie eficientă pentru ameliorarea sensibilității la domiciliu. Fluorura de sodiu, fluorura stanoasă și monofluorofsofatul de sodiu blochează toate tubulii dentinali, reducând sensibilitatea. Prescriptie fluorura dentifrices și aplicarea tava poate fi, de asemenea, de ajutor.29tehnologiile cu fosfat de calciu sunt o altă opțiune pentru tratarea hipersensibilității. Fosfatul de calciu amorf face ca ionii de calciu și fosfat să fie disponibili în salivă pentru a accelera remineralizarea și poate ajuta la minimizarea sensibilității induse de albire. Este disponibil în gel și produse de albire.29 În plus, produsele care conțin fosfopeptidă de cazeină-fosfat de calciu amorf (CPP-ACP) pot fi utilizate pentru a bloca parțial tubulii dentinali. Deși pretratarea cu un agent de desensibilizare va interfera uneori cu legarea restaurativă, un studiu realizat de Borges și colab.30 a constatat că pasta cu CPP-ACP nu a afectat negativ rezistența legăturii și, în unele cazuri, a îmbunătățit-o. Fosfosilicatul de sodiu de calciu poate ajuta, de asemenea, la infiltrarea și remineralizarea tubulilor. Silica din material funcționează ca o poziție de nucleație pentru precipitarea calciului și a fosfatului.31 fosfatul tricalcic (TCP) este cea mai recentă adăugare la familia tehnologiilor de fosfat de calciu. Oferind o eliberare lentă de calciu pe suprafața dinților, TCP este conceput pentru a stimula efectele remineralizante ale fluorului, care pot, de asemenea, să scadă sensibilitatea. Este disponibil într-o rețetă de pastă de dinți și lac de fluor.32
ca primă linie de apărare împotriva sensibilității, clinicienii ar putea dori să recomande o pastă de dinți cu săruri de potasiu (de exemplu, azotat de potasiu, clorură de potasiu sau citrat de potasiu), săruri de stronțiu (de exemplu, clorură de stronțiu sau acetat de stronțiu) sau fluorură. Ionii de potasiu difuzează de-a lungul tubulilor dentinali, care blochează acțiunea nervoasă și plictisesc durerea asociată cu hipersensibilitatea. Dentifricele cu sare de potasiu sunt eficiente, dar pot necesita două săptămâni de utilizare consecventă pentru ca pacienții să simtă efectele.28 prin comparație, metoda de acțiune Găsită în dentifricele de sare de stronțiu sau fluorură este ocluzia tubulară. Fluorul sub diferite forme este o strategie eficientă pentru ameliorarea sensibilității la domiciliu. Fluorura de sodiu, fluorura stanoasă și monofluorofsofatul de sodiu blochează toate tubulii dentinali, reducând sensibilitatea. Prescriptie fluorura dentifrices și aplicarea tava poate fi, de asemenea, de ajutor.29tehnologiile cu fosfat de calciu sunt o altă opțiune pentru tratarea hipersensibilității. Fosfatul de calciu amorf face ca ionii de calciu și fosfat să fie disponibili în salivă pentru a accelera remineralizarea și poate ajuta la minimizarea sensibilității induse de albire. Este disponibil în gel și produse de albire.29 În plus, produsele care conțin fosfopeptidă de cazeină-fosfat de calciu amorf (CPP-ACP) pot fi utilizate pentru a bloca parțial tubulii dentinali. Deși pretratarea cu un agent de desensibilizare va interfera uneori cu legarea restaurativă, un studiu realizat de Borges și colab.30 a constatat că pasta cu CPP-ACP nu a afectat negativ rezistența legăturii și, în unele cazuri, a îmbunătățit-o. Fosfosilicatul de sodiu de calciu poate ajuta, de asemenea, la infiltrarea și remineralizarea tubulilor. Silica din material funcționează ca o poziție de nucleație pentru precipitarea calciului și a fosfatului.31 fosfatul tricalcic (TCP) este cea mai recentă adăugare la familia tehnologiilor de fosfat de calciu. Oferind o eliberare lentă de calciu pe suprafața dinților, TCP este conceput pentru a stimula efectele remineralizante ale fluorului, care pot, de asemenea, să scadă sensibilitatea. Este disponibil într-o rețetă de pastă de dinți și lac de fluor.32
aplicație în birou
terapiile Simple în birou pot fi utile în abordarea sensibilității. Clinicienii pot aplica o pastă de profilaxie desensibilizantă formulată cu 8% arginină și carbonat de calciu pentru a bloca tubulii cu dopuri de arginină, calciu, fosfat și carbonat. S-a demonstrat că suportă presiunea pulpară normală și provocările acide, minimizând cu succes fluxul fluidului tubular dentinal și, astfel, sensibilitatea,33 fără a afecta rezistența legăturii.34
Lacul fluorurat permite eliberarea lentă și continuă a fluorurii. Lacurile oferă un vehicul natural pe bază de rășină pentru Fluor. Fluorura de calciu este depozitată pe suprafața dinților, ducând la formarea fluorapatitei. Adăugarea oxalatului de potasiu determină formarea oxalatului de calciu rezistent la acid după reacția cu calciul dentinei.35 Lacul cu contact extins este un lac fluorurat fotocurizat care poate fi utilizat pentru a reduce hipersensibilitatea dentinală. Se compune dintr-un ionomer de sticlă modificat cu rășină care încorporează glicerofosfat cu eliberare de fluor. De asemenea, încurajează formarea etichetelor de rășină, permițând ocluzia instantanee și pe termen lung a tubulilor. Un alt produs de lac combină 5% glutaraldehidă și 35% hidroxietilmetacrilat. Acționează ca un fixativ biologic și creează o coagulare a proteinelor plasmatice în tubuli, blocând deschiderile. Capabil să reducă sensibilitatea timp de cel puțin trei luni,,sup>36 se poate infiltra dentina gravată cu acid și umedă. Aceste lacuri sunt compatibile cu adezivi, cimenturi și materiale de restaurare și de bază.37
Lacul de clorhexidină formează o barieră mecanică după uscare, ceea ce reduce sensibilitatea, asigurând în același timp o acțiune antiplacă și antibacteriană.38
oxalații s-au dovedit, de asemenea, că diminuează permeabilitatea dentinală și blochează tubulii.39 oxalatul reacționează cu ionii de calciu din dentină pentru a forma cristale de oxalat de calciu în tubuli și la suprafață. Efectul este redus în timp, totuși, deoarece cristalele sunt îndepărtate prin periere și acizi dietetici. Gravarea îmbunătățește infiltrarea cristalelor de oxalat de calciu în tubuli.39
clinicienii pot utiliza, de asemenea, Un desensibilizator vindecat ușor, care reduce sensibilitatea prin reacția monomerului cu calciu în formarea dinților și a etichetelor de rășină, rezultând ocluzia tubulilor. O lumină de întărire polimerizează ulterior stratul de rășină. Poate fi utilizat pentru etanșarea imediată a dentinei dinților pregătiți.
Opțiuni de tratament invaziv
atunci când terapiile mai puțin invazive nu sunt eficiente, legarea, altoirea și tratamentul cu laser pot oferi ameliorarea hipersensibilității dentinale. Agenții de lipire pot fi utilizați pentru desensibilizarea și legarea simultană.40 în funcție de produsul utilizat, un potențial dezavantaj al acestei abordări este necesitatea acidului fosforic înainte de introducerea agentului de legătură, care poate necesita utilizarea anesteziei.
o alternativă este utilizarea unui adeziv auto-gravat. Un alt agent de lipire disponibil blochează tubulii dentinali și conține triclosan pentru a minimiza formarea plăcii.41 Un mod alternativ de desensibilizare este acoperirea suprafețelor radiculare expuse cu altoire. Acest lucru trebuie luat în considerare înainte de tehnicile de legare, totuși, deoarece restaurările legate ar putea împiedica o grefă reușită.42 utilizarea Nd:Laserele YAG asigură absorbția energiei termice pe dentină, ceea ce poate duce la ocluzia sau îngustarea tubulilor dentinali.39,43
rezumat
hipersensibilitatea Dentinală este cauzată de dentina expusă în care stimulii declanșează mișcarea fluidului tubular dentinal care activează fibrele nervoase pentru a provoca durere. Relația dintre precipitațiile de suprafață și intratubulare și moderarea sensibilității nu este simplă. Nu cantitatea de precipitat, ci, mai degrabă, calitatea, densitatea, porozitatea, adâncimea de penetrare și rezistența atașamentului la dentină afectează rezultatele.40 în cele din urmă, eficacitatea tratamentului este determinată de durata diminuării sau eliminării.
deciziile de tratament trebuie să se bazeze pe severitatea și etiologia hipersensibilității dentinale. Unele tratamente la birou aduc o ușurare imediată care poate fi urmată cu o varietate de remedii la domiciliu. O combinație de tehnici poate fi justificată pentru a oferi ajutor pe termen lung.
key TAKEAWAYS
-
- teoria hidrodinamică este cea mai comună cauză a hipersensibilității dentinale.
- tubulii dentinali deschisi demonstrează o conductanță hidraulică ridicată, contribuind astfel la sensibilitate; dimpotrivă, fluxul de fluid scade dacă tubulii sunt blocați. Aceasta oferă un mijloc pentru diferite abordări ale tratamentului.
- prevalența acestei afecțiuni este ușor mai mare în rândul femeilor,3 cu canini și premolari ai ambelor arcuri cel mai frecvent implicați.4
- de obicei, durerea de hipersensibilitate este localizată și de scurtă durată; aceasta diferă de durerea pulpară, care este prelungită, plictisitoare, dureroasă, slab localizată și durează mai mult decât stimulul aplicat.
- utilizarea unui baraj de cauciuc poate fi utilă atunci când încercați să izolați dintele — sau dinții — supuși hipersensibilității.
- clinicienii pot recomanda o varietate de terapii pentru utilizarea la domiciliu sau în birou. Cele mai frecvente tratamente includ agenți antiinflamatori, precipitanți proteici, agenți de ocluzie a tubulilor și agenți de etanșare a tubulilor.
- deciziile de tratament trebuie să se bazeze pe severitatea și etiologia sensibilității, iar o combinație de tehnici poate fi justificată pentru a oferi o ușurare eficientă.
-
-
- Addy M. hipersensibilitate dentină: noi perspective asupra unei probleme vechi. Int Dent J. 2002; 52: 367-375.
- Addy M. etiologia și implicațiile clinice ale hipersensibilității dentinei. Dent Clin Nord Am. 1990;34:503–514.
- Flyn J, Galloway R, Orchardson R. incidența dinților hipersensibili în vestul Scoției. J Dent. 1985;13:230–236.
- Addy M, Mostafa P, Newcombe RG. Hipersensibilitate dentină: distribuția recesiunii, sensibilității și plăcii. J Dent. 1987;15:242–248.
- Dababneh RH, Khouri AT, Addy M. hipersensibilitate dentină-o enigmă? O revizuire a terminologiei, mecanismelor, etiologiei și managementului. Br Dent J. 1999; 187: 606-611.
- Holland GR, Narhi mn, Addy M, Gangarosa l, Orchardson R. linii directoare pentru proiectarea și desfășurarea studiilor clinice privind hipersensibilitatea dentinei. J Clin Periodontol. 1997;24:803–813.
- li Y. inovații pentru combaterea hipersensibilității dentinei: stadiul actual al tehnicii. Compend Contin Educ Dent. 2012; 33(supliment):10-16.
- Kramer IRH. Relația dintre sensibilitatea dentinei și mișcările din conținutul tubulilor dentinali. Br Dent J. 1955; 98: 391-392.
- Brännström M. suscitare a durerii umane în dentină și pulpă de stimuli chimici. Arch Oral Biol. 1962;7:59–62.
- Pashley DH. Complexul Dentin-predentin și permeabilitatea acestuia: prezentare fiziologică. J Dent Res. 1985; 64 (Supliment): 613-620.
- Magloire H, Maurin JC, Couble ML și colab. Revizuire de actualitate. Dureri dentare și odontoblaste: fapte și ipoteze. J Orofac Durere. 2010;24:335–349.
- Camilotti V, Zilly J, Nassar CA, Nassar PO. Tratamente de desensibilizare pentru hipersensibilitatea dentinei: un studiu clinic randomizat, cu gură divizată. Braz Oral Res. 2012; 26: 263-268.
- Chabanski MB, Gillam DG, Bulman JS, Newman HN. Prevalența sensibilității dentinei cervicale la o populație de pacienți se referă la un departament specializat de Parodontologie. J Clin Periodontol. 1996;23:989–992.
- Uchida A, Wakano Y, Fukuyama O, Miki T, Iwayama Y, Okada H. Evaluarea clinică controlată a unei substanțe dentare de clorură de stronțiu 10% în tratamentul hipersensibilității dentinei după intervenția chirurgicală parodontală. J Periodontol. 1980;51:578–581.
- Absi EG, Addy M, Adams D. hipersensibilitate la dentină — efectul spălării dinților și al compușilor dietetici asupra dentinei in vitro: un studiu SEM. J Reabilitare Orală. 1992;19:101–110.
- Kahler W. Enigma dinților crăpați: terminologie, clasificare, diagnostic și management. Sunt J. Dent. 2008;21:275–282.
- Bartlett DW. Rolul eroziunii în uzura dinților: etiologie, prevenire și management. Int Dent J. 2005; 55 (Supliment): 277-284.
- Zero DT, Lussi A. eroziunea — factori chimici și biologici de importanță pentru medicul stomatolog. Int Dent J. 2005; 55: 285-290.
- Lambrechts P, Van Meerbeek B, Perdig Inktico J, Gladys S, Braem M, Vanherle G. terapia restaurativă pentru leziunea erozivă. Eur J Oral Sci. 1996;104:229–240.
- Grippo JO. Leziuni cervicale necarioase: decizia de a ignora sau de a restabili. J Esthet Dent. 1992;4:55–64.
- Abrahamsen TC. Dentiția uzată – modele patognomonice de abraziune și eroziune. Int Dent J. 2005; 55 (Suppl):268–276.
- McIntyre F. restabilirea esteticii și ghidării anterioare în dinții anteriori uzați. O abordare multidisciplinară conservatoare. Sunt Dent Conf. 2000;131:1279–1283.
- Michael JA, Townsend GC, Greenwood LF, Kaidonis JA. Abfraction: separarea faptului de ficțiune. Aust Dent J. 2009; 54: 2-8.
- Lee WC, Eakle WS. Rolul posibil al stresului de tracțiune în etiologia leziunilor erozive cervicale ale dinților. J Prothet Dent. 1984;52:374–380.
- Swift ej Jr.sensibilitatea și albirea dinților. Compend Conținut Dent Educ Dent.2005; 26(supliment): 4-10.
- Consiliul Consultativ Canadian privind hipersensibilitatea dentinei. Recomandări bazate pe consens pentru diagnosticul și gestionarea hipersensibilității dentinei. J Poate Dent Assoc. 2003;69:221–226.
- Al-Saud LM, Al-Nahedh HN. Efectul ocluziv al laserului Nd: YAG și al diferiților agenți de desensibilizare a dentinei asupra tubulilor dentinali umani in vitro: o investigație de microscopie electronică de scanare. Oper Dent. 2012;37:340–355.
- Poulsen S, Errboe M, Hovgaard O, Worthington HW. Pasta de dinți cu nitrat de potasiu pentru hipersensibilitate la dentină. Cochrane baza de date Syst Rev. 2001; 2: CD001476.
- Orchardson R, Gillam DG. Gestionarea hipersensibilității dentinei. J Dent Conf. 2006;137:990–998.
- Borges BC, Souza-Junior EJ, da Costa Gde F, și colab. Efectul pretratării dentinei cu o pastă de fosfat de calciu fosfopeptidamorf de cazeină (CPP-ACP) asupra rezistenței legăturii dentinei în cavitățile tridimensionale. Acta Odontol Scand. 2013;71:271–277.
- Forsback AP, Areva S, Salonen JI. Mineralizarea dentinei indusă prin tratament cu sticlă bioactivă s53p4 in vitro. Acta Odontol Scand. 2004;62:14–20.
- Karlinsey RL, Mackey AC. Pregătirea în stare solidă și aplicarea dentară a unui fosfat de calciu modificat organic. J Mater Sci. 2009;44:346–349.
- Panagakos F, Schiff T, Guignon A. hipersensibilitate la dentină: tratament eficient cu o pastă desensibilizantă în birou care conține 8% arginină și carbonat de calciu. Sunt J. Dent. 2009; 22(Suppl):3A–7A.
- Garcia Elqua-Godoy a, Garcia Elqua-Godoy F. efectul unei paste desensibilizante de 8,0% arginină și carbonat de calciu în birou asupra rezistenței legăturii de forfecare a compozitelor la smalțul dentar uman. Sunt J. Dent. 2010;23:324–326.
- Camilotti V, Zilly J, Busato Dop M, Nassar CA, Nassar PO. Tratamente de desensibilizare pentru hipersensibilitatea dentinei: un studiu clinic randomizat, cu gură divizată. Braz Oral Res. 2012; 26: 263-268.
- Sethna GD, Prabhulji MLV, Karthikeyan BV. Compararea a două forme diferite de lacuri în tratamentul hipersensibilității dentinei: un studiu clinic randomizat orb. Sănătate Orală Prev Dent. 2011;9:143–150.
- Dijkman GE, Jongebloed WL, de Vries J, Ogaard B, Arends J. închiderea tubulilor dentinali prin tratamentul cu glutaraldehidă, un studiu de microscopie electronică de scanare. Scand J Dent Res. 1994; 102: 144-150.
- sk Untld-Larsson K, Sollenius O, Petersson LG, Twetman S. efectul aplicațiilor topice ale unei noi formule de lac clorhexidină-timol asupra streptococilor mutani și dezvoltarea cariilor în fisurile ocluzale ale molarilor permanenți. J Clin Dent. 2009;20:223–226.
- Lan WH, Lee BS, Liu HC, Lin CP. Studiul morfologic al utilizării laserului Nd: YAG în tratamentul hipersensibilității dentinale. J Endod. 2004;30:131–134.
- Ide M, Morel AD, Wilson RF, Ashley FP. Rolul unui agent de lipire a dentinei în reducerea sensibilității dentinei cervicale. J Clin Periodontol. 1998;25:286–290.
- Yu X, Liang B, Jin X, Fu B, Hannig M. studiu comparativ in vivo privind eficacitatea desensibilizantă a desensibilizatorilor de dentină și a adezivilor de auto-gravare cu o singură sticlă. Oper Dent. 2010;35:279–286.
- Douglas de Oliveira DW, Marques DP, Aguiar-Cantu Otrivtria IC, Flecha OD, Gon Univalves PF. Efectul acoperirii defectelor chirurgicale asupra hipersensibilității dentinei cervicale și a calității vieții. J Periodontol. 2013;84:768–775.
- Orhan K, Aksoy U, Can-Karabulut DC, Kalender A. Terapia cu laser la nivel scăzut a hipersensibilității dentinei: un studiu clinic pe termen scurt. Lasere Med Sci. 2011;26:591–598.
-