tratamentul cu vitamina E pentru pacienții cu steatohepatită nealcoolică
Jhonathan Ferney V Okticlez M. (1), Gustavo Amador Crespo H. (1), Juan Carlos Restrepo G. MD. Esp, MSc, PhD. (2)
(1) Student la medicină la Facultatea de Medicină de la Universidad De Antioquia din Medell, Columbia.
(2) profesor asociat la Departamentul de Medicină Internă și grupul de Gastrohepatologie de la Universidad De Antioquia și hepatolog la Spitalul Pablo Tob Uribe din Medell, Columbia. [email protected]
primit: 12-02-14 acceptat: 05-11-14
rezumat
steatohepatita nealcoolică (NASH) se caracterizează histologic prin balonarea hepatocitelor, inflamația lobulară și steatoza. Dacă se suspectează acest diagnostic, este important să se excludă alte cauze ale afectării hepatice, în special consumul excesiv de alcool. Cu toate acestea, până în prezent, o biopsie este singura metodă disponibilă pentru confirmarea diagnosticului. Vitamina E trebuie considerată o terapie de primă linie pentru tratamentul acestei boli, deoarece mai multe studii clinice au arătat că o doză de 800 UI/zi îmbunătățește histologia adulților non-diabetici care suferă de NASH chiar și atunci când nu există un impact semnificativ asupra fibrozei. Aceste rezultate au fost confirmate de biopsii. În ciuda beneficiilor dovedite ale utilizării acestui medicament, este important să fim conștienți de faptul că utilizarea acestuia nu poate înlocui modificările dietei și exercițiilor fizice, ci mai degrabă ar trebui văzută ca o completare a acestor măsuri.
cuvinte cheie
steatohepatită nealcoolică, vitamina E, stres oxidativ.
introducere
NASH se caracterizează histologic prin balonarea hepatocitelor, inflamația lobulară și steatoza (1, 2). În prezent, NASH poate fi diagnosticat doar printr-o biopsie hepatică, care este standardul de aur pentru diagnostic. De asemenea, oferă informații privind prezența și gradul de inflamație, necroză și fibroză, care sunt toate importante pentru stabilirea prognosticului pacientului (2-5). Diferențele dintre NASH și steatohepatita alcoolică sunt microscopice mici, ceea ce face dificilă diferențierea histologică între ele. Din acest motiv, este important să obțineți informații de la pacient despre obiceiurile sale de băut (4).
NASH face parte dintr-o entitate mult mai largă numită NAFLD (boală hepatică grasă nealcoolică) care include stadiile incipiente ale steatozei hepatice: steatoza fără inflamație și steatoza cu inflamație ușoară. În cele din urmă, NAFLD se dezvoltă în starea inflamatorie caracteristică a NASH care progresează spre fibroză și, în final, ciroză (1, 2, 5). Nu este încă complet clar că indivizii progresează de la steatoză simplă la starea inflamatorie. Interacțiunile dintre susceptibilitatea genetică, tulburările metabolice și stresul oxidativ sunt cei mai importanți factori (6, 7).
NAFLD este cea mai răspândită boală hepatică la nivel mondial (2, 4, 6). Prevalența NAFLD este estimată a fi de la 20% la 30%, iar prevalența NASH este considerată a fi de la 2% la 3% în populația generală a lumii occidentale (8).
datorită calităților sale antioxidante, vitamina E a fost recomandată în liniile directoare americane actuale pentru tratarea NASH. „Vitamina E (tocoferol-tocoferol) administrată în doză zilnică de 800 UI / zi îmbunătățește histologia hepatică la adulții non-diabetici cu NASH dovedit prin biopsie” acest lucru nu elimină importanța intervenției în stilul de viață și dieta pacientului ca parte tratament de bază pentru pacienții cu NASH (9, 10). În acest articol vom examina fiziopatologia NASH cu accent pe rolul vitaminei E în tratamentul pacienților cu această boală.
Fiziopatologie
în timp ce patogeneza NASH nu este încă complet clară, cea mai bine acceptată ipoteză propusă până în prezent pentru a explica evenimentele care au dus la steatoză și ulterior la steatohepatită este teoria „cu două lovituri”. Prima lovitură la debutul acestei boli este supraîncărcarea grăsimilor (11, 12). Un stil de viață sedentar, factorii genetici și aportul crescut de calorii îi fac pe indivizi mai sensibili la dezvoltarea rezistenței la insulină și a hiperinsulinemiei, ceea ce duce la o creștere a sintezei lipidelor hepatice și la eliberarea acizilor grași liberi din țesutul adipos. Dacă ficatul este menținut în această stare, acesta devine incapabil să metabolizeze toți acizii grași pe care îi produce și care sunt eliminați din circulație. Această afecțiune duce în cele din urmă la a doua lovitură, care este steatoza hepatică și stresul oxidativ (4, 5, 13).
stresul oxidativ este un dezechilibru care favorizează pro-oxidanții față de antioxidanți (3). În timpul steatozei hepatice, hepatocitele intră într-o stare hipermetabolică care duce la creșterea producției de radicali liberi în organele celulare (13). Creșterea cantităților de specii reactive de oxigen (ROS) în hepatocite duce la peroxidarea lipidelor, care este o reacție care asigură o aprovizionare continuă de radicali liberi suplimentari cu efecte potențial devastatoare (14, 15).
un antioxidant este vitamina E (tocoferol), care reacționează cu peroxizi lipidici pentru a le reduce față de acizi grași. Ele formează tocoferoxilul radical relativ stabil care persistă suficient de mult pentru a trece înapoi la tocoferol printr-o reacție cu vitamina C pe suprafața celulei (12). Datorită acestei caracteristici, vitamina E a fost luată în considerare pentru utilizare ca tratament pentru pacienții cu NASH (13, 16).
manifestări și diagnostic
NAFLD este un sindrom comun care variază de la steatoză simplă la steatohepatită (NASH) cu fibroză și ciroză ulterioară (5). Deși la diagnostic majoritatea pacienților sunt asimptomatici, unii pacienți, în special copiii, se pot plânge de oboseală și disconfort. Disconfortul în cadranul superior superior al abdomenului, suspiciunea datorată nivelurilor crescute de aminotransferaze și o ecografie abdominală cu o boală hepatică strălucitoare sunt toate semnele acestei boli. Obezitatea, diabetul și dislipidemia ar trebui, de asemenea, luate în considerare în timpul evaluării condițiilor care ar putea fi asociate cu NAFLD și NASH (5, 17).
în timpul evaluării diagnostice ar trebui excluse alte cauze comune ale bolii hepatice, dar în cele din urmă o biopsie hepatică este singura metodă disponibilă pentru confirmarea diagnosticului. De asemenea, este important pentru definirea prognosticului pacientului (Tabelul 1) (3, 4). În ciuda valorii sale clinice mari, o biopsie este costisitoare și duce la o ușoară creștere a morbidității și, în rare ocazii, duce la mortalitate. Acest instrument trebuie luat în considerare numai pentru pacienții pentru care se suspectează prezența steatozei hepatice nealcoolice care prezintă un risc crescut de steatohepatită și fibroză avansată (obezitate, diabet zaharat de tip II, dislipidemie și sindrom metabolic) și în cazurile de diagnostic incert (3, 9).

rolul vitaminei E în tratamentul steatohepatitei nealcoolice
în prezent nu există un tratament eficient pentru NASH. Cu toate acestea, având în vedere rolul important al vitaminei E ca factor antioxidant, au existat mai multe studii clinice pentru a demonstra beneficiile acesteia în evoluția clinică și histopatologică a acestei boli (Tabelul 2).
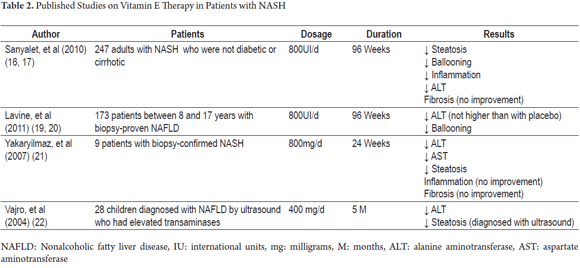
printre acestea se numără studiul PIVENS (pioglitazonă versus vitamina E versus placebo pentru tratamentul pacienților non-diabetici cu steatohepatită nealcoolică). Acesta a fost un studiu multicentric, dublu-orb, controlat cu placebo, în care îmbunătățirea histologică a fost evaluată la 247 de pacienți non-diabetici și non-cirotici care au avut NASH. Pacienții au fost repartizați aleatoriu pentru a primi o doză zilnică de pioglitazonă (80 pacienți), vitamina E (84 pacienți) sau un placebo (83 pacienți) timp de nouăzeci și șase de săptămâni (18). Dozele zilnice au fost de 30 mg pentru pioglitazonă și 800 U pentru vitamina E. Acest studiu a constatat că 43% dintre pacienții care au primit vitamina E (P = 0,001) s-au îmbunătățit față de 34% dintre cei care au primit pioglitazonă (P = 0,04) și 19% dintre cei care au primit placebo. Diferența dintre ratele de ameliorare între pioglitazonă și placebo nu a fost semnificativă statistic, în timp ce diferența dintre ratele de ameliorare ale vitaminei E și placebo a fost semnificativă. Cu toate acestea, ambele medicamente au fost asociate cu îmbunătățirea nivelurilor de aminotransferază, reducerea steatozei și a inflamației lobulare, dar niciuna nu a dus la o îmbunătățire a fibrozei. Același studiu a arătat că, după tratamentul cu vitamina E a fost suspendat nivelurile de aminotransferază a crescut indicând faptul că administrarea nedeterminată a tratamentului poate fi necesară. În plus, nu s-au găsit diferențe semnificative între efectele adverse ale vitaminei E și efectele adverse ale placebo (19).
o reevaluare a studiului PIVENS de către Hoofnagle și colab. concentrat pe răspunsul ALT seric la pacienții care au primit vitamina E sau placebo și pe asocierea acestui răspuns cu modificările clinice, histologice inițiale și interacțiunile cu modificările greutății corporale. Ei au descoperit că modificările ALT au fost mai frecvente în rândul celor care au primit vitamina E (48%) decât la cei care au primit placebo (16%; p <0,001). Dintre grupul care a primit vitamina E, răspunsurile ALT au fost asociate cu scăderea activității bolii hepatice grase nealcoolice (NAFLD), dar nu a existat nicio îmbunătățire a fibrozei după terminarea tratamentului la 96 de săptămâni. Valorile ALT au crescut în grupul cu vitamina E după terminarea administrării, dar nu au crescut în grupul placebo după terminarea administrării. Ambele grupuri de tratament au avut niveluri de ALT aproape identice în săptămâna 120. Aceste rezultate sunt similare cu cele prezentate în cohorta completă a publicației principale A STUDIULUI PIVENS. Mai mult, rezultatele au arătat că pierderea în greutate (2 kg sau mai mult) este, de asemenea, asociată cu răspunsul ALT, cu îmbunătățirea NAFLD (<0,001) și îmbunătățirea fibrozei (p <0,02), dar vitamina E a avut efecte mai mari asupra NAFLD independent de modificările greutății corporale. În cele din urmă, trebuie remarcat faptul că efectele vitaminei E și pierderii în greutate asupra răspunsului ALT și histologiei sunt independente, ceea ce înseamnă că chiar și acei pacienți care pierd în greutate ar beneficia de terapia cu vitamina E (20).
studiul TONIC (tratamentul bolilor hepatice grase nealcoolice la copii) a fost un alt studiu multicentric, dublu-orb, controlat cu placebo. Acesta a inclus 173 de pacienți cu vârste cuprinse între opt și șaptesprezece ani. Pacienții au fost repartizați aleatoriu pentru a primi vitamina E (58 de pacienți), metformină (57 de pacienți) sau placebo (58 de pacienți) timp de 96 de săptămâni. Dozele au fost de 400 UI de două ori pe zi pentru vitamina E și 500 mg de două ori pe zi pentru metformină (21). Niciunul dintre medicamente nu a fost superior placebo-ului pentru obținerea fie a unor reduceri susținute de cel puțin 50% ale valorilor inițiale ale ALT, fie a unor niveluri susținute ale ALT de 40 U/L sau mai puțin. Măsurătorile au fost efectuate la fiecare 12 săptămâni din săptămâna 48 până în săptămâna 96. Acest studiu a constatat, de asemenea, că rezoluția NASH a fost semnificativ mai mare în grupul de pacienți tratați cu vitamina E decât în grupul placebo. Acest rezultat a fost atribuit scăderii semnificative a balonării hepatocelulare care a fost găsită la pacienții tratați cu vitamina E. Acest lucru este similar cu rezultatele PIVENS, chiar dacă studiul TONIC nu a analizat scăderea balonului hepatocelular ca rezultat primar din cauza diferențelor histopatologice dintre NALFD la pacienții pediatrici și adulți. Studiul TONIC nu a găsit nicio îmbunătățire a fibrozei (22).
anterior acestor două studii mari au existat alte studii mai mici care au avut rezultate cu diferențe majore în rezultatele primare evaluate. În plus față de populațiile mult mai mici, aceste studii au avut mai puțin timp de monitorizare, iar unele dintre ele nu au fost controlate cu grupuri placebo.
un studiu din 2007 realizat de Yakaryilmaz și colab. s-a analizat efectul vitaminei E asupra a nouă pacienți ale căror diagnostice de NASH au fost verificate prin biopsie. Studiul a evaluat efectul vitaminei E asupra receptorului Gamma activat de proliferatorul peroxizomului (PPARG) și asupra rezistenței la insulină. Pacienților li s-au administrat 800 mg de vitamina E zilnic timp de 24 de săptămâni. Înainte de începerea tratamentului, ficatul pacienților a fost evaluat biochimic și histologic. Aceste evaluări au fost repetate după terminarea tratamentului. La sfârșitul celor 24 de săptămâni, s-au găsit scăderi semnificative statistic ale AST, ALT și steatoză, dar nu s-au găsit modificări histologice în nivelul inflamației și fibrozei. Niciun pacient nu a prezentat reacții adverse la această doză de vitamina E (23).
Vajro și colab. (2004) a efectuat un studiu al unui grup de 28 de copii cu disfuncție hepatică legată de obezitate. Pacienții au fost împărțiți în două grupuri. Vârsta medie a grupului unu a fost de 9,88 (+/- 3,97) ani, iar a grupului doi a fost de 10,7 (+/- 3,45). Pacienții au fost evaluați pentru a determina dacă au existat efecte benefice ale tratamentului cu vitamina E asupra pierderii în greutate, a nivelurilor de transaminaze și a steatozei măsurate prin ultrasunete. Copiii incluși în acest studiu au avut hipertransaminazemie cronică (niveluri AST sau ALT de 1,5 ori peste valoarea normală pentru mai mult de 6 luni) și semne de steatoză la ultrasunete. Studiul a avut un design unic orb în care pacienții au fost randomizați într-unul din cele două grupuri: grupul 1 (Dieta placebo plus) și Grupul 2 (Dieta cu vitamina E+). Ulterior, Fiecare grup a fost subdivizat în funcție de respectarea tratamentului de către pacient. Grupul 1 a fost împărțit în subgrupul 1a pentru cei care au respectat dieta și subgrupul 1B pentru cei care nu s-au conformat. Grupul 2 a fost împărțit în subgrupul 2a pentru cei care au respectat terapia cu vitamina E și subgrupul 2B pentru cei care nu au respectat terapia cu vitamina E. Subgrupul 2A a fost împărțit în continuare în subgrupul 2A1 pentru cei care nu au respectat dieta și subgrupul 2A2 pentru cei care au respectat dieta. Studiul a constatat că doza de 400 mg/zi de vitamina E a produs scăderi semnificative ale valorilor ALT pentru pacienții din subgrupul 2a care au abordat normalizarea independent de orice modificare a greutății. Pe de altă parte, acei pacienți care au atins niveluri serice ridicate de vitamina E și, de asemenea, au pierdut în greutate au obținut normalizarea ALT și remiterea steatozei. Mai mult, o comparație între subgrupul 1a care a respectat doar dieta și subgrupul 2A1 care a respectat doar terapia cu vitamina E a constatat că ambele grupuri de pacienți au avut niveluri scăzute de ALT la două luni de monitorizare, dar că a existat o scădere mai mare a subgrupului 1a (a respectat doar dieta) decât în subgrupul 2A1 (a respectat doar vitamina E) la cinci luni de monitorizare. Toate semnele de steatoză au dispărut din imaginile cu ultrasunete din grupul subgrupului 2A2 care a pierdut în greutate în timpul tratamentului cu 400 mg de vitamina E. Aceste rezultate evidențiază importanța promovării alimentației sănătoase ca una dintre intervențiile majore de tratament pentru pacienții cu NASH, dar trebuie de asemenea remarcat faptul că mulți pacienți nu respectă regimurile alimentare care duc la eșecul intervenției. Acest lucru subliniază importanța utilizării antioxidanților, cum ar fi vitamina E, ca o bună terapie alternativă pentru acești pacienți (24).
un studiu pilot realizat de Kugelmas și colab. (2003) a evaluat efectele etapei 1 a dietei American Heart Association combinate cu exerciții aerobice crescute cu și fără administrarea zilnică de vitamina E pe profilurile citokinelor (TNF alfa, IL-8, IL -6) și nivelurile enzimelor hepatice la 16 pacienți cu vârsta cuprinsă între 18 și 65 de ani cu biopsie dovedită NASH. Acesta a fost un studiu cu un singur orb în care pacienții au fost repartizați aleatoriu pentru a primi 800 UI de vitamina E zilnic. Pacienții care nu au primit vitamina E au primit placebo. Testul a fost efectuat pe o perioadă de 12 săptămâni. Valorile citokinelor nu s-au diminuat semnificativ odată cu pierderea în greutate cu sau fără administrarea de vitamina E în timpul studiului. Modificările stilului de viață au fost asociate cu îmbunătățiri ale enzimelor hepatice și ale colesterolului plasmatic la pacienții cu NASH, în timp ce doza de vitamina E utilizată în acest studiu nu a arătat niciun beneficiu suplimentar. Acest rezultat se poate datora dimensiunii mici a eșantionului, timpului scurt de urmărire sau dozei de vitamina E utilizată (25, 26).
o revizuire publicată în noiembrie 2013 despre opțiunile disponibile în prezent pentru tratamentul pacienților cu NASH a recunoscut recomandarea actuală pentru utilizarea vitaminei E ca terapie de primă linie la pacienții cu NASH confirmată prin biopsie care nu sunt cirotici și care nu au diabet, dar a subliniat, de asemenea, faptul că această terapie a arătat doar un beneficiu semnificativ la mai puțin de jumătate dintre pacienți. Din acest motiv, Revizuirea a concluzionat că strategiile viitoare de tratament ar trebui să se bazeze pe căile de boală patogenă dacă se va dezvolta vreodată un tratament eficient pentru pacienții cu NASH (27).
Ji H-F și colab. a efectuat o meta-analiză pentru a evalua efectul vitaminei E asupra scăderii aminotransferazelor la pacienții cu NAFLD, NASH și hepatită cronică C (CHC). Cele patru studii pe care le-au analizat au inclus pacienți cu NASH care au primit suplimente de vitamina E. Studiile au inclus studiile TONIC și PIVENS. Ei au descoperit că vitamina E ar putea optimiza nivelurile de AST și ALT la acești pacienți. Cu toate acestea, trebuie remarcat faptul că această meta-analiză a fost limitată de incapacitatea de a exclude o incapacitate de a exclude efectele intervențiilor care implică modificări ale stilului de viață, exerciții fizice și utilizarea altor antioxidanți și de incapacitatea de a exclude efectele altor factori de risc pentru boli hepatice cronice, cum ar fi consumul de alcool și droguri, în plus, eterogenitatea studiilor trebuie luată în considerare, deoarece limitează analiza globală, precum și având o specificitate mai mică pentru nivelurile aminotransferazei decât biopsiile luate la momentul diagnosticării și evaluării bolii hepatice (28).
deși printre studiile majore pentru a evalua efectul utilizării vitaminei E la pacienții cu NASH nu am găsit diferențe semnificative statistic cu utilizarea placebo și alte opțiuni terapeutice pe termen scurt, există îngrijorare cu privire la posibilele efecte adverse ale utilizării prelungite a vitaminei E.
o revizuire sistematică a nouă randomizate a inclus noi studii randomizate controlate cu placebo pentru a evalua efectele vitaminei E pentru o perioadă de cel puțin un an asupra incidenței globale a accidentelor cerebrovasculare, precum și a subtipurilor de Accidente cerebrovasculare. S-a constatat un risc crescut de accident vascular cerebral hemoragic (RR = 1,22, IÎ 95%: 1,0 până la 1,48, p = 0,045). Datorită rezultatelor obținute din revizuirea lor, cercetătorii recomandă evitarea utilizării nediscriminatorii a vitaminei E din cauza consecințelor grave ale accidentelor vasculare cerebrale hemoragice în morbiditate și mortalitate (29).
un studiu randomizat controlat cu placebo, care a inclus 35.533 de pacienți urmăriți timp de cel puțin șapte ani, a studiat riscurile vitaminei E legate de cancerul de prostată. Acesta a comparat un grup placebo cu un grup care a primit vitamina E la o doză zilnică de 400 UI. A existat o creștere semnificativă a riscului de cancer de prostată în rândul celor care au luat vitamina E (HR 1,17; 99% CI, 1,004-1,360; p = 0,008). Creșterea absolută a riscului a fost de 1,6 la 1000 persoane ani (30).
o altă meta-analiză a analizat relația doză-răspuns a suplimentării cu vitamina E și mortalitatea totală la adulți. Acesta a arătat că pacienții care primesc doze mari de vitamina E (mai mari sau egale cu 400 UI/zi) au crescut mortalitatea din toate cauzele. Această meta-analiză și-a limitat căutarea la studii randomizate controlate ale căror probe de pacienți au constat din adulți care au primit tratament cu vitamina E singură sau în combinație cu alte vitamine sau minerale și care au exclus femeile însărcinate și care au avut un minim de 1 an de tratament și monitorizare. Rezultatele furnizate de această meta-analiză trebuie luate în considerare cu precauție, deoarece mai multe studii au dimensiuni mici ale eșantioanelor și au fost efectuate la pacienții cu mai multe boli cronice. Acest lucru limitează capacitatea studiului de a generaliza rezultatele la populația adultă sănătoasă (31).
concluzie
deși în prezent nu există o terapie medicamentoasă eficientă pentru pacienții cu NASH, dovezile prezentate de studiul PIVENS sugerează că administrarea corectă a vitaminei E îmbunătățește histologia hepatică la pacienții adulți non-cirotici cu NASH care nu au diabet. Cu toate acestea, sunt necesare mai multe studii înainte ca această recomandare să poată fi extinsă la pacienții diabetici sau la pacienții care au ciroză cu NASH. Studiile efectuate pe pacienți pediatrici cu NASH nu au găsit dovezi suficiente pentru a susține utilizarea vitaminei E. Pe lângă administrarea de vitamina E, S-a demonstrat că pierderea în greutate reduce steatoza și inflamația ficatului. Pierderea în greutate printr-o dietă cu conținut scăzut de calorii combinată cu o activitate fizică crescută trebuie recomandată tuturor pacienților. În ceea ce privește efectele secundare, nu am găsit diferențe semnificative statistic în utilizarea pe termen scurt a vitaminei E cu placebo și alte opțiuni de tratament. Totuși, utilizarea nediscriminatorie a vitaminei E nu este recomandată pentru perioade lungi de timp, deoarece există dovezi care sugerează riscuri crescute de cancer de prostată, accident vascular cerebral hemoragic și deces din toate cauzele.
1. Abbas AK, Fausto N. H. Ro: Robbins SL, Mitchell RN, Kumar V, Abbas AK, Fausto N. patologie nouă funcțională și estructurală. 8va Ed. Barcelona: Elsevier; 2012. p. 645-687.
2. Brunt E, Neuschwander-Tetri B, Burt AD. Boala hepatică grasă: alcoolică și nealcoolică. En: Burt AD, Ferrell, l Portmann BC. Patologia MacSween a ficatului. Ediția a 6-a. MAREA BRITANIE: Elservier; 2012. p. 293-359.
3. Corrado RL, Torres DM, Harrison SA. Revizuirea opțiunilor de tratament pentru boala hepatică grasă nealcoolică. Med Clin N Am 2014; 98: 55-72.
4. Koek GH, LIEDORP PR, Bast A. rolul stresului oxidativ în steatohepatita nealcoolică. Clinica Chimica Acta 2011; 412: 1297-1305.
5. Cortez-Pinto H, Ermelinda Camilo M. Boala hepatică grasă nealcoolică / steatohepatita nealcoolică (NAFLD/NASH): diagnostic și curs clinic. Cele Mai Bune Practici & Cercetare Gastroenterologie Clinică 2004; 18(6): 1089-104.
6. Mishra A, Younossi ZM. Epidemiologie și istoric Natural al bolii hepatice grase nealcoolice. Jurnalul de Hepatologie clinică și experimentală 2012; 2(2): 135-44.
7. Rolo AP, Teodoro JS, Palmeira CM. Rolul stresului oxidativ în patogeneza steatohepatitei nealcoolice. Gratuit Radic Biol Med 2012; 52 (1): 59-69.
8. Machado MV, Cortez-Pinto H. Diagnosticul neinvaziv al bolii hepatice grase nealcoolice. O evaluare critică. Jurnalul de Hepatologie 2013; 58 (5): 1007-19.
9. Chalasani N, și colab. Diagnosticul și gestionarea bolilor hepatice grase nealcoolice: Ghid de practică de către Asociația Americană pentru studiul bolilor hepatice, Colegiul American de Gastroenterologie și Asociația gastroenterologică Americană. Hepatologie 2012; 55.
10. Mazzella N, Ricciardi LR, Mazzotti A, Marchesini G. rolul medicamentelor pentru gestionarea pacienților cu NAFLD. Clin Ficat Dis 2014; 18: 73-89.
11. Chunga mea, Yeunga SF, Parka HJ, Volekb JS, Brunoa RS. Suplimentarea dietetică cu tocoferol și cu tocoferol atenuează stresul oxidativ indus de lipopolizaharide și răspunsurile legate de inflamație într-un model de șoarece obez de steatohepatită nealcoolică. Jurnalul de Biochimie nutrițională 2010; 21: 1200-1206.
12. Ziua CP, James de. Steatohepatita: o poveste a două hituri? Gastroenterologie 1998; 114: 842-4.
13. Harper HA, Murray RK, Rodwell VW, Bender DA. Bioqqumica ilustrada, 28 ed. M: McGraw-Hill Interamericana; 2010. p. 484-485.
14. Neuschwander-Tetri BA. Lipotoxicitatea hepatică și patogeneza steatohepatitei nealcoolice: rolul central al metaboliților acizilor grași nontrigliceridici. Hepatologie 2010; 52 (2): 774-88.
15. Le T, Loomba R. gestionarea bolilor hepatice grase nealcoolice și a steatohepatitei. Jurnalul de Hepatologie clinică și experimentală 2012; 2: 156-173.
16. Verdam FJ, Dallinga JW, Driessen, De Jonge C, Moonen E, van Berkel J, Luijk J, Bouvy ND, Buurman AW, Rensen SS, Greve JW. Steatohepatita Non-alcoolică: un diagnostic neinvaziv prin analiza respirației expirate. Jurnalul de Hepatologie 2013; 58: 543-548.
17. Palmentieri B, de Sio I, La Mura V, și colab. Rolul modelului ecou hepatic luminos pe examinarea cu ultrasunete B-mod în diagnosticul steatozei hepatice. Dig Dis Ficat 2006; 38: 485-9.
18. Sanyal AJ și colab. Pioglitazonă versus vitamina E versus placebo pentru tratamentul pacienților non-diabetici cu steatohepatită nealcoolică: proiectarea studiului PIVENS. Procesele Contemp Clin 2009; 30 (1): 88-96.
19. Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, bas NM și colab. Pioglitazonă, vitamina E sau placebo pentru steatohepatită nealcoolică. N Engl J Med 2010; 362 (18): 1675-85.
20. De asemenea, este important să se țină cont de faptul că, în cazul în care nu există nici un fel de probleme, este necesar să se ia în considerare. Vitamina E și modificări ale nivelurilor serice de alanin aminotransferază la pacienții cu steatohepatită nealcoolică. Aliment Pharmacol Ther 2013; 38 (2): 134-43.
21. Lavine JE, Schwimmer JB, Molleston JP, Scheimann AO, Murray KF, Abrams Sh și colab. Tratamentul bolii hepatice grase nealcoolice la copii: proiectarea procesului TONIC. Procesele Contemp Clin 2010; 31(1): 62-70.
22. Lavine JE, Schwimmer JB, Van Natta ML și colab. Efectul vitaminei E sau metforminei pentru tratamentul bolii hepatice grase nealcoolice la copii și adolescenți: studiul tonic randomizat controlat. JAMA 2011; 305(16): 1659-68.
23. Yakaryilmaz F, Guliter S, Savas B, Erdem O, Ersoy R, Erden E și colab. Efectele tratamentului cu vitamina E asupra expresiei alfa a receptorului activat de proliferatorul peroxizomului și a rezistenței la insulină la pacienții cu steatohepatită nealcoolică: rezultatele unui studiu pilot. Intern Med J 2007; 37 (4): 229-35.
24. Vajro P, Mandato C, Franzese A, Ciccimarra E, Lucariello S, Savoia M, și colab. Tratamentul cu vitamina E în bolile hepatice legate de obezitate pediatrică: un studiu randomizat. J Pediatr Gastroenterol Nutr 2004; 38(1): 48-55
25. Papastergiou V, și colab. Nouă modele de notare pentru mortalitatea pe termen scurt în hepatita alcoolică: validare încrucișată într-o cohortă dovedită prin biopsie. Aliment Pharmacol Ther 2014; 39: 721-732.
26. Kugelmas M, Hill DB, Vivian B, Marsano L, McClain CJ. Citokine și NASH: un studiu pilot al efectelor modificării stilului de viață și a vitaminei E. Hepatologie 2003; 38(2): 413-9.
27. Younossi ZM, Reyes MJ, Mishra MA, Mehta R, Henry L. revizuire sistematică cu meta-analiză: steatohepatita nealcoolică-un caz de tratament personalizat bazat pe ținte patogene. Aliment Pharmacol Ther2014; 39: 3-14.
28. Ji HF, și colab. Efectul suplimentării cu vitamina E asupra nivelurilor de aminotransferază la pacienții cu NAFLD, NASH și CHC: rezultă dintr-o meta-analiză. Nutriție 2014; 1-6.
29. Markus S, Robert JG, Pamela MR, Christophe T, Tobias K. efectele vitaminei E asupra subtipurilor de accident vascular cerebral: meta-analiză a studiilor controlate randomizate. BMJ 2010; 341.
30. Klein EA, Thompson IM, Tangen CM și colab. Vitamina E și riscul de cancer de prostată: studiul de prevenire a cancerului cu seleniu și vitamina E (selectați). JAMA 2011; 306(14): 1549-56.
31. Miller ER, 3rd, Pastor-Barriuso R, Dalal D, Riemersma RA, Appel LJ, Guallar E. Meta-analiză: suplimentarea cu doze mari de vitamina E poate crește mortalitatea din toate cauzele. Ann Med Intern 2005; 142(1): 37-46.