Estereoisomerización en el\(\alfa\)-carbono
Los enolatos son un intermediario común en reacciones donde la configuración estereoquímica de un \(\alfa\)-carbono quiral está interconvertida. Estos se conocen comúnmente como reacciones de racemización o epimerización, dependiendo de si los isómeros interconvertidos son enantiómeros o epímeros (recordemos que el término «epímero» se refiere a un par de diastereómeros que difieren por un solo centro quiral).
Racemización / epimerización:
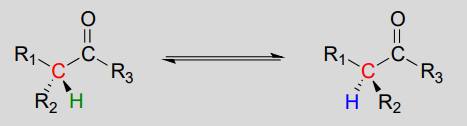
Mecanismo:
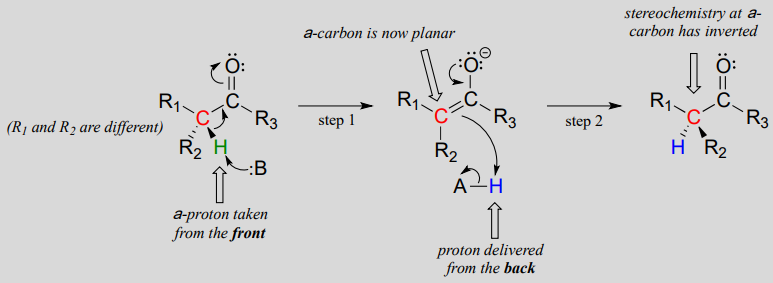
Estas reacciones proceden a través de un mecanismo de desprotonación-reprotonación, ilustrado arriba. En el paso 1, el carbono a quiral se desprotona, dando lugar a un enolato aquiral plano. En el paso 2, un protón se devuelve al carbono a, pero desde el lado opuesto del que se tomó el protón en el paso 1, lo que resulta en la estereoquímica opuesta a este carbono. Dos grupos ácido-base, ubicados en lados opuestos del sitio activo de la enzima, trabajan en conjunto para lograr esta hazaña.
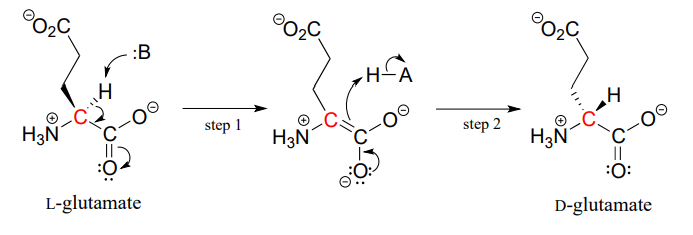
Las proteínas y péptidos en todos los seres vivos conocidos están construidos casi exclusivamente de L-aminoácidos, pero en casos raros los científicos han identificado péptidos que incorporan D-aminoácidos, que tienen la estereoquímica opuesta en el carbono a. Las enzimas racemasas de aminoácidos catalizan la interconversión de los aminoácidos L y D. Como recordarán de la sección introductoria de este capítulo, el veneno del ornitorrinco macho contiene un péptido neurotóxico en el que un aminoácido L-leucina ha sido convertido por una enzima racemasa en D-leucina. En otro ejemplo, las paredes celulares de las bacterias se construyen en parte de péptidos que contienen D-glutamato, convertidos a partir de L-glutamato por la enzima glutamato racemasa. (EC 5.1.1.3) (Bioquímica 2001, 40, 6199).
Una reacción (EC 5.1.3.1) en el metabolismo del azúcar implica la interconversión de los epímeros ribulosa-5-fosfato y xilulosa-5-fosfato. La enzima que cataliza esta reacción se llama «epimerasa». (J. Mol. Biol. 2003, 326, 127).

Ejercicio \(\Índice de página{2}\)
Dibuje un mecanismo razonable para la reacción de epimerización de ribulosa-5-fosfato anterior. Su mecanismo debe mostrar un intermedio enolato y especificar estereoquímica en todas partes.
Ejercicio \(\Índice de página{3}\)
Predecir los productos de las reacciones de epimerización a partir de cada uno de los sustratos mostrados.
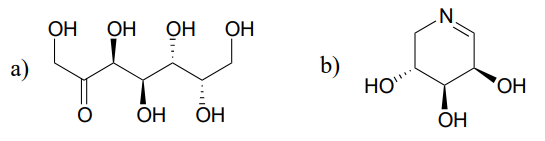
Sugerencia
Los carbonos junto a los grupos iminos también se pueden considerar\(\alfa\)-¡carbonos!
Recuerde del capítulo 3 que un problema importante con el medicamento talidomida es el hecho de que el enantiómero R, que es un sedante eficaz, se isomeriza rápidamente en el cuerpo al enantiómero S terotogénico (que causa mutaciones). Tenga en cuenta que el centro quiral de la talidomida es un carbono \(\alfa\).
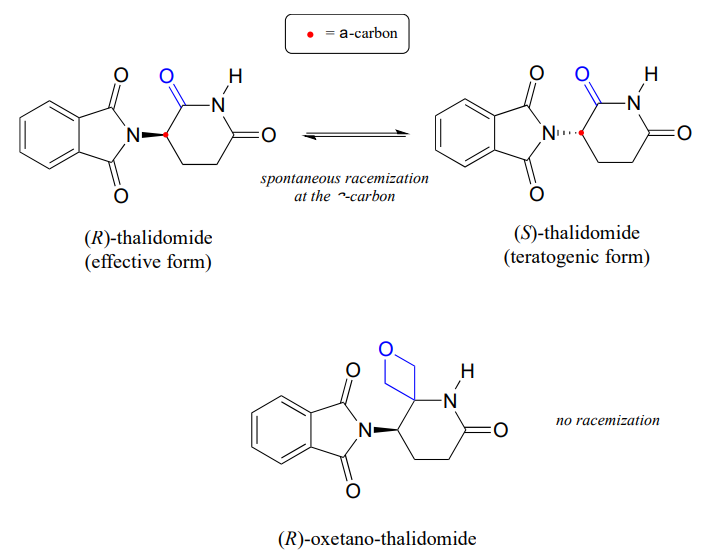
Recientemente, los químicos informaron la síntesis de un derivado de talidomida en el que el grupo carbonilo es reemplazado por un anillo de ‘oxetano’, con el objetivo de hacer una forma isotópicamente estable del fármaco (debido a que se ha eliminado el grupo carbonilo, la racemización ya no es posible, ¡no hay carbono a!) (Org. Lett. 2013, 15, 4312.)