Stereoisomerisatie op de\(\alpha\)-koolstof
Enolaten zijn een veel voorkomend tussenproduct in reacties waarbij de stereochemische configuratie van een chirale \(\alpha\)-koolstof onderling is geconverteerd. Deze worden algemeen bedoeld als racemization of epimerisatiereacties, afhankelijk van of de interconverted isomeren enantiomers of epimers zijn (Herinner dat de term ‘epimer’ verwijst naar een paar diastereomeren die door één enkel chiral centrum verschillen).
racemisatie / epimerisatie:
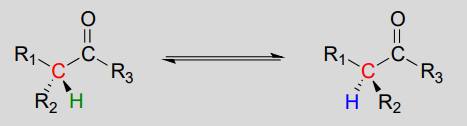
mechanisme:
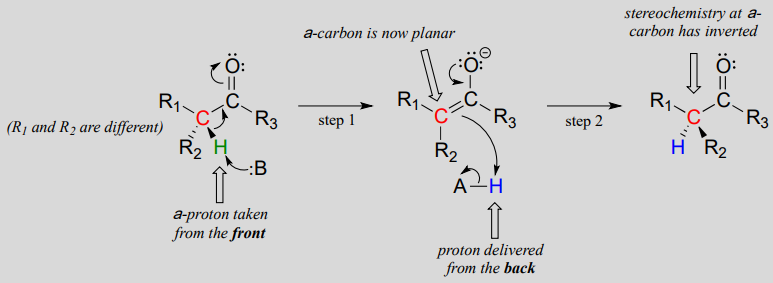
deze reacties verlopen via een deprotonatie-reprotonatiemechanisme, zoals hierboven geïllustreerd. In Stap 1, wordt de chirale a-koolstof gedeprotoneerd, leidend tot een vlakke, achiral enolaat. In Stap 2 wordt een proton teruggevoerd naar de A-koolstof, maar van de andere kant van waaruit het proton werd genomen in Stap 1, wat resulteert in de tegenovergestelde stereochemie bij deze koolstof. Twee zuur-base groepen, gepositioneerd bij tegengestelde kanten van de actieve plaats van het enzym, werken in tandem om deze prestatie te bereiken.
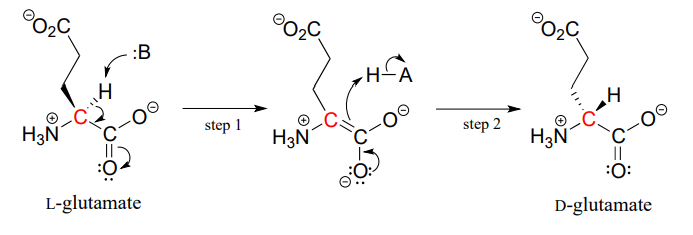
de eiwitten en peptiden in alle bekende levende wezens zijn bijna uitsluitend opgebouwd uit L-aminozuren, maar in zeldzame gevallen hebben wetenschappers peptiden geïdentificeerd die D-aminozuren bevatten, die de tegenovergestelde stereochemie hebben bij de A-koolstof. Aminozuurracemase enzymen katalyseren de interconversie van L en D aminozuren. Zoals u zich wellicht herinnert uit de inleiding tot dit hoofdstuk, bevat het gif van het mannelijke vogelbekdier een neurotoxisch peptide waarin een L-leucine aminozuur door een racemase-enzym is omgezet in D-leucine. In een ander voorbeeld, worden de celwanden van bacteriën geconstrueerd in deel van peptides die d-glutamate bevatten, omgezet van L-glutamate door het enzymglutamate racemase. (EC 5.1.1.3) (Biochemie 2001, 40, 6199).
een reactie (EC 5.1.3.1) in het suikermetabolisme impliceert de interconversie van de epimeren ribulose-5-fosfaat en xylulose-5-fosfaat. Het enzym dat deze reactie katalyseert wordt een ‘epimerase’genoemd. (J. Mol. Biol. 2003, 326, 127).

oefening \(\Paginindex{2}\)
teken een redelijk mechanisme voor de ribulose-5-fosfaat epimerisatie reactie hierboven. Uw mechanisme moet tonen een enolate tussenliggende en specificeer stereochemie hele.
oefening \(\Paginindex{3}\)
voorspel de producten van epimerisatie reacties te beginnen met elk van de getoonde substraten.
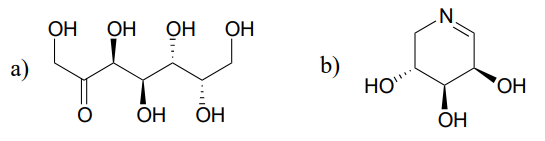
Hint
koolstof naast imine groepen kan ook worden beschouwd als \(\alpha\) – koolstof!
herinner uit hoofdstuk 3 dat een belangrijk probleem met het geneesmiddel thalidomide het feit is dat de R-enantiomeer, een effectief sedatief, snel isomeriseert in het lichaam tot het terotogene (mutatie veroorzakende) S-enantiomeer. Merk op dat het chirale centrum in thalidomide een \(\alpha\)-koolstof is!
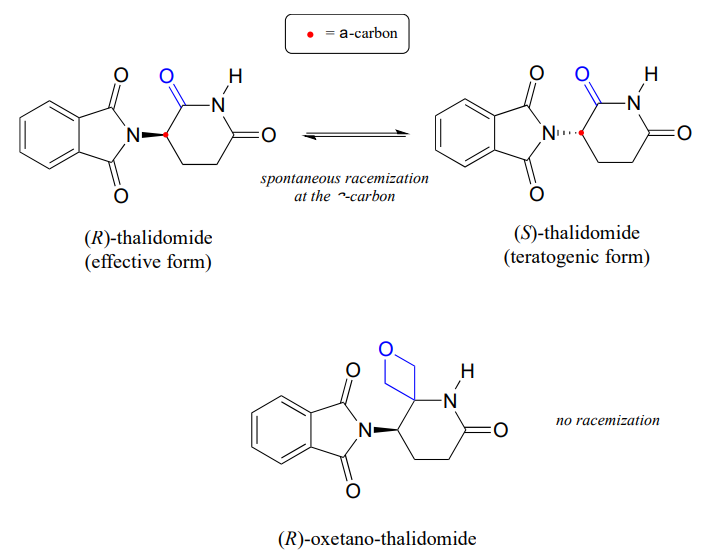
onlangs meldden chemici de synthese van een thalidomidederivaat waarin de carbonylgroep wordt vervangen door een ‘oxetaan’ ring, met als doel een isotopisch stabiele vorm van het geneesmiddel te maken (omdat de carbonylgroep is verwijderd, is racemisatie niet langer mogelijk – er is geen A-koolstof!) (Organisatie. Lett. 2013, 15, 4312.)