a \(\alfa\)-szén
az Enolátok gyakori köztitermékek azokban a reakciókban, ahol a királis \(\alfa\)-szén sztereokémiai konfigurációja átalakul. Ezeket általában racemizációs vagy epimerizációs reakcióknak nevezik, attól függően, hogy az interkonvertált izomerek enantiomerek vagy epimerek (emlékezzünk arra, hogy az ‘epimer’ kifejezés egy diasztereomer párra utal, amelyek egyetlen királis centrummal különböznek egymástól).
racemizáció / epimerizáció:
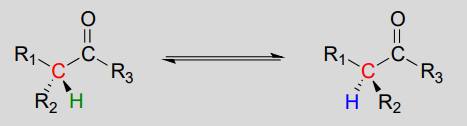
mechanizmus:
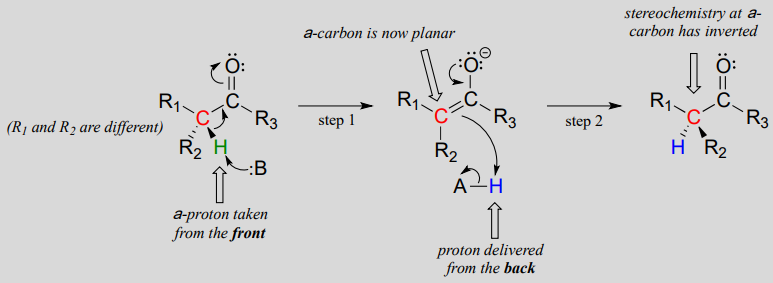
ezek a reakciók deprotonációs-reprotonációs mechanizmuson keresztül zajlanak, a fentiekben bemutatva. Az 1. lépésben a királis a-szén deprotonálódik, ami sík, achirális enoláthoz vezet. A 2. lépésben egy protont juttatunk vissza az a-szénhez, de az ellenkező oldalról, ahonnan a protont az 1.lépésben vettük, ennek a szénnek az ellentétes sztereokémiáját eredményezve. Két sav-bázis csoport, amelyek az enzim aktív helyének ellentétes oldalán helyezkednek el, párhuzamosan dolgoznak ennek a teljesítménynek a megvalósításában.
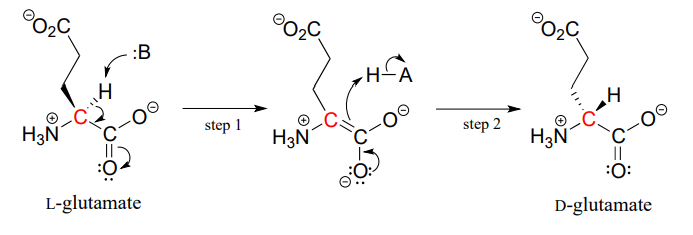
az összes ismert élőlény fehérjéi és peptidjei szinte kizárólag L-aminosavakból épülnek fel, de ritka esetekben a tudósok olyan peptideket azonosítottak, amelyek D-aminosavakat tartalmaznak, amelyek ellentétes sztereokémiával rendelkeznek az a-szénnél. Az aminosav-racemáz enzimek katalizálják az L és D aminosavak interkonverzióját. Amint a fejezet bevezető szakaszából emlékeztethet, a hím kacsacsőrű emlős mérge neurotoxikus peptidet tartalmaz, amelyben egy L-leucin aminosavat racemáz enzim d-leucinná alakított át. Egy másik példában a baktériumok sejtfalait d-glutamátot tartalmazó peptidek egy részében építjük fel, amelyet a glutamát racemáz enzim l-glutamátból alakít át. (EK 5.1.1.3.) (Biochemistry 2001, 40, 6199).
a cukor metabolizmusában egy reakció (EC 5.1.3.1) az epimerek ribulóz-5-foszfát és xilulóz-5-foszfát interkonverzióját foglalja magában. Az enzimet, amely katalizálja ezt a reakciót, epimeráznak nevezzük. (J. Mol. Biol. 2003, 326, 127).

gyakorlat \(\PageIndex{2}\)
rajzoljunk egy ésszerű mechanizmust a fenti ribulóz-5-foszfát epimerizációs reakcióra. A mechanizmusnak enolate köztiterméket kell mutatnia, és meg kell határoznia a sztereokémiát.
gyakorlat \(\PageIndex{3}\)
jósolja meg az epimerizációs reakciók termékeit, kezdve az egyes ábrázolt szubsztrátokkal.
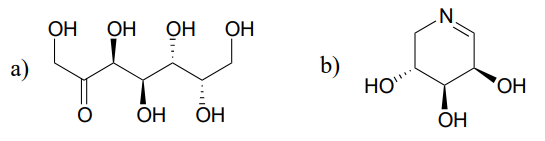
tipp
az imincsoportok melletti szénatomok \(\alpha\)-szénatomoknak is tekinthetők!
Emlékezzünk vissza a 3.fejezetből, hogy a talidomid gyógyszer egyik fő problémája az a tény, hogy az R enantiomer, amely hatékony nyugtató, gyorsan izomerizálódik a szervezetben a terotogén (mutációt okozó) s enantiomerré. Vegye figyelembe, hogy a talidomid királis központja \(\alfa\)-szén!
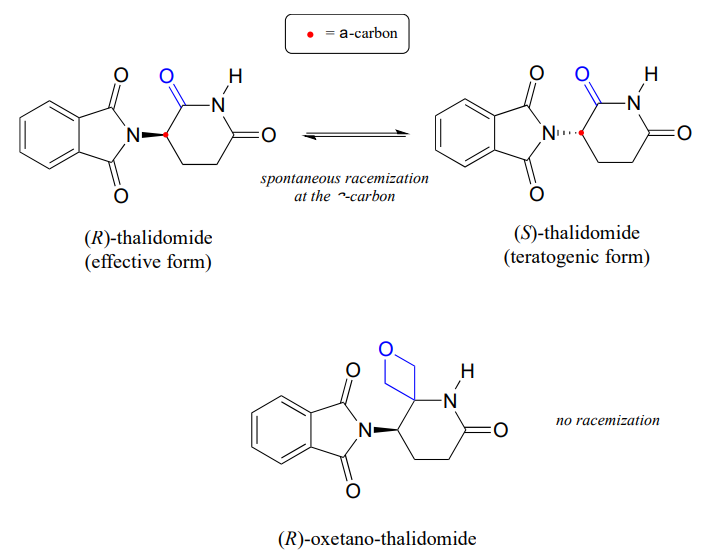
a közelmúltban a vegyészek beszámoltak egy talidomid-származék szintéziséről, amelyben a karbonilcsoportot egy ‘oxetán’ gyűrű váltja fel, azzal a céllal, hogy a gyógyszer izotóposan stabil formáját hozzák létre (mivel a karbonilcsoportot eltávolították, a racemizáció már nem lehetséges – nincs a-szén!) (Org. Lett. 2013, 15, 4312.)