Stereoisomerisaatio \(\alpha\)-hiilessä
Enolaatit ovat yleinen Välituote reaktioissa, joissa kiraalisen \(\alpha\)-hiilen stereokemiallinen konfiguraatio on interconverted. Näitä kutsutaan yleisesti rasemisaatioksi tai epimerisaatioreaktioiksi riippuen siitä, ovatko keskenään muuntuneet isomeerit enantiomeerejä vai epimeerejä (muista, että termi ”epimer” viittaa diastereomeeripariin, jotka eroavat toisistaan yhden kiraalisen keskuksen avulla).
Rasemisaatio/ epimerisaatio:
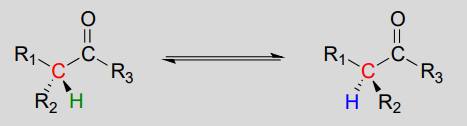
mekanismi:
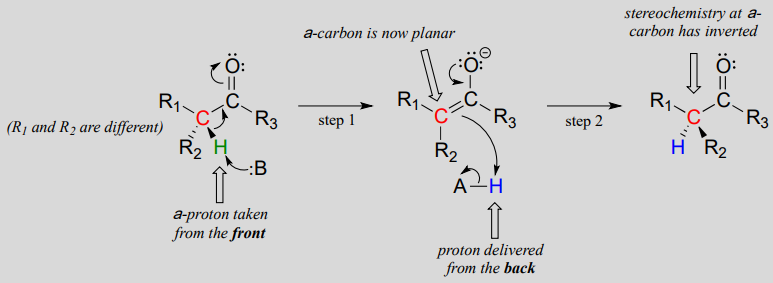
nämä reaktiot etenevät deprotonaatio-reprotonaatiomekanismilla, kuten yllä on kuvattu. Vaiheessa 1 kiraalinen a-hiili deprotonoituu, jolloin muodostuu tasomainen, akiraalinen enolaatti. Vaiheessa 2 a-hiilelle luovutetaan protoni takaisin, mutta vastakkaiselta puolelta, jolta protoni otettiin vaiheessa 1, jolloin tämän hiilen stereokemia on päinvastainen. Kaksi happo-emäsryhmää, jotka sijaitsevat vastakkaisilla puolilla entsyymin aktiivista kohtaa, toimivat yhdessä tämän tehtävän saavuttamiseksi.
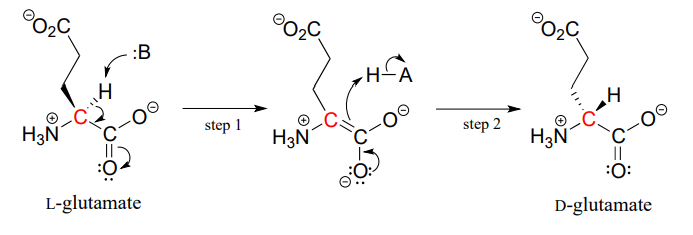
kaikkien tunnettujen elollisten proteiinit ja peptidit rakentuvat lähes yksinomaan L-aminohapoista, mutta harvoissa tapauksissa tutkijat ovat tunnistaneet D-aminohappoja sisältäviä peptidejä, joiden stereokemia a-hiilessä on päinvastainen. Aminohapporasemaasientsyymit katalysoivat L-ja D-aminohappojen transkonversiota. Kuten ehkä muistatte tämän luvun johdantokappaleesta, vesinokkaeläin-uroksen myrkky sisältää neurotoksista peptidiä, jossa rasemaasientsyymi on muuttanut l-leusiiniaminohapon d-leusiiniksi. Toisessa esimerkissä bakteerien soluseinät rakentuvat osaan D-glutamaattia sisältävistä peptideistä, jotka glutamaattirasemaasientsyymi muuntaa L-glutamaatista. (EC 5.1.1.3) (Biochemistry 2001, 40, 6199).
sokeriaineenvaihdunnan reaktiossa (EC 5.1.3.1) epimeerien ribuloosi-5-fosfaatti ja ksyluloosi-5-fosfaatti muuntuvat keskenään. Tätä reaktiota katalysoivaa entsyymiä kutsutaan ”epimeraasiksi”. (J. Mol. Biol. 2003, 326, 127).

harjoitus \(\PageIndex{2}\)
Piirrä kohtuullinen mekanismi ribuloosi-5-fosfaatin epimerisaatioreaktiolle edellä. Mekanismissasi pitäisi näkyä enolaattiväli ja määrittää stereokemia kauttaaltaan.
harjoitus \(\PageIndex{3}\)
ennustetaan epimerisaatioreaktioiden tuotteet Alkaen kustakin esitetystä substraatista.
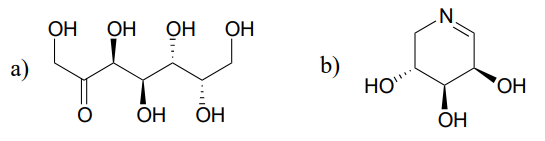
Vihje
Imiiniryhmien vieressä olevia hiilivetyjä voidaan pitää myös \(\alpha\) – hiilivetyjä!
muista luvusta 3, että merkittävä ongelma talidomidilääkkeessä on se, että R-enantiomeeri, joka on tehokas rauhoittava aine, isomeroituu elimistössä nopeasti terotogeeniseksi (mutaatiota aiheuttavaksi) S-enantiomeeriksi. Huomaa, että talidomidin kiraalinen keskus on \(\alpha\)-hiili!
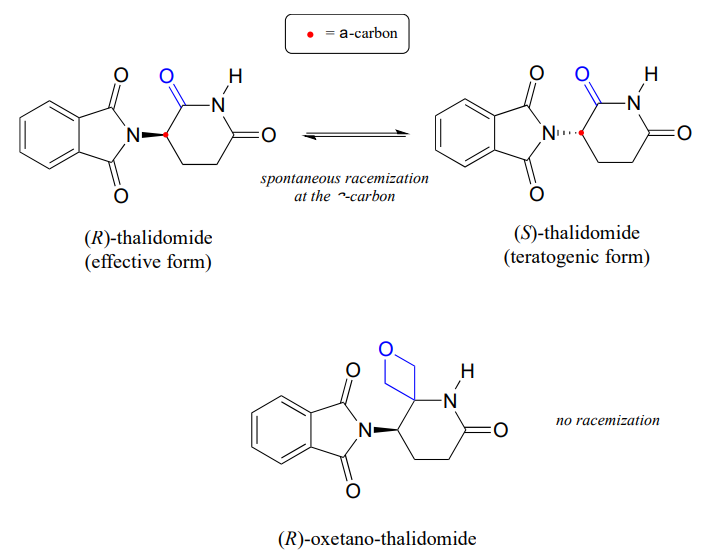
äskettäin kemistit raportoivat talidomidijohdannaisen synteesistä, jossa karbonyyliryhmä korvataan oksetaanirenkaalla, tavoitteena tehdä lääkkeestä isotooppisesti stabiili muoto (koska karbonyyliryhmä on poistettu, rasemisaatio ei ole enää mahdollista – ei ole a-hiiltä!) (Org. Lett. 2013, 15, 4312.)