Quick Takes
- Trotz des Mangels an longitudinalem Outcome-Nutzen In den vorherigen klinischen Studien kann die Beurteilung der myokardialen Lebensfähigkeit immer noch eine Rolle spielen auf einer personalisierten Ebene der klinischen Entscheidungsfindung für Hochrisikopatienten mit mittelschwerer und fortgeschrittener koronarer Herzkrankheit.
- Frühere Studien verwendeten hauptsächlich Einzelphotonenemissions-Computertomographie (SPECT) und Dobutamin-Stress-Echokardiographie zur Beurteilung der Lebensfähigkeit; die neue Technologie bietet eine höhere Sensitivität mit kontrastverstärkter kardiovaskulärer Magnetresonanz (CMR) und eine höhere Spezifität mit Dobutamin-Stress-CMR, um eine Verbesserung der regionalen Funktion vorherzusagen nach Revaskularisation.
- Klinische Marker wie ischämische Symptome sowie das Vorhandensein von Zielgefäßen für die Revaskularisation sollten vor der Bewertung für die nicht-invasive Lebensfähigkeitsbewertung sorgfältig überprüft werden.
Einleitung
Herz-Kreislauf-Erkrankungen sind nach wie vor die häufigste Ursache für Mortalität und Morbidität in der modernen Medizin.1 Es gab zahlreiche Forschungsstudien, die sich auf kardiovaskuläre Präventionsstrategien konzentrierten, um zukünftige akute ischämische Ereignisse zu verhindern, indem das Fortschreiten der Atherosklerose verlangsamt und das Risiko einer Plaquestörung und einer überlagerten Thrombose verringert wurde. Die Beurteilung der myokardialen Lebensfähigkeit befand sich am Ende dieses Spektrums und wurde entwickelt, um Patienten mit ischämischer Kardiomyopathie auszuwählen, die möglicherweise eine Umkehrung der Myokardfunktionsstörung aufweisen.
Akute und rezidivierende ischämische Ereignisse führen zu einer ischämischen Kardiomyopathie, die mit wiederkehrenden Krankenhausaufenthalten, schlechter Lebensqualität und erhöhter Mortalität einhergeht. Dieser Prozess kann umgekehrt werden, wenn wir dysfunktionale, aber lebensfähige Myokardzellen bei Patienten mit ischämischer Kardiomyopathie identifizieren können. In den letzten Jahrzehnten hat die Fähigkeit, lebensfähiges Myokard zu erkennen, mit aufkommenden Technologien in der kardiovaskulären Bildgebung zugenommen und entwickelt sich mit zunehmender Technologie weiter.
Trotz aller Fortschritte beim Nachweis lebensfähiger Myokardzellen wurde in prospektiven Studien kein Einfluss auf das klinische Ergebnis nach Revaskularisation nachgewiesen.2,3 Dieser Artikel wird die aktuelle Rolle der nicht-invasiven Bewertung der myokardialen Lebensfähigkeit in der klinischen Praxis überprüfen und die wichtigsten Punkte im kürzlich veröffentlichten Dokument zum Stand der Technik zur Bildgebung der myokardialen Lebensfähigkeit der American Heart Association (AHA) zusammenfassen.4
Irreversible und reversible ischämische Schädigung: Fibrose, Winterschlaf und Betäubung
Bei chronischer Verringerung des myokardialen Blutflusses führt die Aktivierung der verschiedenen Wege zu Entzündungen, Apoptose, Nekrose und schließlich zur Bildung von Narbengewebe. Wenn die Blutversorgung deutlich verringert, aber nicht vollständig gestört ist, kann der Myokardschaden in geringerem Maße sein; Myokardzellen wären immer noch lebensfähig und könnten nach Wiederherstellung der Blutversorgung ihre Funktion wiedererlangen. Es gibt zwei verschiedene Arten von Myokardfunktionsstörungen bei Ischämie: Winterschlaf und Betäubung.
Eine anhaltend verminderte Blutversorgung kann eine Herunterregulierung der Myokardfunktion im Winterschlaf induzieren, wohingegen Betäubung sich auf eine beeinträchtigte kontraktile Funktion trotz normalem Ruhefluss bezieht.5,6 Unabhängig vom Blutfluss ist die Koronarflussreserve bei beiden Arten von Myokardfunktionsstörungen verringert, was schließlich zu strukturellen und funktionellen Veränderungen des Myokards führt, indem eine koronare Ischämie verursacht wird. Es kann auch zu einer Abnahme der koronaren Flussreserve bei Patienten ohne epikardiale flussbegrenzende Erkrankung, aber mit schwerer mikrovaskulärer Dysfunktion kommen. Fibrosen oder Infarktgewebe haben nachteilige Auswirkungen auf den Myokardumbau und sind mit nachteiligen Ergebnissen verbunden; Selbst ein Myokard im Winterschlaf kann jedoch als Substrat für Herzrhythmusstörungen dienen und das Risiko eines plötzlichen Herztodes erhöhen.7
Nicht-invasive Bildgebungsmodalitäten zur Beurteilung der myokardialen Lebensfähigkeit
Die Beurteilung der linksventrikulären Größe und Funktion mit Echokardiographie ist ein wesentliches Instrument zur Bewertung der myokardialen Lebensfähigkeit. Während die Wandverdünnung nicht zuverlässig ist, um die reversible Myokardfunktion abzuschätzen, ist eine erhöhte linksventrikuläre Größe mit einer schlechten Prognose nach Revaskularisation verbunden.
Die Dobutamin-Stress-Echokardiographie wurde häufig zur Beurteilung der Kontraktilität und Lebensfähigkeit des Myokards eingesetzt. Bei kontinuierlicher Dobutamininfusion nimmt die Myokardperfusion zunächst zusammen mit der Kontraktilität zu, aber mit zunehmender Dobutamindosis kann der Blutfluss nicht weiter eskaliert werden, was zu einer verringerten Kontraktilität führt. Dieses Phänomen ist als biphasische Reaktion bekannt, die die Wiederherstellung der Myokardfunktion nach der Revaskularisation vorhersagt.8
Die Speckle-Tracking-Echokardiographie ist eine weitere aufkommende Modalität, mit der die linksventrikuläre Erholung nach Myokardinfarkt genau abgeschätzt werden kann. Die Echokontrast-Perfusionsbildgebung, die die mikrovaskuläre Integrität des Herzens erkennt, ist ebenfalls vielversprechend; Aufgrund der sehr variablen Reproduzierbarkeit erfordert sein Nutzen für die Lebensfähigkeitsbewertung jedoch weitere Untersuchungen.9
In den letzten Jahrzehnten wurden die Einzelphotonenemissions-Computertomographie (SPECT) und die Positronen-Emissions-Tomographie (PET) in großem Umfang zur Beurteilung der Myokardlebensfähigkeit eingesetzt. Als Kaliumanalogon kann Thallium verwendet werden, um die Integrität der Myokardzellmembran über Na / K-Atpasekanäle nachzuweisen, bei denen lebensfähige Zellen im Vergleich zur ruhenden Bildgebung eine verzögerte Aufnahme aufweisen.10 Im Gegensatz zu Thallium weist SPECT auf Technetiumbasis keine verzögerte Verteilung auf.11 In den letzten Jahrzehnten wurde Thallium aufgrund der Zunahme ionisierender Strahlung im Vergleich zu Technetium selten verwendet.
Eine weitere häufig verwendete nukleare Bildgebungsmodalität zur Beurteilung der myokardialen Vitalität ist die kardiale PET. In einem gesunden Myokard stammt die Energiequelle aus Fettsäuren, während sie sich in einem ischämischen Zustand in Richtung eines glukosebasierten Stoffwechsels verschiebt. 18F-Fluorodesoxyglucose (18F-FDG) kann diese Verschiebung im lebensfähigen Myokard nachweisen. Die übliche Beurteilung der Lebensfähigkeit besteht aus Rest Imaging und metabolische Bildgebung mit 18F-FDG. In Bereichen ohne Ruheperfusion, wie mit gezeigt N-13 Ammoniak oder Rubidium-82, Vorhandensein einer 18F-FDG-Aufnahme zeigt die Lebensfähigkeit an. Im Vergleich zu SPECT hat PET eine höhere räumliche Auflösung, eine geringere Strahlung und eine bessere Dämpfungskorrektur. Bei Patienten mit Insulinresistenz kann die FDG-Aktualisierung im normalen Bereich geringer bleiben als in ischämischen oder im Winterschlaf befindlichen Regionen. Eine Einschränkung der PET ist die Variabilität der FDG-Werte, die durch Herzzeitvolumen, Herzinsuffizienz, Grad der Ischämie und sympathische Aktivität beeinflusst werden kann.12
Wenn die Ischämie anhält, treten myokardiale Apoptose und Nekrose auf, was zu einem erhöhten extrazellulären Raum führt, der durch kardiovaskuläre Magnetresonanz (CMR) mit später Gadoliniumverstärkung (LGE) nachgewiesen werden kann. Bei Patienten mit chronischer ischämischer Kardiomyopathie sagt die transmurale Ausdehnung von LGE die Reversibilität der Myokardkontraktion nach erfolgreicher Revaskularisation voraus.13 Während ein minimales LGE (< 25%) in einem dysfunktionalen Myokardsegment eine hohe Heilungschance anzeigt, ist die Heilungschance bei einem > 50% igen LGE eines transmuralen Infarkts sehr gering.13 In dieser Hinsicht liefert die LGE-CMR nützliche Informationen zur Anleitung der Revaskularisation. In Segmenten mit Borderline-LGE-Beteiligung (25-50%) ist die Erholungsprognose mit LGE nicht stark genug.13
Unter allen oben genannten Studien weist der LGE-Prozentsatz der Wanddicke die höchste Sensitivität (95%) und die Dobutamin-Stress-CMR die höchste Spezifität (91%) zur Vorhersage der regionalen myokardialen Erholung auf, während die Dobutamin-Stress-Echokardiographie eine gute Vorhersagbarkeit mit einer Sensitivität von 80% und einer Spezifität von 78% zeigte. SPECT (87% bzw. 83% für Thallium- und Technetium-Bildgebung) und PET (92%) basierte Kernlebensfähigkeitsstudien haben eine gute Sensitivität; Die Spezifität war jedoch im Vergleich zu anderen Modalitäten geringer (< 70%).14-16
The Role of Viability Imaging in Clinical Practice
Die Autoren des State of the Art: Imaging for Viability4 schlugen zwei verschiedene Algorithmen bei Patienten mit chronischer (Abbildung 1) und subakuter (Abbildung 2) ischämischer Kardiomyopathie vor. Für beide Algorithmen ist es wichtig, mehrere Faktoren zu bewerten, zu denen die Symptome, die Zielgefäße für die Revaskularisation und der Grad des Umbaus gehören.
Abbildung 1
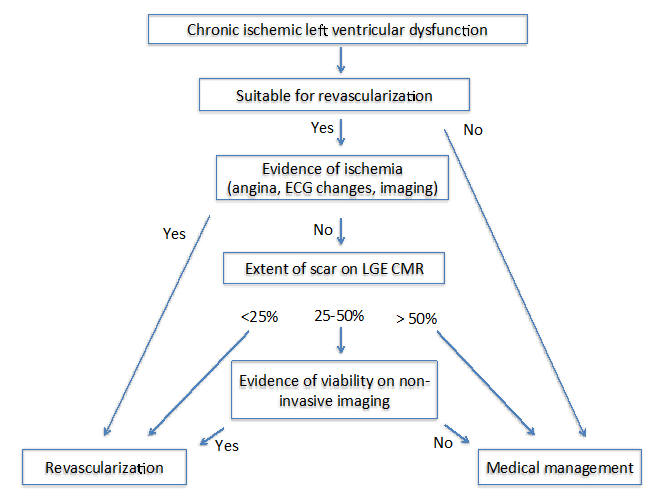
Abbildung 1

Abbildung 2
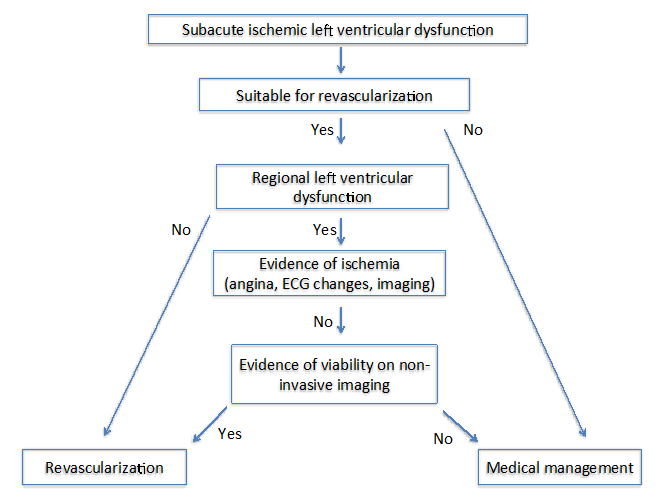
Abbildung 2

Die Auswirkungen auf die Beurteilung der Lebensfähigkeit auf das Ergebnis
Die Subgruppenanalyse der Studie zur chirurgischen Behandlung der ischämischen Herzinsuffizienz (STICH) zeigte, dass Patienten mit Lebensfähigkeit eine geringere Langzeitmortalität aufwiesen als Patienten, die keine Anzeichen einer Lebensfähigkeit zeigten, und es gab eine signifikante Verbesserung der linksventrikulären Ejektionsfraktion (LVEF) bei Patienten, die unabhängig von der Behandlungsstrategie eine myokardiale Lebensfähigkeit zeigten. Das Ergebnis nach Koronararterien-Bypass-Transplantation (CABG) unterschied sich jedoch nicht signifikant bei Patienten mit Lebensfähigkeit im Vergleich zu Patienten ohne Lebensfähigkeit.3 Die Verbesserung der LVEF war bei Patienten mit Lebensfähigkeit, die eine Revaskularisation aufwiesen, im Vergleich zu Patienten, die mit einer medikamentösen Therapie behandelt wurden, ähnlich.3
Bemerkenswert ist, dass in der STICH-Studie die Lebensfähigkeit mit Dobutamin-Stress-Echokardiographie oder SPECT beurteilt wurde. In ähnlicher Weise unterschied sich das Ergebnis jedoch in der F-18-Fluorodesoxyglucose-Positronen-Emissions-Tomographie-gestützten Behandlung von Patienten mit schwerer linksventrikulärer Dysfunktion und Verdacht auf Koronarerkrankung (PARR-2) nicht, wenn die Lebensfähigkeit über PET bei Patienten mit ischämischer Kardiomyopathie, die sich einer CABG unterziehen, beurteilt wurde.17 Es ist unklar, warum die Lebensfähigkeit im Vergleich zur medizinischen Therapie keinen Einfluss auf das Ergebnis nach der Revaskularisation hatte; dies könnte an der erfolgreichen Durchführung der medizinischen Therapie liegen oder einfach an der Komplexität der Entscheidungsfindung bei diesen Patienten, bei denen mehrere andere Risikofaktoren eine Rolle spielen, die über eine Bildgebungsmodalität hinausgehen.
Schlussfolgerung
Obwohl kein Einfluss der myokardialen Lebensfähigkeit auf das Überleben nach Revaskularisation nachgewiesen wurde, könnte es in der klinischen Praxis immer noch eine Rolle spielen, insbesondere bei Hochrisikopatienten mit fortgeschrittenem Alter oder mit signifikanten Komorbiditäten, bei denen Risiken und Nutzen der Revaskularisation unklar bleiben. Bei Patienten mit ischämischer Kardiomyopathie und einem hohen Risikowert der Society of Thoracic Surgeons (STS) ist das Management komplex und zukünftige Studien sollten diese Ära weiterhin mit multimodaler Bildgebung unter Berücksichtigung mehrerer anderer Risikofaktoren untersuchen, die das Ergebnis beeinflussen könnten.
Die zugrunde liegenden Komorbiditäten und Patientenmerkmale sollten sorgfältig überprüft werden, um die richtige Bildgebungsmodalität für die Beurteilung der Lebensfähigkeit zu wählen. Die Entscheidung, PET oder CMR zu verwenden, wird von Patient zu Patient getroffen. PET sollte in Betracht gezogen werden, wenn ein Patient mit einem großen Myokardinfarkt, von dem angenommen wurde, dass er durch eine alternative Bildgebungstechnik nicht lebensfähig ist, weiterhin eine refraktäre oder symptombegrenzende Angina pectoris, Herzinsuffizienz-Exazerbationen trotz maximaler medizinischer Therapie, ventrikuläre Arrhythmien oder eine signifikante Koronararterienstenose aufweist, bei der das Vorhandensein einer kleinen Insel lebensfähigen Myokards wahrscheinlich die Entscheidung zugunsten der Revaskularisation beeinflusst. Bei Patienten mit Nierenversagen oder einem implantierten Herzgerät wird PET bevorzugt. Bei Patienten mit schlecht kontrolliertem Diabetes, stark reduzierter Ejektionsfraktion mit einer enddiastolischen Dicke von weniger als 6 mm oder bei Patienten mit Stenose bei multipler Koronararterienverteilung sollte PET vermieden werden Bei schwerer Klaustrophobie, Nierenversagen oder Vorhandensein von implantierten Geräten ist die Anwendung von CMR begrenzt und / oder kontraindiziert.
- Murray CJ, Lopez ANZEIGE. Alternative Projektionen von Mortalität und Behinderung nach Ursache. 1990-2020: globale Krankheitslaststudie. Lanzette 1997;349: 1498-504.
- Bonow RO, Maurer G, Lee KL, et al. Myokardiale Lebensfähigkeit und Überleben bei ischämischer linksventrikulärer Dysfunktion. N Engl J Med 2011;364:1617-25.
- Panza JA, Ellis AM, Al-Khalidi HR, et al. Myokardiale Lebensfähigkeit und langfristige Ergebnisse bei ischämischer Kardiomyopathie. N Engl J Med 2019;381:739-8.
- Garcia MJ, Kwong RY, Scherrer-Crosbie M, et al. Stand der Technik: Bildgebung für myokardiale Lebensfähigkeit: eine wissenschaftliche Erklärung der American Heart Association. Circ Cardiovasc Imaging 2020;Juli 13:.
- Bolli R. Grundlegende und klinische Aspekte des Myokardinfarkts. Prog Cardiovasc Dis 1998;40:477-516.
- Ryan MJ, Perera D. Identifizieren und Verwalten von hibernating Myokard: Was ist neu und was bleibt unbekannt? Curr Herz versagen Rep 2018;15: 214-23.
- Canty JM Jr, Suzuki G, Banas MD, Verheyen F, Borgers M, Fallavollita JA. Myokard im Winterschlaf: chronisch an Ischämie angepasst, aber anfällig für plötzlichen Tod. Circ Res 2004;94:1142-9.
- Hernandez-Pampaloni M, Peral V, Carreras JL, Sanchez-Harguindey L, Vilacosta I. Die zweiphasige Reaktion auf Dobutamin sagt eine Verbesserung der linksventrikulären Dysfunktion nach Revaskularisation voraus: korrelation mit Positronen-Emissions- und Rest-Umverteilung 2017 Tomographien. Int J Cardiovasc Bildgebung 2003;19:519-28.
- Porter TR, Mulvagh SL, Abdelmoneim SS, et al. Klinische Anwendungen von ultraschallverstärkenden Wirkstoffen in der Echokardiographie: 2018 American Society of Echocardiography Guidelines Update. J Am Soc Echocardiogr 2018;31:241-74.
- Piwnica-Worms D, Chiu ML, Kronauge JF. Divergente Kinetik von 201Tl und 99mTc-SESTAMIBI in kultivierten linksventrikulären Myozyten während der ATP-Depletion. Auflage 1992;85:1531-41.
- Berman DS, Kiat H, Van Train KF, Friedman J, Garcia EV, Maddahi J. Vergleich von SPECT unter Verwendung von Technetium-99m-Agenten und Thallium-201 und PET zur Beurteilung der Myokardperfusion und Lebensfähigkeit. Am J Cardiol 1990;66:72E-79E.
- Löffler AI, Kramer CM. Myokardiale Lebensfähigkeitstests zur Anleitung der koronaren Revaskularisation. Interv Cardiol Clin 2018;7:355-65.
- Kim RJ, Wu E, Rafael A, et al. Die Verwendung einer kontrastmittelverstärkten Magnetresonanztomographie zur Identifizierung einer reversiblen Myokardfunktionsstörung. N Engl J Med 2000;343:1445-53.
- Bax JJ, Poldermans D, Elhendy A, Boersma E, Rahimtoola SH. Sensitivität, Spezifität und Vorhersagegenauigkeiten verschiedener nichtinvasiver Techniken zum Nachweis von Myokard im Ruhezustand. Curr Probl Cardiol 2001;26:147-186.
- Bax JJ, van der Wall EE, Harbinson M. Radionuklidtechniken zur Beurteilung der myokardialen Lebensfähigkeit und des Winterschlafs. Herz 2004;90: v26-v33.
- Pagano D., Bonser R., Townend J., Ordoubadi F., Lorenzoni R., Camici P. Prädiktiver Wert der Dobutamin-Echokardiographie und Positronen-Emissions-Tomographie bei der Identifizierung des hibernierenden Myokards bei Patienten mit postischämischer Herzinsuffizienz. Herz 1998;79: 281-8.
- Beanlands RSB, Nichol G, Huszti E, et al. F-18-Fluorodesoxyglucose-Positronen-Emissions-Tomographie-Bildgebung-unterstütztes Management von Patienten mit schwerer linksventrikulärer Dysfunktion und Verdacht auf koronare Herzkrankheit: eine randomisierte, kontrollierte Studie (PARR-2). J Am Coll Cardiol 2007;50:2002-12.
Klinische Themen: Arrhythmien und klinische Symptome, Diabetes und kardiometabolische Erkrankungen, Dyslipidämie, Herzinsuffizienz und Kardiomyopathien, Nichtinvasive Bildgebung, Implantierbare Geräte, SCD/ventrikuläre Arrhythmien, Vorhofflimmern/supraventrikuläre Arrhythmien, Lipidstoffwechsel, Neuartige Wirkstoffe, Computertomographie, Echokardiographie/Ultraschall, Nukleare Bildgebung
Schlüsselwörter: Dyslipidemias, Apoptosis, Arrhythmias, Cardiac, Biological Phenomena, Atherosclerosis, Ammonia, Cardiomyopathies, Cicatrix, Cardiovascular Diseases, Constriction, Pathologic, Contrast Media, Coronary Vessels, Death, Sudden, Cardiac, Dobutamine, Down-Regulation, Echocardiography, Echocardiography, Stress, Extracellular Space, Fatty Acids, Fluorodeoxyglucose F18, Gadolinium, Glucose, Hemodynamics, Hibernation, Hospitalization, Inflammation, Insulin Resistance, Myocardial Ischemia, Ischemia, Multimodal Imaging, Myocardium, Myocytes, Cardiac, Plaque, Atherosclerotic, Positron-Emission Tomography, Prognose, Kalium, Lebensqualität, Reproduzierbarkeit der Ergebnisse, Risikofaktoren, Rubidium, Rubidium-Radioisotope, Schlagvolumen, Technetium, Thallium, Thrombose, Tomographie, Emission-Computed, Ventrikuläre Funktion, Links
< Zurück zu den Auflistungen