Quick Takes
- ondanks het gebrek aan longitudinale uitkomstvoordeel in de vorige klinische onderzoeken, kan de beoordeling van de levensvatbaarheid van de myocardiale patiënt nog steeds een rol spelen op een gepersonaliseerd niveau van klinische besluitvorming bij patiënten met een hoog risico met matige en gevorderde coronaire hartziekte.
- in eerdere studies werd voornamelijk gebruik gemaakt van single-photon emission computed tomography (SPECT) en dobutamine stress echocardiografie voor de beoordeling van de levensvatbaarheid; opkomende technologie biedt een hogere gevoeligheid met contrast versterkte cardiovasculaire magnetische resonantie (CMR) en een hogere specificiteit met dobutamine stress CMR om verbetering van de regionale functie na revascularisatie te voorspellen.
- klinische markers zoals ischemische symptomen en de aanwezigheid van doelvaten voor revascularisatie dienen zorgvuldig te worden beoordeeld voordat een beoordeling van de niet-invasieve levensvatbaarheid wordt uitgevoerd.
hart-en vaatziekten blijven de belangrijkste oorzaak van mortaliteit en morbiditeit in de moderne tijd van de geneeskunde.1 Er zijn tal van onderzoeken gericht op cardiovasculaire preventie strategieën om te helpen voorkomen toekomstige acute ischemische gebeurtenissen door het vertragen van de progressie van atherosclerose en het verminderen van het risico van plaque verstoring en gesuperponeerde trombose. De beoordeling van de levensvatbaarheid van het myocard is aan het einde van dit spectrum uitgevoerd en is ontworpen om patiënten met ischemische cardiomyopathie te selecteren die een omkering van de myocarddisfunctie kunnen vertonen.
Acute en recidiverende ischemische voorvallen leiden tot ischemische cardiomyopathie die geassocieerd wordt met recidiverende ziekenhuisopnames, slechte kwaliteit van leven en verhoogde mortaliteit. Dit proces kan worden omgekeerd als we disfunctionele maar levensvatbare myocardiale cellen in patiënten met ischemische cardiomyopathie kunnen identificeren. In de afgelopen decennia is de capaciteit om levensvatbare myocardium te ontdekken met opkomende technologieën in cardiovasculaire weergave toegenomen en blijft evolueren aangezien de technologie groeit.
ondanks alle vorderingen bij het opsporen van levensvatbare myocardiale cellen, is in prospectieve studies niet aangetoond dat beeldvorming van de levensvatbaarheid een impact heeft op de klinische uitkomst na revascularisatie.2,3 dit artikel zal de huidige rol van niet-invasieve myocardiale viability assessment in de klinische praktijk evalueren en de belangrijkste punten samenvatten in het onlangs gepubliceerde state of the art document on imaging for myocardiale viability document van de American Heart Association (AHA).4
irreversibele en reversibele ischemische schade: Fibrose, winterslaap en bedwelming
met chronische vermindering van de myocardbloeddoorstroming leidt activering van de verschillende routes tot ontsteking, apoptose, necrose en uiteindelijk littekenweefsel vorming. Wanneer de bloedtoevoer duidelijk verminderd maar niet volledig verstoord is, kan de myocardiale schade van een mindere mate zijn; myocardiale cellen zouden nog steeds levensvatbaar zijn en potentieel hun functie herwinnen nadat de bloedtoevoer hersteld is. Er zijn twee verschillende soorten myocardiale dysfunctie in de setting van ischemie: winterslaap en verbluffend.
aanhoudend verminderde bloedtoevoer kan leiden tot downregulatie van de myocardiale functie tijdens de winterslaap, terwijl bedwelming verwijst naar een verminderde contractiele functie ondanks een normale ruststroom.5,6 ongeacht de bloedstroom, coronaire stroomreserve is verlaagd in beide soorten myocardiale disfunctie, die uiteindelijk leidt tot structurele en functionele veranderingen in het myocardium door het veroorzaken van de vraag ischemie. Er kan ook een afname van de coronaire flow reserve zijn bij patiënten zonder epicardiale flow beperkende ziekte maar met ernstige microvasculaire disfunctie. Fibroses of infarcted weefsel heeft schadelijke gevolgen voor myocardiale remodellering en wordt geassocieerd met ongunstige resultaten; nochtans, kan zelfs het hibernating myocardium als substraat voor hartritmestoornissen dienen en het risico van plotselinge hartdood verhogen.7
niet-invasieve Beeldvormingsmodaliteiten om de levensvatbaarheid van het myocardinfarct te beoordelen
beoordeling van de grootte en functie van het linkerventrikel met echocardiografie is een essentieel instrument voor de evaluatie van de levensvatbaarheid van het myocardinfarct. Hoewel dunner worden van de wand niet betrouwbaar is om de reversibele myocardiale functie in te schatten, wordt een verhoogde linker ventriculaire grootte geassocieerd met een slechte prognose na revascularisatie.
echocardiografie van dobutaminestress is op grote schaal gebruikt om de contractiliteit en levensvatbaarheid van het myocard te beoordelen. Bij continue dobutamine-infusie neemt de myocardiale perfusie aanvankelijk samen met de contractiliteit toe, maar naarmate de dobutamine-dosis toeneemt, kan de bloedstroom niet verder worden geëscaleerd, wat resulteert in verminderde contractiliteit. Dit fenomeen staat bekend als bifasische reactie die het herstel van de myocardiale functie na revascularisatie voorspelt.8
Speckle tracking echocardiografie is een andere opkomende modaliteit die het herstel van de linkerventrikel na een myocardinfarct nauwkeurig kan inschatten. De echo contrast perfusie beeldvorming die cardiale microvasculaire integriteit detecteert is ook veelbelovend; echter, als gevolg van zeer variabele reproduceerbaarheid, het nut voor de levensvatbaarheid beoordeling zal verder onderzoek vereisen.9
in de afgelopen decennia zijn single-photon emission computed tomography (SPECT) en positron emission tomography (PET) op grote schaal gebruikt om de levensvatbaarheid van het myocardinfarct te beoordelen. Omdat het een kaliumanalogon is, kan thallium worden gebruikt om de integriteit van het myocardiale celmembraan via de kanalen van Na/K ATPase te detecteren, waar levensvatbare cellen vertraagde opname in vergelijking met rustweergave aantonen.In tegenstelling tot thallium vertoont SPECT op basis van technetium geen vertraagde distributie.11 in de afgelopen decennia is thallium zelden gebruikt vanwege een toename van ioniserende straling in vergelijking met technetium.
een andere veelgebruikte nuclear imaging modaliteit om de vitaliteit van het myocard te beoordelen is cardiac PET. In een gezond myocardium, is de energiebron afgeleid van vetzuren, terwijl in een ischemische toestand het verschuift naar glucose-gebaseerde metabolisme. 18F-fluorodeoxyglucose (18F-FDG) kan deze verschuiving in levensvatbaar myocardium ontdekken. De gebruikelijke beoordeling van de levensvatbaarheid bestaat uit rest imaging en metabole imaging met 18F-FDG. In gebieden zonder rustperfusie, zoals aangetoond met n-13 ammoniak of rubidium-82, duidt de aanwezigheid van 18F-FDG opname op levensvatbaarheid. Vergeleken met SPECT, heeft huisdier hogere ruimtelijke resolutie, lagere straling, en heeft betere demping correctie. Van nota, bij patiënten met insulineresistentie, kan de FDG-update in normaal gebied minder dan die van ischemische of overwinterende gebieden blijven. Een beperking van PET is de variabiliteit van FDG-update, die kan worden beïnvloed door cardiale output, hartfalen, mate van ischemie en sympathische activiteit.12
wanneer ischemie aanhoudt, treedt myocardiale apoptose en necrose op, wat resulteert in een verhoogde extracellulaire ruimte die kan worden gedetecteerd door cardiovasculaire magnetische resonantie (CMR) met late gadoliniumversterking (LGE). Bij patiënten met chronische ischemische cardiomyopathie voorspelt de transmurale omvang van LGE de reversibiliteit van de myocardiale contractie na succesvolle revascularisatie.Hoewel minimale LGE (<25%) in een disfunctioneel myocardiaal segment duidt op een hoge waarschijnlijkheid van herstel, is de kans op herstel in een >50% LGE van transmuraal infarct zeer laag.13 in dit verband biedt LGE CMR nuttige informatie als leidraad voor de revascularisatie. In segmenten met borderline LGE-betrokkenheid (25-50%) is de herstelvoorspelling met LGE niet sterk genoeg.13
van alle bovengenoemde studies heeft het LGE-percentage van de wanddikte de hoogste gevoeligheid (95%) en heeft dobutaminestress CMR de hoogste specificiteit (91%) om regionaal myocardiologisch herstel te voorspellen, terwijl de echocardiografie van dobutaminestress een goede voorspelbaarheid vertoonde met 80% gevoeligheid en 78% specificiteit. SPECT (87% en 83% voor respectievelijk thallium-en technetiumbeeldvorming), en PET (92%) gebaseerde studies naar de nucleaire levensvatbaarheid hebben een goede gevoeligheid; de specificiteit was echter lager in vergelijking met andere modaliteiten (<70%).14-16
the Role of Viability Imaging in Clinical Practice
de auteurs van The State of the Art: Imaging for Viability4 stelden twee verschillende algoritmen voor bij patiënten met chronische (figuur 1) en subacute (Figuur 2) ischemische cardiomyopathie. Voor beide algoritmen, is het belangrijk om verscheidene factoren te beoordelen die de symptomen, doelvaten voor revascularisatie en de graad van het remodelleren omvatten.
figuur 1
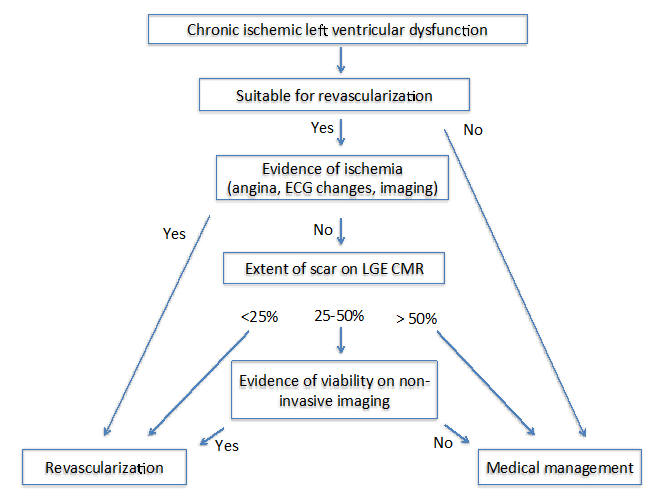
figuur 1

Figuur 2
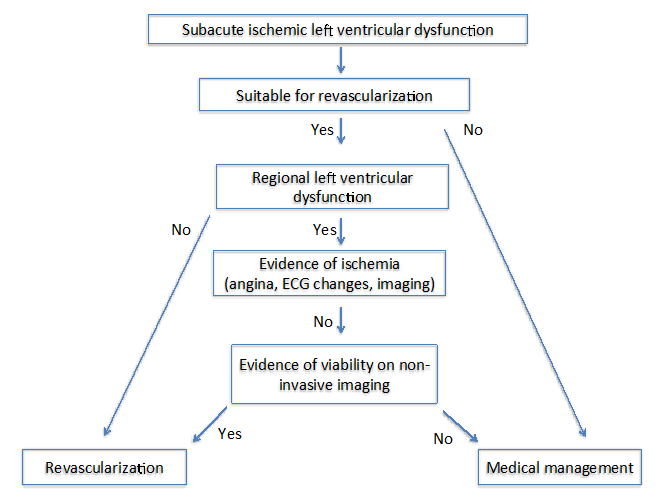
Figuur 2

the Impact on Viability Assessment on Outcome
de subgroepanalyse van de studie Surgical Treatment for Ischemic Heart Failure (STICH) toonde aan dat patiënten met levensvatbaarheid een lagere langetermijnsterfte hadden in vergelijking met patiënten die geen tekenen van levensvatbaarheid vertoonden, en dat er een significante verbetering was in de linkerventrikelejectiefractie (LVEF) bij patiënten die myocardiale levensvatbaarheid vertoonden, ongeacht de behandelingsstrategie. Het resultaat na coronaire bypass-enten (CABG) was echter niet significant verschillend bij patiënten met levensvatbaarheid in vergelijking met patiënten zonder levensvatbaarheid.3 de verbetering van de LVEF was vergelijkbaar bij patiënten met levensvatbaarheid die revascularisatie hadden in vergelijking met patiënten die werden behandeld met medische therapie.3
in het STICH-onderzoek werd de levensvatbaarheid beoordeeld met behulp van echocardiografie of SPECT van dobutaminestress. Ook in het F-18-fluorodeoxyglucose positron emissie tomografie imaging assisted management van patiënten met ernstige linkerventrikeldisfunctie en vermoedelijke coronaire ziekte (PARR-2) onderzoek was de uitkomst niet anders wanneer de levensvatbaarheid werd beoordeeld via PET bij patiënten met ischemische cardiomyopathie die CABG ondergingen.Het is onduidelijk waarom levensvatbaarheid geen invloed had op de uitkomst na revascularisatie in vergelijking met medische therapie; het zou aan succesvolle uitvoering van de medische therapie toe te schrijven kunnen zijn, of het zou eenvoudig de ingewikkeldheid van de besluitvorming in die patiënten kunnen weerspiegelen, waar verscheidene andere risicofactoren een rol voorbij een weergavemodaliteit spelen.
conclusie
hoewel niet is aangetoond dat de levensvatbaarheid van het myocardinfarct een effect heeft op de overleving na revascularisatie, kan het nog steeds een rol spelen in de klinische praktijk, met name bij hoogrisicopatiënten in gevorderde leeftijd of met significante comorbiditeiten waarbij de risico ‘ s en voordelen van revascularisatie onduidelijk blijven. Bij patiënten met ischemische cardiomyopathie en een High Society of Thoracic Surgeons (STS) risk score, is de behandeling complex en toekomstige studies moeten doorgaan met het verkennen van dit tijdperk met multimodaliteit beeldvorming in overweging van verschillende andere risicofactoren die de uitkomst kunnen beïnvloeden.
onderliggende comorbiditeiten en patiëntkenmerken moeten zorgvuldig worden beoordeeld om de juiste beeldvormingsmodaliteit te kiezen voor de beoordeling van de levensvatbaarheid. De beslissing om PET of CMR te gebruiken wordt genomen op patiënt-tot-patiënt basis. PET moet worden overwogen wanneer een patiënt met een groot myocardinfarct dat werd gedacht niet-levensvatbaar door een alternatieve beeldvormingstechniek te zijn blijft refractaire of symptoom beperkende angina, hartfalen exacerbaties ondanks maximale medische therapie, ventriculaire aritmieën, of heeft een significante coronaire arteriële stenose waar de aanwezigheid van zelfs een klein eiland van levensvatbare myocardium zal waarschijnlijk swing de beslissing ten gunste van revascularisatie. Bij patiënten met nierfalen of een geïmplanteerd hartapparaat heeft PET de voorkeur. Bij patiënten met slecht gecontroleerde diabetes, ernstig gereduceerde ejectiefractie, met een diastolische einddikte van minder dan 6 mm, of patiënten met stenose in de distributie van meerdere kransslagaders, dient PET te worden vermeden terwijl bij ernstige claustrofobie, nierfalen of de aanwezigheid van geïmplanteerde hulpmiddelen het gebruik van CMR beperkt en/of gecontra-indiceerd is.
- Murray CJ, Lopez AD. Alternatieve prognoses van sterfte en invaliditeit naar oorzaak. 1990-2020: global burden of disease study. Lancet 1997; 349: 1498-504.
- Bonow RO, Maurer G, Lee KL, et al. Myocardiale levensvatbaarheid en overleving bij ischemische linkerventrikeldisfunctie. N Engl J Med 2011; 364: 1617-25.
- Panza JA, Ellis AM, Al-Khalidi HR, et al. Myocardiale levensvatbaarheid en langetermijnresultaten bij ischemische cardiomyopathie. N Engl J Med 2019; 381: 739-8.
- Garcia MJ, Kwong RY, Scherrer-Crosbie m, et al. State of the art: imaging for myocardial viability: een wetenschappelijke verklaring van de American Heart Association. Circ Cardiovasc Imaging 2020;Jul 13:.
- Bolli R. basis-en klinische aspecten van myocardiale bedwelming. Prog Cardiovasc Dis 1998; 40: 477-516.
- Ryan MJ, Perera D. identificeren en beheren van het myocardium in winterslaap: Wat is nieuw en wat blijft onbekend? Ik Heb Nog Geen Bericht Van Steam Support Ontvangen.
- Canty JM Jr, Suzuki G, Banas MD, Verheyen F, Borgers M, Fallavollita JA. Myocardium in winterslaap: chronisch aangepast aan ischemie, maar kwetsbaar voor plotselinge dood. Circ Res 2004; 94: 1142-9.Hernandez-Pampaloni m, Peral V, Carreras JL, Sanchez-Harguindey L, Vilacosta I. bifasische respons op dobutamine voorspelt verbetering van de linkerventrikeldisfunctie na revascularisatie: correlatie met positron emissie en rust-herverdeling 201tl tomografieën. Int J Cardiovasc Imaging 2003; 19: 519-28.
- Porter TR, Mulvagh SL, Abdelmoneim SS, et al. Klinische toepassingen van ultrasone enhancing agents in echocardiography: 2018 American Society of Echocardiography guidelines update. J Am Soc Echocardiogr 2018; 31: 241-74.
- Piwnica-Worms D, Chiu ML, Kronauge JF. Divergente kinetiek van 201Tl en 99mTc-SESTAMIBI in gekweekte chick ventriculaire myocyten tijdens ATP uitputting. Oplage 1992; 85: 1531-41.
- Berman DS, Kiat H, van Train KF, Friedman J, Garcia EV, Maddahi J. Comparison of SPECT using technetium-99m agents and thallium-201 and PET for the assessment of myocardial perfusion and viability. Am J Cardiol 1990; 66: 72E-79E.
- Löffler AI, Kramer CM. Myocardiale levensvatbaarheid testen om coronaire revascularisatie te begeleiden. Interv Cardiol Clin 2018; 7: 355-65.
- Kim RJ, Wu E, Rafael A, et al. Het gebruik van contrastverhogende magnetic resonance imaging om reversibele myocardiale disfunctie te identificeren. N Engl J Med 2000; 343: 1445-53.
- Bax JJ, Poldermans D, Elhendy A, Boersma E, Rahimtoola SH. Gevoeligheid, specificiteit, en voorspellende nauwkeurigheid van diverse niet-invasieve technieken voor het ontdekken van winterslaap myocardium. Curr Probl Cardiol 2001; 26: 147-186.
- Bax JJ, Van der Wall EE, Harbinson M. radionuclide techniques for the assessment of myocardial viability and hibernation. Hart 2004; 90: v26-v33.
- Pagano D, Bonser R, Townend J, Ordoubadi F, Lorenzoni R, Camici P. Predictive value of dobutamine echocardiography and positron emission tomography in identifying hibernating myocardium in patients with postischemic heart failure. Heart 1998; 79: 281-8.
- Beanlands RSB, Nichol G, Huszti E, et al. F-18-fluorodeoxyglucose positron emissie tomografie imaging-assisted management van patiënten met ernstige linkerventrikeldisfunctie en vermoedelijke coronaire ziekte: een gerandomiseerde, gecontroleerde studie (PARR-2). J Am Coll Cardiol 2007; 50: 2002-12.
klinische onderwerpen: Aritmieën en klinische EP, Diabetes en cardiometabole ziekte, dyslipidemie, hartfalen en cardiomyopathieën, niet-invasieve beeldvorming, implanteerbare hulpmiddelen, SCD/ventriculaire aritmieën, atriumfibrilleren/supraventriculaire aritmieën, lipidenmetabolisme, nieuwe middelen, computertomografie, echocardiografie/echografie, nucleaire beeldvorming
: Dyslipidemias, Apoptosis, Arrhythmias, Cardiac, Biological Phenomena, Atherosclerosis, Ammonia, Cardiomyopathies, Cicatrix, Cardiovascular Diseases, Constriction, Pathologic, Contrast Media, Coronary Vessels, Death, Sudden, Cardiac, Dobutamine, Down-Regulation, Echocardiography, Echocardiography, Stress, Extracellular Space, Fatty Acids, Fluorodeoxyglucose F18, Gadolinium, Glucose, Hemodynamics, Hibernation, Hospitalization, Inflammation, Insulin Resistance, Myocardial Ischemia, Ischemia, Multimodal Imaging, Myocardium, Myocytes, Cardiac, Plaque, Atherosclerotic, Positron-Emission Tomography, Prognose, kalium, kwaliteit van leven, reproduceerbaarheid van resultaten, risicofactoren, Rubidium, rubidium radio-isotopen, beroerte Volume, Technetium, Thallium, trombose, tomografie, emissie-berekend, ventriculaire functie, Links
< terug naar lijst