a Quick
- annak ellenére, hogy a korábbi klinikai vizsgálatokban nem volt longitudinális eredmény, a szívizom életképességének értékelése továbbra is szerepet játszhat a klinikai döntéshozatal személyre szabott szintjén magas kockázatú, közepes és előrehaladott koszorúér-betegségben szenvedő betegek esetében.
- a korábbi vizsgálatok főként egyfoton emissziós komputertomográfiát (SPECT) és dobutamin stressz echokardiográfiát alkalmaztak az életképesség értékeléséhez; a feltörekvő technológia nagyobb érzékenységet biztosít a kontraszt fokozott cardiovascularis mágneses rezonanciával (CMR) és magasabb specifitással a dobutamin stressz CMR-rel a regionális funkció javulásának előrejelzésére a revaszkularizáció után.
- a klinikai markereket, például az ischaemiás tüneteket, valamint a revaszkularizációra szánt célerek jelenlétét gondosan felül kell vizsgálni a nem invazív életképesség értékelésének értékelése előtt.
Bevezetés
a szív-és érrendszeri betegségek továbbra is a halálozás és a morbiditás vezető okai a modern orvostudomány korában.1 számos olyan kutatási tanulmány készült, amely a kardiovaszkuláris megelőzési stratégiákra összpontosít, hogy segítsen megelőzni a jövőbeni akut ischaemiás eseményeket az ateroszklerózis progressziójának lassításával és a plakk-zavar és az egymásra helyezett trombózis kockázatának csökkentésével. A szívizom életképességének értékelése ennek a spektrumnak a végén volt, amelyet ischaemiás cardiomyopathiában szenvedő betegek kiválasztására terveztek, amelyek a myocardialis diszfunkció megfordulását mutathatják.
az akut és visszatérő ischaemiás események ischaemiás cardiomyopathiához vezetnek, amely visszatérő kórházi kezelésekkel, rossz életminőséggel és megnövekedett mortalitással jár. Ez a folyamat megfordítható, ha azonosítani tudjuk diszfunkcionális, de életképes miokardiális sejtek ischaemiás kardiomiopátiában szenvedő betegeknél. Az elmúlt évtizedekben az életképes szívizom kimutatásának képessége nőtt a kardiovaszkuláris képalkotó technológiák kialakulásával, és a technológia növekedésével tovább fejlődik.
az életképes miokardiális sejtek kimutatásában elért összes előrelépés ellenére az életképesség képalkotása nem bizonyított, hogy hatással lenne a klinikai eredményre revaszkularizáció prospektív vizsgálatokban.2,3 ez a cikk áttekinti a nem invazív myocardialis életképesség értékelésének jelenlegi szerepét a klinikai gyakorlatban, és összefoglalja az American Heart Association (AHA) nemrégiben közzétett korszerű dokumentumának legfontosabb pontjait a myocardialis életképesség képalkotásáról.4
irreverzibilis és reverzibilis ischaemiás károsodás: Fibrózis, hibernáció és kábítás
a myocardialis véráramlás krónikus csökkenésével a különböző útvonalak aktiválása gyulladáshoz, apoptózishoz, nekrózishoz és végül hegszövetképződéshez vezet. Ha a vérellátás jelentősen csökken, de nem teljesen megszakad, a szívizom károsodása kisebb mértékű lehet; a miokardiális sejtek továbbra is életképesek, és potenciálisan visszanyerik funkciójukat a vérellátás helyreállítása után. A myocardialis diszfunkciónak két különböző típusa van az ischaemia hátterében: hibernálás és kábítás.
a tartósan csökkent vérellátás a miokardiális funkció lefelé szabályozását idézheti elő hibernált állapotban, míg a kábítás a normál nyugalmi áramlás ellenére károsodott kontraktilis funkcióra utal.5,6 a véráramlástól függetlenül a szívkoszorúér áramlási tartaléka mindkét típusú myocardialis diszfunkcióban csökken, ami végül strukturális és funkcionális változásokhoz vezet a szívizomban azáltal, hogy keresleti ischaemiát okoz. A szívkoszorúér áramlási tartaléka is csökkenhet azoknál a betegeknél, akiknél nincs epikardiális áramlást korlátozó betegség, de súlyos mikrovaszkuláris diszfunkció. A fibrózisok vagy az infarktusos szövetek káros hatással vannak a szívizom átalakítására, és káros következményekkel járnak; azonban még a hibernáló szívizom is szolgálhat a szívritmuszavarok szubsztrátjaként és növeli a hirtelen szívhalál kockázatát.7
Non-invazív képalkotó módszerek a szívizom életképességének értékelésére
a bal kamra méretének és működésének értékelése echokardiográfiával elengedhetetlen eszköz a szívizom életképességének értékeléséhez. Míg a fal elvékonyodása nem megbízható a reverzibilis miokardiális funkció becsléséhez, a megnövekedett bal kamra mérete a revaszkularizáció utáni rossz prognózissal jár.
a dobutamin stressz echokardiográfiát széles körben használják a szívizom kontraktilitásának és életképességének értékelésére. Folyamatos dobutamin infúzióval a szívizom perfúziója kezdetben növekszik a kontraktilitással együtt, de a dobutamin dózisának növekedésével a véráramlás nem fokozható tovább, ami csökkent kontraktilitást eredményez. Ezt a jelenséget kétfázisú reakciónak nevezik, amely megjósolja a miokardiális funkció helyreállítását a revaszkularizáció után.8
a Foltkövető echokardiográfia egy másik feltörekvő modalitás, amely pontosan megbecsülheti a bal kamrai gyógyulást miokardiális infarktus után. Az echo kontraszt perfúziós képalkotás, amely kimutatja a szív mikrovaszkuláris integritását, szintén ígéretes; a nagyon változó reprodukálhatóság miatt azonban hasznossága az életképesség értékeléséhez további vizsgálatokat igényel.9
az elmúlt évtizedekben az egyfoton emissziós komputertomográfiát (SPECT) és a pozitron emissziós tomográfiát (PET) széles körben alkalmazták a szívizom életképességének felmérésére. Mivel kálium-analóg, a tallium felhasználható a szívizom sejtmembrán integritásának kimutatására Na / K ATPáz csatornákon keresztül, ahol az életképes sejtek késleltetett felvételt mutatnak a nyugalmi képalkotáshoz képest.10 a talliumtól eltérően a technécium alapú SPECT nem mutat késleltetett eloszlást.11 az utóbbi évtizedekben a talliumot ritkán használták az ionizáló sugárzás növekedése miatt a technéciumhoz képest.
egy másik általánosan használt nukleáris képalkotási mód a szívizom vitalitásának értékelésére a szív PET. Egészséges szívizomban az energiaforrás zsírsavakból származik, míg ischaemiás állapotban a glükóz alapú anyagcsere felé tolódik el. A 18F-fluorodeoxiglükóz (18F-FDG) képes kimutatni ezt az elmozdulást az életképes szívizomban. Az életképesség szokásos értékelése nyugalmi képalkotásból és metabolikus képalkotásból áll 18F-FDG-vel. Az N-13 ammóniával vagy rubídium-82-vel bemutatott nyugalmi perfúzió nélküli területeken A 18F-FDG felvétel jelenléte életképességet jelez. A SPECT-hez képest a PET nagyobb térbeli felbontással, alacsonyabb sugárzással és jobb csillapítási korrekcióval rendelkezik. Megjegyzendő, hogy inzulinrezisztenciában szenvedő betegeknél az FDG frissítése a normál területen kisebb lehet, mint az ischaemiás vagy hibernáló régióké. A PET egyik korlátja az FDG változékonysága frissítés, amelyet befolyásolhatja a szívteljesítmény, a szívelégtelenség, az ischaemia mértéke és a szimpatikus aktivitás.12
ha az ischaemia továbbra is fennáll, myocardialis apoptosis és nekrózis lép fel, ami megnövekedett extracelluláris teret eredményez, amelyet késői gadolínium-fokozással (LGE) lehet kimutatni kardiovaszkuláris mágneses rezonancia (CMR). Krónikus ischaemiás kardiomiopátiában szenvedő betegeknél az LGE transzmurális mértéke megjósolja a szívizom összehúzódásának reverzibilitását a sikeres revaszkularizáció után.13 míg a diszfunkcionális miokardiális szegmensben a minimális LGE (<25%) a gyógyulás nagy valószínűségét jelzi, a transzmurális infarktus >50% – os LGE-jében a gyógyulás esélye nagyon alacsony.13 E tekintetben az LGE CMR hasznos információkkal szolgál a revaszkularizáció irányításához. A határ menti LGE-vel (25-50%) rendelkező szegmensekben az LGE-vel történő helyreállítási előrejelzés nem elég erős.13
a fenti vizsgálatok közül a falvastagság LGE százalékának van a legnagyobb érzékenysége (95%), a dobutamin stressz CMR pedig a legmagasabb specifitással rendelkezik (91%) a regionális myocardialis helyreállítás előrejelzésére, míg a dobutamin stressz echokardiográfia jó kiszámíthatóságot mutatott 80% érzékenységgel és 78% specifitással. A SPECT (87%, illetve 83% a tallium és technécium képalkotás esetében), valamint a PET (92%) alapú nukleáris életképességi vizsgálatok jó érzékenységgel rendelkeznek; a specificitás azonban alacsonyabb volt a többi módszerhez képest (<70%).14-16
az életképesség képalkotásának szerepe a klinikai gyakorlatban
a korszerű képalkotás a Életképességért4 szerzői két különböző algoritmust javasoltak krónikus (1.ábra) és szubakut (2. ábra) ischaemiás kardiomiopátiában szenvedő betegeknél. Mindkét algoritmus esetében fontos több tényező felmérése, amelyek magukban foglalják a tüneteket, a revaszkularizáció céledényeit és az átalakítás mértékét.
ábra 1
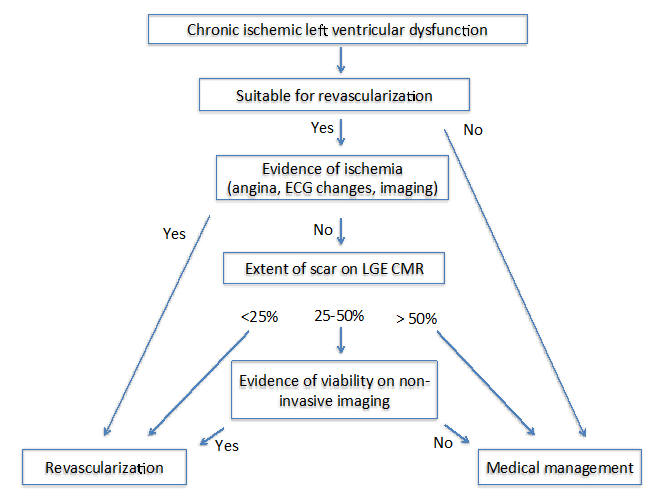
ábra 1

ábra 2
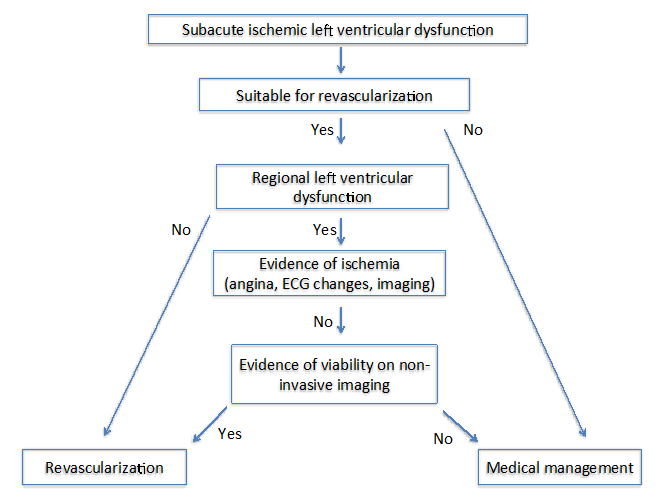
ábra 2

az életképességre gyakorolt hatás értékelése az eredményre
az ischaemiás szívelégtelenség sebészeti kezelése (Stich) vizsgálat alcsoport-elemzése azt mutatta, hogy az életképességgel rendelkező betegeknél alacsonyabb volt a hosszú távú mortalitás, mint azoknál a betegeknél, akik nem mutattak életképességre utaló jeleket, és a bal kamrai ejekciós frakció (LVEF) szignifikáns javulást mutatott azoknál a betegeknél, akik myocardialis életképességet mutattak, függetlenül a kezelési stratégiától. A koszorúér bypass oltása (CABG) utáni eredmény azonban nem volt szignifikánsan különbözik azoknál a betegeknél, akiknek életképességük volt az életképesség nélküli betegekhez képest.3 az LVEF javulása hasonló volt a revaszkularizációval rendelkező életképességű betegeknél, mint a gyógyszeres kezeléssel kezelt betegeknél.3
Megjegyzendő, hogy a STICH-vizsgálatban az életképességet dobutamin stressz echokardiográfiával vagy SPECT-tel értékelték. Ugyanakkor, hasonlóan az F-18-fluorodeoxiglükóz pozitron emissziós tomográfiás képalkotással segített betegek kezelése súlyos bal kamrai diszfunkció és feltételezett koszorúér-betegség (PARR-2) vizsgálatban az eredmény nem volt eltérő, amikor az életképességet pet-n keresztül értékelték CABG-n átesett ischaemiás cardiomyopathiában szenvedő betegeknél.17 nem világos, hogy az életképesség miért nem befolyásolta a revaszkularizáció utáni eredményt az orvosi terápiához képest; ennek oka lehet az orvosi terápia sikeres végrehajtása, vagy egyszerűen tükrözheti a döntéshozatal összetettségét azokban a betegekben, ahol számos más kockázati tényező játszik szerepet a képalkotó modalitáson túl.
következtetés
bár a miokardiális életképességről nem kimutatták, hogy hatással lenne a túlélésre a revaszkularizáció után, még mindig szerepet játszhat a klinikai gyakorlatban, különösen magas kockázatú, előrehaladott korú vagy jelentős társbetegségben szenvedő betegeknél, ahol a revaszkularizáció kockázata és előnyei továbbra sem tisztázottak. Ischaemiás kardiomiopátiában szenvedő betegeknél a mellkasi sebészek magas Társasága (STS) kockázati pontszám, a kezelés összetett, és a jövőbeni vizsgálatoknak folytatniuk kell ezt a korszakot multimodalitási képalkotással, figyelembe véve számos más kockázati tényezőt, amelyek befolyásolhatják az eredményt.
a mögöttes társbetegségeket és a beteg jellemzőit gondosan felül kell vizsgálni az életképesség értékeléséhez megfelelő képalkotó módszer kiválasztása érdekében. A PET vagy CMR használatáról szóló döntés betegenként történik. A PET-t akkor kell figyelembe venni, ha egy nagy miokardiális infarktusban szenvedő betegnek, amelyet alternatív képalkotó technikával életképtelennek tartottak, továbbra is refrakter vagy tünetkorlátozó anginája van, szívelégtelenség exacerbációk a maximális orvosi kezelés ellenére, kamrai aritmiák, vagy jelentős koszorúér-szűkülete van, ahol még egy kis életképes sziget is szívizom valószínűleg a revaszkularizáció javára dönt. Veseelégtelenségben vagy beültetett szívberendezésben szenvedő betegeknél a PET előnyös. Rosszul kontrollált cukorbetegségben, súlyosan csökkent ejekciós frakcióban, 6 mm-nél kisebb végdiasztolés Vastagsággal vagy többszörös koszorúér-eloszlásban szenvedő betegeknél kerülni kell a PET-t, míg súlyos klausztrofóbiában, veseelégtelenségben vagy beültetett eszközök jelenlétében a CMR alkalmazása korlátozott és/vagy ellenjavallt.
- Murray CJ, Lopez AD. A halálozás és a fogyatékosság ok szerinti alternatív előrejelzései. 1990-2020: a betegség globális terhe tanulmány. Lancet 1997; 349: 1498-504.
- Bonow RO, Maurer G, Lee KL és mtsai. Myocardialis életképesség és túlélés ischaemiás bal kamrai diszfunkcióban. N Engl J Med 2011; 364: 1617-25.
- Panza JA, Ellis AM, Al-Khalidi HR, et al. Myocardialis életképesség és hosszú távú eredmények ischaemiás cardiomyopathiában. N Engl J Med 2019; 381: 739-8.
- Garcia MJ, Kwong RY, Scherrer-Crosbie M és mtsai. A technika állása: képalkotás a szívizom életképességéért: az American Heart Association tudományos nyilatkozata. Circ Cardiovasc Képalkotás 2020; Július 13:.
- Bolli R. a miokardiális kábítás alapvető és klinikai vonatkozásai. Prog Cardiovasc Dis 1998;40:477-516.
- Ryan MJ, Perera D. a hibernáló szívizom azonosítása és kezelése: mi új és mi marad ismeretlen? Curr Szív Nem Rep 2018; 15: 214-23.
- Canty JM Jr, Suzuki G, Banas MD, Verheyen F, Borgers M, Fallavollita JA. Hibernáló szívizom: krónikusan alkalmazkodik az ischaemiához, de érzékeny a hirtelen halálra. Circ Res 2004;94:1142-9.
- Hernandez-Pampaloni M, Peral V, Carreras JL, Sanchez-Harguindey L, Vilacosta I. A dobutaminra adott kétfázisú válasz a bal kamrai diszfunkció javulását jósolja a revaszkularizáció után: korreláció a pozitron emisszióval és a rest-redistribution 201tl tomográfiákkal. Int J Cardiovasc Képalkotás 2003;19:519-28.
- Porter TR, Mulvagh SL, Abdelmoneim SS, et al. Az ultrahangos fokozó szerek klinikai alkalmazása az echokardiográfiában: 2018 American Society of Echokardiography guidelines frissítés. J Am Soc Echokardiogr 2018; 31: 241-74.
- Piwnica-férgek D, Chiu ML, Kronauge JF. A 201tl és 99mTc-SESTAMIBI eltérő kinetikája tenyésztett chick ventricularis myocytákban ATP depléció során. Circulation 1992; 85: 1531-41.
- Berman DS, Kiat H, Van Train KF, Friedman J, Garcia EV, Maddahi J. a SPECT összehasonlítása technécium-99m és tallium-201 és PET szerekkel a myocardialis perfúzió és életképesség értékeléséhez. Am J Cardiol 1990; 66: 72E-79E.
- l 6100 l. A szívizom életképességének vizsgálata a koszorúér revaszkularizációjának irányítására. Interv Cardiol Clin 2018; 7:355-65.
- Kim RJ, Wu E, Rafael A és mtsai. Kontraszt-fokozott mágneses rezonancia képalkotás alkalmazása a reverzibilis myocardialis diszfunkció azonosítására. N Engl J Med 2000; 343:1445-53.
- Bax JJ, Poldermans D, Elhendy A, Boersma E, Rahimtoola SH. Érzékenység, specificitás és prediktív pontossága különböző noninvazív technikák kimutatására hibernáló szívizom. Curr Probl Cardiol 2001;26:147-186.
- Bax JJ, van der Wall EE, Harbinson M. radionuklid technikák a myocardialis életképesség és a hibernáció értékelésére. Szív 2004; 90: v26-v33.
- Pagano D, Bonser R, Townend J, Ordoubadi F, Lorenzoni R, Camici P. A dobutamin echokardiográfia és a pozitron emissziós tomográfia prediktív értéke a hibernáló myocardium azonosításában postischaemiás szívelégtelenségben szenvedő betegeknél. Szív 1998; 79: 281-8.
- Beanlands RSB, Nichol G, Huszti E, et al. F-18-fluorodeoxiglükóz pozitron emissziós tomográfia súlyos bal kamrai diszfunkcióban és feltételezett coronaria betegségben szenvedő betegek képalkotással segített kezelése: randomizált, kontrollos vizsgálat (PARR-2). J Am Coll Cardiol 2007;50:2002-12.
klinikai témák: Aritmiák és klinikai EP, cukorbetegség és kardiometabolikus betegség, dyslipidaemia, szívelégtelenség és cardiomyopathiák, noninvazív képalkotás, beültethető eszközök, SCD/ventricularis arrhythmiák, pitvarfibrilláció/supraventricularis arrhythmiák, Lipid anyagcsere, új szerek, komputertomográfia, echokardiográfia/ultrahang, nukleáris képalkotás
kulcsszavak: Dyslipidemias, Apoptosis, Arrhythmias, Cardiac, Biological Phenomena, Atherosclerosis, Ammonia, Cardiomyopathies, Cicatrix, Cardiovascular Diseases, Constriction, Pathologic, Contrast Media, Coronary Vessels, Death, Sudden, Cardiac, Dobutamine, Down-Regulation, Echocardiography, Echocardiography, Stress, Extracellular Space, Fatty Acids, Fluorodeoxyglucose F18, Gadolinium, Glucose, Hemodynamics, Hibernation, Hospitalization, Inflammation, Insulin Resistance, Myocardial Ischemia, Ischemia, Multimodal Imaging, Myocardium, Myocytes, Cardiac, Plaque, Atherosclerotic, Positron-Emission Tomography, Prognózis, kálium, életminőség, az eredmények reprodukálhatósága, kockázati tényezők, rubídium, rubídium radioizotópok, Stroke térfogat, technécium, tallium, trombózis, tomográfia, emisszió-számított, kamrai funkció, bal
< vissza a listákhoz