Quick tar
- trots brist på longitudinella resultatfördelar i de tidigare kliniska prövningarna kan myocardial viability assessment fortfarande spela en roll på en personlig nivå av kliniskt beslutsfattande för högriskpatienter med måttlig och avancerad kranskärlssjukdom.
- tidigare studier använde huvudsakligen enfotonemissionsberäknad tomografi (SPECT) och dobutamin stressekokardiografi för livskraft bedömning; emerging technology ger högre känslighet med kontrastförstärkt kardiovaskulär magnetisk resonans (CMR) och högre specificitet med dobutaminspänning CMR för att förutsäga förbättring av regional funktion efter revaskularisering.
- kliniska markörer såsom ischemiska symtom samt närvaro av målkärl för revaskularisering bör noggrant granskas före utvärdering för icke-invasiv livsbedömning.
Inledning
kardiovaskulär sjukdom är fortfarande den främsta orsaken till dödlighet och sjuklighet i den moderna eran av medicin.1 Det har gjorts många forskningsstudier med fokus på kardiovaskulära förebyggande strategier för att förhindra framtida akuta ischemiska händelser genom att bromsa utvecklingen av ateroskleros och minska risken för plackstörning och överlagrad trombos. Myocardial viability assessment har varit i slutet av detta spektrum och utformades för att välja patienter med ischemisk kardiomyopati som kan uppvisa reversering av myokarddysfunktionen.
akuta och återkommande ischemiska händelser leder till ischemisk kardiomyopati som är associerad med återkommande sjukhusvistelser, dålig livskvalitet och ökad dödlighet. Denna process kan vändas om vi kan identifiera dysfunktionella men livskraftiga myokardceller hos patienter med ischemisk kardiomyopati. Under de senaste decennierna har förmågan att upptäcka livskraftigt myokardium ökat med ny teknik inom kardiovaskulär avbildning och fortsätter att utvecklas när tekniken växer.
trots alla framsteg när det gäller att upptäcka livskraftiga myokardceller har viability imaging inte visat sig ha någon inverkan på kliniskt resultat efter revaskularisering i prospektiva studier.2,3 denna artikel kommer att granska den nuvarande rollen för icke-invasiv bedömning av myokardiell livskraft i klinisk praxis och sammanfatta de viktigaste punkterna i det nyligen publicerade toppmoderna dokumentet om avbildning för myokardiell livskraft dokument från American Heart Association (aha).4
irreversibel och reversibel ischemisk skada: Fibros, viloläge och bedövning
med kronisk minskning av hjärtblodflödet leder aktivering av flera vägar till inflammation, apoptos, nekros och så småningom en ärrvävnadsbildning. När blodtillförseln är markant minskad men inte helt störd kan myokardiell skada vara av mindre grad; myokardceller skulle fortfarande vara livskraftiga och potentiellt återfå sin funktion efter att blodtillförseln återställts. Det finns två olika typer av myokardiell dysfunktion vid ischemi: viloläge och bedövning.
ihållande minskad blodtillförsel kan inducera nedreglering av myokardfunktionen i viloläge, medan bedövning avser nedsatt kontraktil funktion trots normalt viloflöde.5,6 oavsett blodflödet minskar koronarflödesreserven i båda typerna av myokardiell dysfunktion, vilket så småningom leder till strukturella och funktionella förändringar i myokardiet genom att orsaka efterfrågan ischemi. Det kan också finnas en minskning av koronarflödesreserven hos patienter utan epikardiell flödesbegränsande sjukdom men med svår mikrovaskulär dysfunktion. Fibroser eller infarkt vävnad har skadliga effekter på myokardiell ombyggnad och är förknippad med negativa resultat; men även viloläge kan fungera som ett substrat för hjärtarytmier och öka risken för plötslig hjärtdöd.7
icke-invasiva avbildningsmetoder för att bedöma myokardiell livskraft
bedömning av vänster ventrikulär storlek och funktion med ekokardiografi är ett viktigt verktyg för utvärdering av myokardiell livskraft. Medan väggförtunning inte är tillförlitlig för att uppskatta reversibel myokardfunktion, är ökad vänster ventrikulär storlek associerad med dålig prognos efter revaskularisering.
Dobutaminstressekokardiografi har använts i stor utsträckning för att bedöma myokardiell kontraktilitet och livskraft. Med kontinuerlig dobutamininfusion ökar myokardiell perfusion initialt tillsammans med kontraktilitet, men när dobutamindosen ökar kan blodflödet inte eskaleras ytterligare, vilket resulterar i minskad kontraktilitet. Detta fenomen är känt som bifasisk reaktion som förutsäger återhämtning av myokardfunktionen efter revaskularisering.8
Speckle tracking ekokardiografi är en annan framväxande modalitet som exakt kan uppskatta vänster ventrikulär återhämtning efter hjärtinfarkt. Ekokontrastperfusionsavbildningen som upptäcker hjärtmikrovaskulär integritet är också lovande; på grund av mycket variabel Reproducerbarhet kommer dess användbarhet för lönsamhetsbedömning att kräva ytterligare undersökningar.9
under de senaste decennierna har enfotonemissionsberäknad tomografi (SPECT) och positronemissionstomografi (PET) använts i stor utsträckning för att bedöma myokardiell livskraft. Att vara en kaliumanalog kan tallium användas för att detektera myokardiell cellmembranintegritet via Na/K ATPas-kanaler, där livskraftiga celler visar fördröjt upptag jämfört med vilande avbildning.10 till skillnad från tallium visar teknetium-baserad SPECT inte en försenad distribution.11 under de senaste decennierna har tallium sällan använts på grund av ökad joniserande strålning jämfört med teknetium.
en annan vanlig kärnbildningsmetod för att bedöma myokardiell vitalitet är hjärt PET. I ett hälsosamt myokardium härrör energikällan från fettsyror, medan det i ett ischemiskt tillstånd skiftar mot glukosbaserad metabolism. 18F-fluorodeoxyglukos (18F-FDG) kan upptäcka detta skifte i livskraftigt myokardium. Den vanliga bedömningen för livskraft består av vila avbildning och metabolisk avbildning med 18F-FDG. I områden utan vilande perfusion som visas med N-13 ammoniak eller rubidium-82 indikerar närvaron av 18F-FDG-upptag livskraft. Jämfört med SPECT har PET högre rumslig upplösning, lägre strålning och har bättre dämpningskorrigering. Observera att hos patienter med insulinresistens kan FDG-uppdatering i normalt område förbli mindre än för ischemiska eller viloläge. En begränsning av PET är variationen i FDG-uppdatering, som kan påverkas av hjärtutgång, hjärtsvikt, grad av ischemi och sympatisk aktivitet.12
när ischemi kvarstår uppträder myokardiell apoptos och nekros, vilket resulterar i ökat extracellulärt utrymme som kan detekteras genom sen gadoliniumförbättring (LGE) kardiovaskulär magnetisk resonans (CMR). Hos patienter med kronisk ischemisk kardiomyopati transmural utsträckning lge förutspår reversibilitet myokardial kontraktion efter framgångsrik revaskularisering.13 medan minimal LGE (<25%) i ett dysfunktionellt myokardsegment indikerar en hög sannolikhet för återhämtning, är risken för återhämtning i en >50% LGE av transmural infarkt mycket låg.13 i detta avseende tillhandahåller LGE CMR användbar information för att vägleda revaskularisering. I segment med borderline lge-engagemang (25-50%) är återhämtningsprognosen med LGE inte tillräckligt stark.13
bland alla studier ovan har lge-procentandelen väggtjocklek den högsta känsligheten (95%) och dobutaminstress CMR har den högsta specificiteten (91%) för att förutsäga regional myokardiell återhämtning, medan dobutaminstressekokardiografi visade god förutsägbarhet med 80% känslighet och 78% specificitet. SPECT (87%, och 83% för tallium och teknetium imaging respektive), och PET (92%) baserade kärnviabilitetsstudier har god känslighet; specificiteten har dock varit lägre jämfört med andra metoder (<70%).14-16
rollen av Viability Imaging i klinisk praxis
författarna till den senaste tekniken: Imaging for Viability4 föreslog två olika algoritmer hos patienter med kronisk (Figur 1) och subakut (Figur 2) ischemisk kardiomyopati. För båda algoritmerna är det viktigt att bedöma flera faktorer som inkluderar symtomen, målkärl för revaskularisering och graden av ombyggnad.
Figur 1
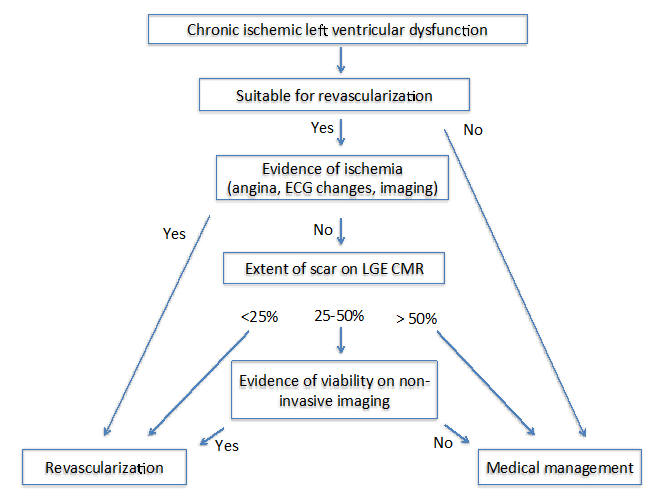
Figur 1

Figur 2
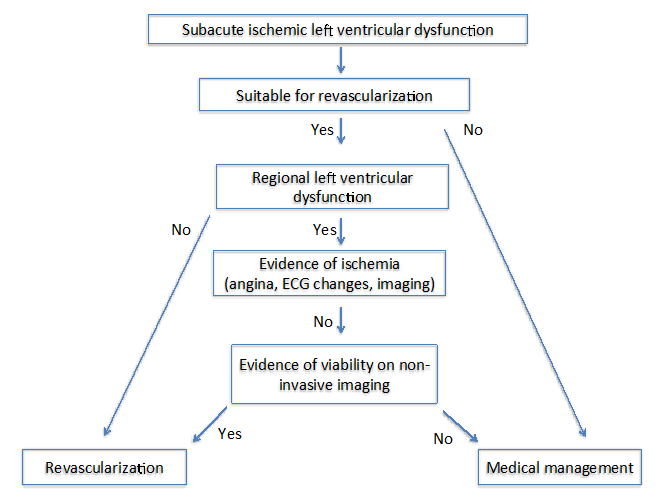
Figur 2

konsekvensbedömningen av livskraft på resultat
subgruppsanalysen av studien Surgical Treatment for Ischemic Heart Failure (STICH) visade att patienter med livskraft hade lägre långtidsdödlighet jämfört med patienter som inte visade några tecken på livskraft, och det var signifikant förbättring av vänster ventrikulär ejektionsfraktion (LVEF) hos patienter som visade myokardiell livskraft, oavsett behandlingsstrategi. Resultatet efter koronar bypass-ympning (CABG) var emellertid inte signifikant annorlunda hos patienter som hade livskraft jämfört med patienter utan livskraft.3 förbättringen av LVEF var likartad hos patienter med livskraft som hade revaskularisering jämfört med patienter som behandlades med medicinsk behandling.3
Observera att i STICH-studien bedömdes livskraften med dobutamin stressekokardiografi eller SPECT. Men på samma sätt i F-18-fluorodeoxyglukos positron emission tomography imaging-assisterad hantering av patienter med svår vänsterkammardysfunktion och misstänkt kranskärlssjukdom (PARR-2) studie var resultatet inte annorlunda när lönsamheten bedömdes via PET hos patienter med ischemisk kardiomyopati som genomgår CABG.17 Det är oklart varför lönsamheten inte hade någon inverkan på resultatet efter revaskularisering jämfört med medicinsk terapi; det kan bero på framgångsrikt genomförande av medicinsk terapi, eller det kan helt enkelt återspegla komplexiteten i beslutsfattandet hos dessa patienter, där flera andra riskfaktorer spelar en roll utöver en bildmodalitet.
slutsats
även om myokardiell livskraft inte har visat sig påverka överlevnaden efter revaskularisering, kan den fortfarande spela en roll i klinisk praxis, särskilt hos högriskpatienter med avancerad ålder eller med signifikanta komorbiditeter där risker och fördelar med revaskulariseringen förblir oklara. Hos patienter med ischemisk kardiomyopati och ett högt samhälle av Thoraxkirurger (STS) riskpoäng är hanteringen komplex och framtida försök bör fortsätta att utforska denna era med multimodalitetsavbildning med hänsyn till flera andra riskfaktorer som kan påverka resultatet.
underliggande komorbiditeter och patientegenskaper bör noggrant granskas för att välja rätt bildmodalitet för bedömning av livskraft. Beslutet att använda PET eller CMR fattas på patient-till-patient-basis. PET bör övervägas när en patient med ett stort hjärtinfarkt som ansågs vara icke-livskraftigt med en alternativ bildteknik fortsätter att ha eldfast eller symtombegränsande angina, hjärtsvikt exacerbationer trots maximal medicinsk behandling, ventrikulära arytmier eller har en signifikant kranskärlsstenos där närvaron av till och med en liten ö av livskraftigt myokardium sannolikt kommer att svänga beslutet till förmån för revaskularisering. Hos patienter med njursvikt eller en implanterad hjärtanordning föredras PET. Hos patienter med dåligt kontrollerad diabetes, kraftigt reducerad ejektionsfraktion, med slutdiastolisk tjocklek mindre än 6 mm, eller de med stenos i multipel kranskärlsfördelning, bör PET undvikas vid svår klaustrofobi, njursvikt eller närvaro av implanterade enheter, användningen av CMR är begränsad och/eller kontraindicerad.
- Murray CJ, Lopez annons. Alternativa prognoser för dödlighet och funktionshinder efter orsak. 1990-2020: global sjukdomsstudie. Lancet 1997; 349: 1498-504.
- Bonow RO, Maurer G, Lee KL, et al. Myokardiell livskraft och överlevnad vid ischemisk vänster ventrikulär dysfunktion. N Engl J Med 2011; 364: 1617-25.
- Panza JA, Ellis AM, Al-Khalidi HR, et al. Myokardiell livskraft och långsiktiga resultat vid ischemisk kardiomyopati. N Engl J Med 2019; 381: 739-8.
- Garcia MJ, Kwong RY, Scherrer-Crosbie M, et al. State of the art: imaging för myokardiell livskraft: ett vetenskapligt uttalande från American Heart Association. Circ Cardiovasc Imaging 2020; Jul 13:.
- Bolli R. grundläggande och kliniska aspekter av myokardiell bedövning. Prog Cardiovasc Dis 1998; 40: 477-516.
- Ryan MJ, Perera D. identifiera och hantera viloläge: vad är nytt och vad som fortfarande är okänt? Curr Hjärta Misslyckas Rep 2018; 15: 214-23.
- Canty JM Jr, Suzuki G, Banas MD, Verheyen F, Borgers M, Fallavollita JA. Hibernating myokardium: kroniskt anpassad till ischemi men sårbar för plötslig död. Circ Res 2004; 94: 1142-9.
- Hernandez-Pampaloni M, Peral V, Carreras JL, Sanchez-Harguindey L, Vilacosta I. bifasiskt svar på dobutamin förutsäger förbättring av vänster ventrikulär dysfunktion efter revaskularisering: korrelation med positronemission och rest-omfördelning 201tl tomografier. Int J Cardiovasc Avbildning 2003; 19: 519-28.
- Porter TR, Mulvagh SL, Abdelmoneim SS, et al. Kliniska tillämpningar av ultraljudsförbättrande medel i ekokardiografi: 2018 American Society of Echocardiography guidelines update. J Am Soc Ekokardiogr 2018; 31: 241-74.
- Piwnica-maskar D, Chiu ML, Kronauge JF. Divergerande kinetik av 201tl och 99mTc-SESTAMIBI i odlade kycklingventrikulära myocyter under ATP-utarmning. Cirkulation 1992; 85: 1531-41.
- Berman DS, Kiat H, Van Train KF, Friedman J, Garcia EV, Maddahi J. jämförelse av SPECT med teknetium-99m-medel och tallium-201 och PET för bedömning av myokardiell perfusion och livskraft. Am J Cardiol 1990; 66: 72E-79E.
- l IC, Kramer CM. Myocardial viability testing för att styra koronar revaskularisering. Interv Cardiol Clin 2018; 7: 355-65.
- Kim RJ, Wu E, Rafael A, et al. Användningen av kontrastförstärkt magnetisk resonansavbildning för att identifiera reversibel myokardiell dysfunktion. N Engl J Med 2000; 343: 1445-53.
- Bax JJ, Poldermans D, Elhendy A, Boersma E, Rahimtoola SH. Känslighet, specificitet och prediktiv noggrannhet hos olika icke-invasiva tekniker för att detektera viloläge myokardium. Curr Probl Cardiol 2001; 26: 147-186.
- Bax JJ, van der Wall EE, Harbinson M. Radionuklidtekniker för bedömning av myokardiell livskraft och viloläge. Hjärta 2004; 90: v26-v33.
- Pagano D, Bonser R, Townend J, Ordoubadi F, Lorenzoni R, Camici P. Prediktivt värde av dobutaminekokardiografi och positronemissionstomografi vid identifiering av viloläge hos patienter med postischemisk hjärtsvikt. Hjärta 1998; 79: 281-8.
- Beanlands RSB, Nichol G, Huszti E, et al. F-18-fluorodeoxyglukos positron emission tomography imaging-assisterad hantering av patienter med svår vänster ventrikulär dysfunktion och misstänkt kranskärlssjukdom: en randomiserad, kontrollerad studie (PARR-2). J Am Coll Cardiol 2007; 50: 2002-12.
kliniska ämnen: Arytmier och klinisk EP, Diabetes och kardiometabolisk sjukdom, dyslipidemi, hjärtsvikt och kardiomyopatier, icke-invasiv Avbildning, implanterbara enheter, SCD/ventrikulära arytmier, förmaksflimmer/supraventrikulära arytmier, lipidmetabolism, nya medel, datortomografi, ekokardiografi/ultraljud, kärnbildning
nyckelord: Dyslipidemias, Apoptosis, Arrhythmias, Cardiac, Biological Phenomena, Atherosclerosis, Ammonia, Cardiomyopathies, Cicatrix, Cardiovascular Diseases, Constriction, Pathologic, Contrast Media, Coronary Vessels, Death, Sudden, Cardiac, Dobutamine, Down-Regulation, Echocardiography, Echocardiography, Stress, Extracellular Space, Fatty Acids, Fluorodeoxyglucose F18, Gadolinium, Glucose, Hemodynamics, Hibernation, Hospitalization, Inflammation, Insulin Resistance, Myocardial Ischemia, Ischemia, Multimodal Imaging, Myocardium, Myocytes, Cardiac, Plaque, Atherosclerotic, Positron-Emission Tomography, Prognos, kalium, livskvalitet, reproducerbarhet av resultat, riskfaktorer, Rubidium, Rubidium radioisotoper, strokevolym, Teknetium, tallium, trombos, tomografi, Emissionsberäknad, ventrikulär funktion, vänster
< tillbaka till listor