Rychlé Bere
- i Přes nedostatek podélné výsledek přínos v předchozích klinických studiích, infarkt založeno hodnocení životaschopnosti, může stále hrát roli na individuální úrovni klinické rozhodování u vysoce rizikových pacientů se středně těžkou a pokročilou ischemickou chorobou srdeční.
- Předchozích studiích používá hlavně jednofotonová emisní počítačová tomografie (SPECT) a dobutamin stres echokardiografie pro posouzení životaschopnosti; rozvíjející se technologie poskytuje vyšší citlivost s kontrastní zvýšenou kardiovaskulární magnetická rezonance (CMR) a vyšší specificitu s dobutamin stres CMR předpovědět zlepšení regionální funkce po revaskularizaci.
- klinické markery, jako jsou ischemické příznaky a přítomnost cílových cév pro revaskularizaci, by měly být pečlivě přezkoumány před hodnocením neinvazivního hodnocení životaschopnosti.
Úvod
kardiovaskulární onemocnění zůstává hlavní příčinou úmrtnosti a morbidity v moderní době medicíny.1 Tam byly četné studie se zaměřením na kardiovaskulární prevence strategie pomoci zabránit budoucím akutní ischemické příhody tím, že zpomaluje progresi aterosklerózy a snížit riziko narušení plaku a překrývá trombózy. Hodnocení životaschopnosti myokardu bylo na konci tohoto spektra a bylo navrženo k výběru pacientů s ischemickou kardiomyopatií, kteří mohou vykazovat zvrácení dysfunkce myokardu.
akutní a opakující se ischemické příhody vedou k ischemické kardiomyopatii, která je spojena s opakovanými hospitalizacemi, špatnou kvalitou života a zvýšenou úmrtností. Tento proces lze zvrátit, pokud dokážeme identifikovat dysfunkční, ale životaschopné buňky myokardu u pacientů s ischemickou kardiomyopatií. V posledních desetiletích se schopnost detekovat životaschopný myokard zvýšila s nově vznikajícími technologiemi v kardiovaskulárním zobrazování a stále se vyvíjí, jak technologie roste.
navzdory všem pokrokům v detekci životaschopných buněk myokardu nebylo prokázáno, že by zobrazování životaschopnosti mělo vliv na klinický výsledek po revaskularizaci v prospektivních studiích.2,3 Tohoto článku posoudí současnou úlohu neinvazivní infarktu životaschopnosti hodnocení v klinické praxi a shrnout klíčové body v nedávno zveřejněné nejmodernější dokument o zobrazování na infarkt životaschopnost dokument z American Heart Association (AHA).4
nevratné a reverzibilní ischemické poškození: Fibróza, Hibernace a Omráčení
S chronickou snížení infarktu prokrvení, aktivace několik cest vede k zánětu, apoptóza, nekróza a nakonec jizva tkáně formace. Když dodávka krve je výrazně snížena, ale ne zcela narušen, poškození myokardu může být v menší míře; buňky myokardu by být stále životaschopné a potenciálně získat jejich funkce po dodávku krve obnoven. Existují dva různé typy dysfunkce myokardu v prostředí ischémie: hibernace a omráčení.
trvale snížený přísun krve může vyvolat down-regulaci funkce myokardu v hibernaci, zatímco omráčení se týká zhoršené kontraktilní funkce navzdory normálnímu klidovému toku.5,6 bez ohledu na průtok krve je u obou typů dysfunkce myokardu snížena rezerva koronárního toku, což nakonec vede ke strukturálním a funkčním změnám v myokardu tím, že způsobuje ischemii poptávky. Může také dojít ke snížení rezervy koronárního toku u pacientů bez onemocnění omezujícího epikardiální tok, ale se závažnou mikrovaskulární dysfunkcí. Fibroses nebo poškozen tkáně má škodlivé účinky na myokardiální remodelaci a je spojena s negativními výsledky; nicméně, i hibernující myokard může sloužit jako substrát pro srdeční arytmie a zvýšit riziko náhlé srdeční smrti.7
neinvazivní zobrazovací modality k posouzení životaschopnosti myokardu
posouzení velikosti a funkce levé komory pomocí echokardiografie je nezbytným nástrojem pro hodnocení životaschopnosti myokardu. Zatímco ztenčení stěny není spolehlivé pro odhad reverzibilní funkce myokardu, zvýšená velikost levé komory je spojena se špatnou prognózou po revaskularizaci.
dobutaminová stresová echokardiografie byla široce používána k posouzení kontraktility a životaschopnosti myokardu. Při kontinuální infuzi dobutaminu se perfúze myokardu zpočátku zvyšuje spolu s kontraktilitou, ale se zvyšující se dávkou dobutaminu nelze průtok krve dále zvyšovat, což má za následek sníženou kontraktilitu. Tento jev je známý jako dvoufázová reakce, která předpovídá obnovení funkce myokardu po revaskularizaci.8
echokardiografie sledování skvrn je další vznikající modalita, která dokáže přesně odhadnout zotavení levé komory po infarktu myokardu. Echo kontrastní perfuzní zobrazování, které detekuje srdeční mikrovaskulární integritu, je také slibné; nicméně, kvůli vysoce variabilní reprodukovatelnosti, jeho užitečnost pro posouzení životaschopnosti bude vyžadovat další vyšetřování.9
V posledních desetiletích, jednofotonová emisní počítačová tomografie (SPECT) a pozitronová emisní tomografie (PET) byly široce využity k posouzení infarktu životaschopnost. Být analog draslíku, thalia mohou být použity k detekci myokardiální buňky membránové integrity pomocí Na/K Atpázy programy, kde životaschopné buňky prokázat zpoždění příjmu oproti klidové zobrazení.10 Na rozdíl od Thalia, SPECT na bázi technecia neprokazuje zpožděnou distribuci.11 V posledních desetiletích se thallium zřídka používá kvůli zvýšení ionizujícího záření ve srovnání s techneciem.
další běžně používanou jadernou zobrazovací modalitou pro hodnocení vitality myokardu je srdeční PET. Ve zdravém myokardu pochází zdroj energie z mastných kyselin, zatímco v ischemickém stavu se posune směrem k metabolismu založenému na glukóze. 18F-fluorodeoxyglukóza (18F-FDG) může detekovat tento posun v životaschopném myokardu. Obvyklé hodnocení životaschopnosti spočívá v zobrazování rest a metabolickém zobrazování pomocí 18F-FDG. V oblastech bez klidové perfúze, jak je znázorněno S N-13 amoniakem nebo rubidiem-82, přítomnost absorpce 18F-FDG naznačuje životaschopnost. Ve srovnání se SPECTEM má PET vyšší prostorové rozlišení, nižší záření a lepší korekci útlumu. Je třeba poznamenat, že u pacientů s inzulínovou rezistencí může aktualizace FDG v normální oblasti zůstat nižší než u ischemických nebo hibernačních oblastí. Jedním z omezení PET je variabilita aktualizace FDG, která může být ovlivněna srdečním výdejem, srdečním selháním, stupněm ischémie a sympatickou aktivitou.12
Pokud ischemie přetrvává, infarkt apoptóza a nekróza se vyskytuje, což vede ke zvýšení extracelulární prostor, který může být detekován pozdě zvýšení gadolinia (LGE) kardiovaskulární magnetická rezonance (CMR). U pacientů s chronickou ischemickou kardiomyopatií transmurální rozsah LGE předpovídá reverzibilitu kontrakce myokardu po úspěšné revaskularizaci.13 Zatímco minimální LGE (<25%) v dysfunkční infarktu segmentu ukazuje na vysokou pravděpodobnost využití, možnost využití v >50% LGE z transmurální infarkt je velmi nízká.13 V tomto ohledu poskytuje LGE CMR užitečné informace pro vedení revaskularizace. V segmentech s hraničním zapojením LGE (25-50%) není predikce zotavení s LGE dostatečně silná.13
Mezi všechny studie výše, LGE procento tloušťky stěny má nejvyšší citlivost (95%), a dobutamin stres CMR má nejvyšší specificitu (91%) předvídat regionální infarktu oživení, zatímco dobutamin stres echokardiografie prokázala dobrou předvídatelnost s 80% citlivost a 78% specifičnost. SPECT (87% a 83% pro thallium a technecium imaging, respektive), a PET (92%) na bázi jaderné životaschopnost studií mají dobrou citlivost; nicméně, specifičnost byla nižší ve srovnání s jinými způsoby (<70%).14-16
Role Životaschopnost Zobrazovací metody v Klinické Praxi
autoři nejmodernější: Imaging pro Viability4 navrhuje dva různé algoritmy u pacientů s chronickou (Obrázek 1) a subakutní (viz Obrázek 2) ischemická kardiomyopatie. Pro oba algoritmy je důležité posoudit několik faktorů, které zahrnují příznaky, cílové cévy pro revaskularizaci a stupeň remodelace.
Obrázek 1
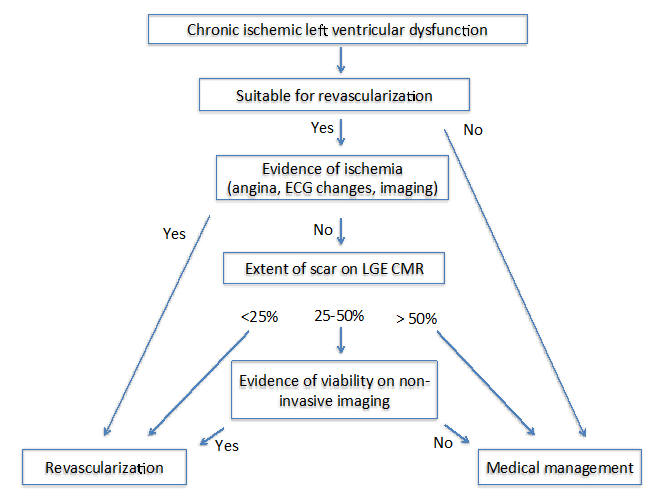
Obrázek 1

Obrázek 2
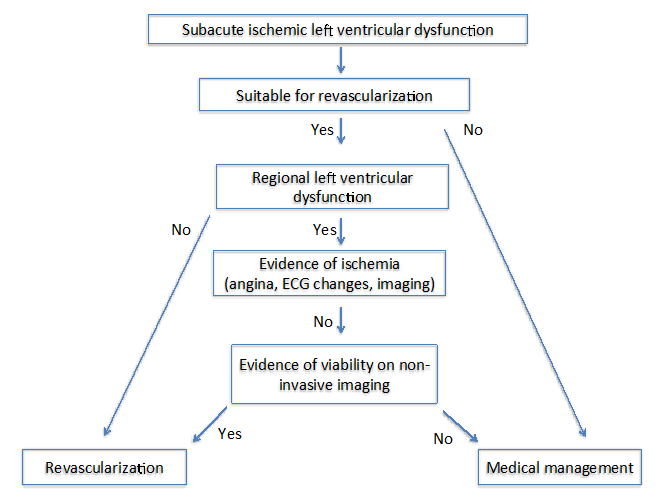
Obrázek 2

Dopad na Posouzení Životaschopnosti na Výsledek
podskupina analýza Chirurgická Léčba Ischemické Srdeční Selhání (STICH) studie ukázala, že u pacientů s životaschopnost měl nižší dlouhodobé úmrtnosti ve srovnání s pacienty, kteří nevykazují žádné známky životaschopnosti, a tam bylo významné zlepšení ejekční frakce levé komory (LVEF) u pacientů, kteří prokázali životaschopnost myokardu, a to bez ohledu na strategii léčby. Výsledek po bypassu koronární arterie (CABG) se však významně nelišil u pacientů, kteří měli životaschopnost, ve srovnání s pacienty bez životaschopnosti.3 zlepšení LVEF bylo podobné u pacientů s životaschopností, kteří měli revaskularizaci ve srovnání s pacienty léčenými lékařskou terapií.3
je třeba poznamenat, že ve studii STICH byla životaschopnost hodnocena pomocí dobutaminové stresové echokardiografie nebo SPECT. Nicméně, podobně jako v F-18-fluorodeoxyglukózy pozitronová emisní tomografie, imaging-asistované řízení pacientů s těžkou dysfunkcí levé komory a podezření na koronární onemocnění (PARR-2) soud, výsledek nebyl jiný, když životaschopnost byla hodnocena pomocí PET u pacientů s ischemickou kardiomyopatií podstupujících CABG.17 není jasné, proč životaschopnost neměla vliv na výsledek po revaskularizaci ve srovnání s lékařskou terapií; to by mohlo být vzhledem k úspěšné provádění lékařské terapii, nebo to může jednoduše odrážet složitost rozhodování v těch pacientů, kde několik dalších rizik, faktory hrají roli mimo zobrazovací modality.
Závěr
i když infarktu životaschopnost nebylo prokázáno, že mají vliv na přežívání po revaskularizaci, pořád to může hrát roli v klinické praxi, zejména ve vysoce rizikových pacientů s pokročilým věku nebo s významnými komorbiditami, kde rizika a přínosy revaskularizace zůstávají nejasné. U pacientů s ischemickou kardiomyopatií a high Society of Thoracic Surgeons (STS) skóre rizika, řízení je složité a budoucí studie by měly i nadále objevovat tato éra s multimodality imaging v úvahu několik dalších faktorů, které by mohly mít vliv na výsledek.
základní komorbidity a charakteristiky pacientů by měly být pečlivě přezkoumány, aby se zvolil správný zobrazovací způsob pro posouzení životaschopnosti. Rozhodnutí o použití PET nebo CMR se provádí na základě pacienta k pacientovi. PET by měly být považovány, když pacient s velkým infarktem myokardu, který byl myšlenka být neživotaschopnými o alternativní zobrazovací technika i nadále žáruvzdorné nebo příznakem omezení angina pectoris, exacerbace srdečního selhání i přes maximální lékařskou terapii, komorové arytmie, nebo má významný koronární tepně stenóza, kde přítomnost i malého ostrova životaschopného myokardu bude pravděpodobně swing rozhodnutí ve prospěch revaskularizace. U pacientů se selháním ledvin nebo implantovaným srdečním zařízením je preferován PET. U pacientů se špatně kontrolovaným diabetes, výrazně snížená ejekční frakce, end diastolický tloušťce menší než 6 mm, nebo ty, se stenózou ve více koronární tepny distribuce, domácího MAZLÍČKA, je třeba se vyhnout, zatímco v těžkých klaustrofobií, selhání ledvin nebo přítomnost implantovaného zařízení, použití CMR je omezený a/nebo kontraindikována.
- Murray CJ, Lopez ad. Alternativní projekce úmrtnosti a postižení podle příčiny. 1990-2020: studie globální zátěže nemocí. Lancet 1997; 349: 1498-504.
- Bonow RO, Maurer G, Lee KL, et al. Životaschopnost a přežití myokardu při ischemické dysfunkci levé komory. N Engl J Med 2011;364: 1617-25.
- Panza JA, Ellis AM, Al-Khalidi HR, et al. Životaschopnost myokardu a dlouhodobé výsledky ischemické kardiomyopatie. N Engl J Med 2019; 381: 739-8.
- Garcia MJ, Kwong RY, Scherrer-Crosbie M, et al. Stav techniky: zobrazování životaschopnosti myokardu: vědecké prohlášení Americké asociace srdce. Circ Cardiovasc Imaging 2020;13. Července:.
- Bolli R. základní a klinické aspekty omráčení myokardu. Prog Cardiovasc Dis 1998; 40: 477-516.
- Ryan MJ, Perera D. identifikace a správa hibernačního myokardu: co je nového a co zůstává neznámé? Curr Heart Fail Rep 2018; 15: 214-23.
- Canty JM Jr, Suzuki G, Banas MD, Verheyen F, Borgers M, Fallavollita JA. Hibernační myokard: chronicky přizpůsobený ischemii, ale náchylný k náhlé smrti. Circ Res 2004; 94: 1142-9.
- Hernandez-Pampaloni M, Peral V, Carreras JL, Sanchez-Harguindey L, Vilacosta I. Dvoufázová odpověď na dobutamin předpovídá zlepšení dysfunkce levé komory po revaskularizaci: korelace s pozitronovou emisí a rest-redistribuce 201Tl tomografií. Int J Cardiovasc Imaging 2003; 19: 519-28.
- Porter TR, Mulvagh SL, Abdelmoneim SS, et al. Klinické aplikace ultrazvukových zesilujících látek v echokardiografii: 2018 aktualizace pokynů Americké společnosti pro echokardiografii. J Am Soc Echocardiogr 2018; 31: 241-74.
- Piwnica-Worms D, Chiu ML, Kronauge JF. Divergentní kinetika 201Tl a 99mTc-SESTAMIBI v kultivovaných myocytech kuřat během deplece ATP. Oběh 1992; 85: 1531-41.
- Berman DS, Kiat H, Van Vlak KF, Friedman J., Garcia EV, Maddahi J. Srovnání SPECT pomocí technecia-99m agenti a thallium-201 a PET pro hodnocení myokardiální perfuze a životaschopnost. Am J Cardiol 1990; 66: 72E-79E.
- Löffler AI, Kramer CM. Testování životaschopnosti myokardu k vedení koronární revaskularizace. Interv Cardiol Clin 2018; 7: 355-65.
- Kim RJ, Wu E, Rafael A et al. Použití kontrastní magnetické rezonance k identifikaci reverzibilní dysfunkce myokardu. N Engl J Med 2000;343: 1445-53.
- Bax JJ, Poldermans D, Elhendy A, Boersma E, Rahimtoola SH. Citlivost, specificita a prediktivní přesnost různých neinvazivních technik pro detekci hibernačního myokardu. Curr Probl Cardiol 2001; 26: 147-186.
- Bax JJ, van der Wall EE, Harbinson m. radionuklidové techniky pro hodnocení životaschopnosti myokardu a hibernace. Srdce 2004; 90: v26-v33.
- Pagano D, Bonser R, Townend J, Ordoubadi F, Lorenzoni R, Camici P. Prediktivní hodnota dobutamin echokardiografie a pozitronové emisní tomografie při identifikaci hibernující myokard u pacientů s postischaemic selhání srdce. Srdce 1998; 79: 281-8.
- Beanlands RSB, Nichol G, Huszti E, et al. F-18-fluorodeoxyglukóza pozitronová emisní tomografie léčba pacientů s těžkou dysfunkcí levé komory a podezřením na koronární onemocnění: randomizovaná kontrolovaná studie (PARR-2). J Am Sb Cardiol 2007; 50: 2002-12.
klinická témata: Arytmií a Klinické EP, Diabetes a Kardiometabolického Onemocnění, Dyslipidemie, Srdeční Selhání a Kardiomyopatie, Neinvazivní Zobrazovací, Implantabilní Zařízení, SCD/Komorové Arytmie, Fibrilace Síní/Supraventrikulární Arytmie, poruchy Metabolismu Lipidů, Román Agenti, Počítačová Tomografie, Echokardiografie/Ultrazvuk, Nukleární Imaging
Klíčová slova: Dyslipidemias, Apoptosis, Arrhythmias, Cardiac, Biological Phenomena, Atherosclerosis, Ammonia, Cardiomyopathies, Cicatrix, Cardiovascular Diseases, Constriction, Pathologic, Contrast Media, Coronary Vessels, Death, Sudden, Cardiac, Dobutamine, Down-Regulation, Echocardiography, Echocardiography, Stress, Extracellular Space, Fatty Acids, Fluorodeoxyglucose F18, Gadolinium, Glucose, Hemodynamics, Hibernation, Hospitalization, Inflammation, Insulin Resistance, Myocardial Ischemia, Ischemia, Multimodal Imaging, Myocardium, Myocytes, Cardiac, Plaque, Atherosclerotic, Positron-Emission Tomography, Prognóza, Draslík, Kvalita Života, Reprodukovatelnost Výsledků, Rizikových Faktorů, Rubidium, Rubidium Radioizotopů, tepový Objem, Technecium, Thalium, Trombóza, Tomografie, měření Emisí-Počítačová, Ventrikulární Funkce, Vlevo
< Zpět na Výpisy