Quick Takes
- Til tross for mangel på longitudinell utfallsfordel i de tidligere kliniske studiene, kan myokardial levedyktighetsvurdering fortsatt spille en rolle på et personlig nivå av klinisk beslutningstaking for høyrisikopasienter med moderat og avansert koronararteriesykdom.
- Tidligere studier brukte hovedsakelig single-photon emission computertomografi (SPECT) og dobutamin stress ekkokardiografi for levedyktighet vurdering; ny teknologi gir høyere følsomhet med kontrastforsterket kardiovaskulær magnetisk resonans (cmr) og høyere spesifisitet med dobutaminstress CMR for å forutsi forbedring av regional funksjon etter revaskularisering.
- Kliniske markører som iskemiske symptomer samt tilstedeværelse av målkar for revaskularisering bør vurderes nøye før evaluering for ikke-invasiv levedyktighetsvurdering.
Innledning
Kardiovaskulær sykdom er fortsatt den ledende årsaken til dødelighet og sykelighet i den moderne æra av medisin.1 det har vært mange forskningsstudier som fokuserer på kardiovaskulære forebyggingsstrategier for å forhindre fremtidige akutte iskemiske hendelser ved å bremse utviklingen av aterosklerose og redusere risikoen for plakkforstyrrelser og overliggende trombose. Hjerteinfarkt levedyktighet vurdering har vært på slutten av dette spekteret, og er designet for å velge pasienter med iskemisk kardiomyopati som kan vise reversering av myokardial dysfunksjon.
Akutte og tilbakevendende iskemiske hendelser fører til iskemisk kardiomyopati som er forbundet med gjentatte sykehusinnleggelser, dårlig livskvalitet og økt dødelighet. Denne prosessen kan reverseres hvis vi kan identifisere dysfunksjonelle, men levedyktige myokardceller hos pasienter med iskemisk kardiomyopati. I løpet av de siste tiårene har evnen til å oppdage levedyktig myokard økt med nye teknologier innen kardiovaskulær bildebehandling og fortsetter å utvikle seg etter hvert som teknologien vokser.
Til tross for alle fremskritt i å oppdage levedyktige myokardceller, har levedyktighetsavbildning ikke vist seg å ha innvirkning på klinisk utfall etter revaskularisering i prospektive studier.2,3 denne artikkelen vil gjennomgå den nåværende rollen som ikke-invasiv hjerteinfarkt levedyktighet vurdering i klinisk praksis og oppsummere de viktigste punktene i den nylig publiserte state of the art document on imaging for hjerteinfarkt levedyktighet dokument Fra American Heart Association (Aha).4
Irreversibel Og Reversibel Iskemisk Skade: Fibrose, Dvalemodus Og Bedøving
med kronisk reduksjon i myokardisk blodstrøm fører aktivering av flere veier til betennelse, apoptose, nekrose og til slutt en arrvevdannelse. Når blodtilførselen er markert redusert, men ikke helt forstyrret, kan myokardskaden være av mindre grad; myokardceller vil fortsatt være levedyktige og potensielt gjenvinne sin funksjon etter at blodtilførselen er gjenopprettet. Det er to forskjellige typer myokarddysfunksjon i innstillingen av iskemi: dvalemodus og bedøvelse.
Vedvarende redusert blodtilførsel kan indusere nedregulering av myokardfunksjonen i dvalemodus, mens bedøvelse refererer til nedsatt kontraktil funksjon til tross for normal hvilestrøm.5,6 uavhengig av blodstrømmen reduseres koronar strømningsreserven i begge typer myokarddysfunksjon, noe som til slutt fører til strukturelle og funksjonelle endringer i myokardiet ved å forårsake etterspørsel iskemi. Det kan også være en reduksjon i koronar strømningsreserve hos pasienter uten epikardial strømningsbegrensende sykdom, men med alvorlig mikrovaskulær dysfunksjon. Fibroses eller infarkt vev har skadelige effekter på myokardial remodeling og er forbundet med uønskede utfall; men selv dvalemodus myokard kan tjene som substrat for hjertearytmier og øke risikoen for plutselig hjertedød.7
Ikke-invasive Imaging Modaliteter For Å Vurdere Myokardial Levedyktighet
Vurdering av venstre ventrikulær størrelse og funksjon med ekkokardiografi er et viktig verktøy for evaluering av myokardial levedyktighet. Mens veggtynning ikke er pålitelig for å estimere reversibel myokardfunksjon, er økt venstre ventrikulær størrelse forbundet med dårlig prognose etter revaskularisering.
Dobutamin stress ekkokardiografi har blitt mye brukt til å vurdere myokardial kontraktilitet og levedyktighet. Ved kontinuerlig dobutamininfusjon øker myokardial perfusjon i utgangspunktet sammen med kontraktilitet, men etter hvert som dobutamindosen øker, kan ikke blodstrømmen økes ytterligere, noe som resulterer i redusert kontraktilitet. Dette fenomenet er kjent som bifasisk reaksjon som forutsier utvinning av myokardfunksjonen etter revaskularisering.8
Speckle sporing ekkokardiografi er en annen fremvoksende modalitet som nøyaktig kan estimere venstre ventrikulær utvinning etter hjerteinfarkt. Echo contrast perfusjon imaging som oppdager hjerte mikrovaskulær integritet er også lovende; men på grunn av svært variabel reproduserbarhet, sin nytte for levedyktighet vurdering vil kreve ytterligere undersøkelser.9
i de siste tiårene har single-photon emission computed tomography (SPECT) og positron emission tomography (PET) blitt mye brukt til å vurdere myokardial levedyktighet. Å være en kaliumanalog, kan thallium brukes til å oppdage myokardcellemembranintegritet via Na / K atpase-kanaler, hvor levedyktige celler viser forsinket opptak i forhold til hvileavbildning.10 I Motsetning til tallium viser ikke technetium-basert SPECT en forsinket distribusjon.11 i de siste tiårene har tallium sjelden blitt brukt på grunn av økning i ioniserende stråling sammenlignet med technetium.
En annen vanlig nuclear imaging modalitet for å vurdere myokardial vitalitet er cardiac PET. I et sunt myokardium kommer energikilden fra fettsyrer, mens den i en iskemisk tilstand skifter mot glukosebasert metabolisme. 18f-fluorodeoksyglukose (18F-FDG) kan oppdage dette skiftet i levedyktig myokard. Den vanlige vurderingen for levedyktighet består av rest imaging og metabolic imaging MED 18F-FDG. I områder uten hvileperfusjon som vist Med n-13 ammoniakk eller rubidium-82, indikerer tilstedeværelse AV 18f-FDG opptak levedyktighet. SAMMENLIGNET MED SPECT, PET har høyere romlig oppløsning, lavere stråling, og har bedre demping korreksjon. Hos pasienter med insulinresistens kan FDG-oppdatering i normalt område forbli mindre enn for iskemiske eller dvalemodus. EN begrensning AV PET er variasjonen AV fdg update, som kan påvirkes av hjerteutgang, hjertesvikt, grad av iskemi og sympatisk aktivitet.12
når iskemi vedvarer, oppstår myokardial apoptose og nekrose, noe som resulterer i økt ekstracellulært rom som kan detekteres ved sen gadoliniumforbedring (LGE) kardiovaskulær magnetisk resonans (CMR). Hos pasienter med kronisk iskemisk kardiomyopati transmural grad lge spår reversibilitet av myokardial sammentrekning etter vellykket revaskularisering.13 mens minimal LGE (< 25%) i et dysfunksjonelt myokardsegment indikerer en høy sannsynlighet for utvinning, er sjansen for utvinning i en >50% LGE av transmural infarkt svært lav.13 I den forbindelse gir LGE CMR nyttig informasjon for å veilede revaskularisering. I segmenter med borderline lge engasjement (25-50%), er utvinning prediksjon MED LGE ikke sterk nok.13
BLANT alle studiene ovenfor har LGE-prosentandel av veggtykkelse den høyeste følsomheten (95%), og dobutaminstress CMR har den høyeste spesifisiteten (91%) for å forutsi regional myokardutvinning, mens dobutaminstressekkokardiografi viste god forutsigbarhet med 80% følsomhet og 78% spesifisitet. SPECT (87%, og 83% for henholdsvis thallium og technetium imaging), OG PET (92%) baserte nukleare levedyktighetsstudier har god følsomhet; spesifisiteten har imidlertid vært lavere sammenlignet med andre modaliteter (<70%).14-16
Rollen Av Levedyktighet Bildebehandling I Klinisk Praksis
forfatterne Av State Of The Art: Imaging For Viability4 foreslått to forskjellige algoritmer hos pasienter med kronisk (Figur 1) og subakutt (Figur 2) iskemisk kardiomyopati. For begge algoritmer er det viktig å vurdere flere faktorer som inkluderer symptomene, målkarene for revaskularisering og graden av remodeling.
Figur 1
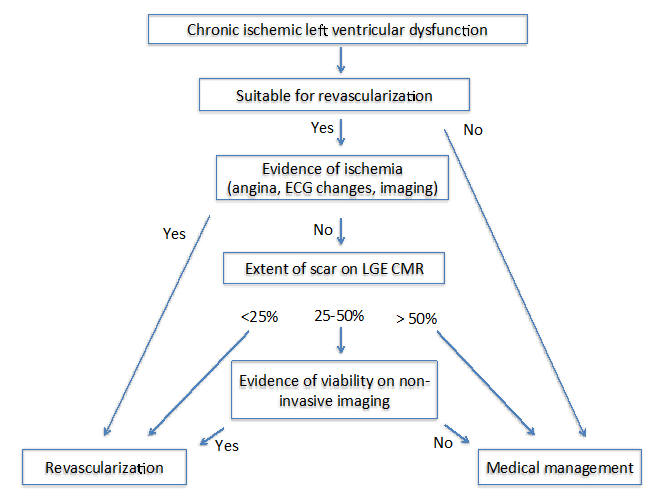
Figur 1

Figur 2
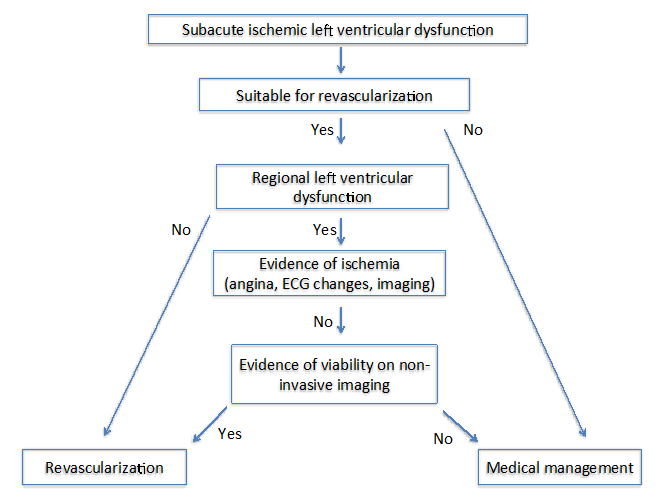
Figur 2

Virkningen På Levedyktighetsvurdering På Utfall
undergruppeanalysen av Studien Kirurgisk behandling for Iskemisk Hjertesvikt (STICH) viste at pasienter med levedyktighet hadde lavere langtids dødelighet sammenlignet med pasienter som ikke viste tegn på levedyktighet, og det var signifikant forbedring i VENSTRE ventrikulær ejeksjonsfraksjon (LVEF) hos pasienter som viste myokardial levedyktighet, uavhengig av behandlingsstrategi. Utfallet etter koronar bypass pode (CABG) var imidlertid ikke signifikant forskjellig hos pasienter som hadde levedyktighet sammenlignet med pasienter uten levedyktighet.3 forbedringen AV LVEF var lik hos pasienter med levedyktighet som hadde revaskularisering sammenlignet med pasienter som ble behandlet med medisinsk behandling.3
I STICH-studien ble levedyktigheten vurdert med dobutaminstressekkokardiografi eller SPECT. På samme måte i F-18-fluorodeoksyglukose positronemisjonstomografi bildebehandlingsassistert behandling av pasienter med alvorlig venstre ventrikulær dysfunksjon og mistenkt koronar sykdom (PARR-2) studien, var utfallet imidlertid ikke annerledes når levedyktighet ble vurdert VIA PET hos pasienter med iskemisk kardiomyopati som gjennomgikk CABG.17 det er uklart hvorfor levedyktighet ikke påvirket utfallet etter revaskularisering sammenlignet med medisinsk behandling; det kan skyldes vellykket implementering av medisinsk terapi, eller det kan bare gjenspeile kompleksiteten i beslutningsprosessen hos de pasientene, der flere andre risikofaktorer spiller en rolle utover en bildemodalitet.
Konklusjon
selv om myokardial levedyktighet ikke har vist seg å ha effekt på overlevelse etter revaskularisering, kan det fortsatt spille en rolle i klinisk praksis, spesielt hos høyrisikopasienter med høy alder eller med signifikante komorbiditeter der risiko og nytte av revaskulariseringen forblir uklar. Hos pasienter med iskemisk kardiomyopati og EN HØY Samfunn Av Thoracic Surgeons (STS) risiko score, er ledelsen kompleks og fremtidige studier bør fortsette å utforske denne epoken med multimodalitet avbildning i betraktning av flere andre risikofaktorer som kan påvirke utfallet.
Underliggende komorbiditeter og pasientkarakteristika bør vurderes nøye for å velge riktig avbildningsmodalitet for vurdering av levedyktighet. Beslutningen om Å bruke PET eller CMR er gjort på pasient-til-pasient basis. PET bør vurderes når en pasient med et stort hjerteinfarkt som ble antatt å være ikke-levedyktig ved en alternativ bildeteknikk fortsetter å ha ildfast eller symptombegrensende angina, hjertesvikt eksacerbasjoner til tross for maksimal medisinsk terapi, ventrikulære arytmier, eller har en betydelig koronar stenose hvor tilstedeværelsen av enda en liten øy av levedyktig myokardium vil trolig svinge avgjørelsen til fordel for revaskularisering. HOS pasienter med nyresvikt eller implantert hjerteanordning foretrekkes PET. HOS pasienter med dårlig kontrollert diabetes, alvorlig redusert ejeksjonsfraksjon, med endediastolisk tykkelse mindre enn 6 mm, eller de med stenose i flere koronararterie distribusjon, BØR PET unngås mens i alvorlig klaustrofobi, nyresvikt eller tilstedeværelse av implanterte enheter, er BRUK AV CMR begrenset og / eller kontraindisert.
- Murray CJ, Lopez ANNONSE. Alternative fremskrivninger av dødelighet og uførhet etter årsak. 1990-2020: global sykdomsbyrde studie. Lancet 1997;349:1498-504.
- Bonow RO, Maurer G, Lee KL, Et al. Myokardial levedyktighet og overlevelse i iskemisk venstre ventrikulær dysfunksjon. N Engl J Med 2011; 364:1617-25.
- Panza JA, Ellis AM, Al-Khalidi HR, et al. Myokardial levedyktighet og langsiktige resultater i iskemisk kardiomyopati. N Engl J Med 2019; 381: 739-8.
- Garcia MJ, Kwong RY, Scherrer-Crosbie M, Et al. State of the art: imaging for hjerteinfarkt levedyktighet: en vitenskapelig uttalelse Fra American Heart Association. Circ Cardiovasc Bildebehandling 2020; Juli 13:.
- Bolle R. Grunnleggende og kliniske aspekter ved hjerteinfarkt. Prog Cardiovasc Dis 1998; 40: 477-516.
- Ryan MJ, Perera D. Identifisere og administrere hibernating myokardium: hva er nytt og hva som fortsatt er ukjent? Curr Hjerte Mislykkes Rep 2018;15: 214-23.
- Canty Jm Jr., Suzuki G, Banas MD, Verheyen F, Borgers M, Fallavollita JA. Hibernating myokardium: kronisk tilpasset iskemi, men sårbar for plutselig død. Circ Res 2004; 94: 1142-9.
- Hernandez-Pampaloni M, Peral V, Carreras JL, Sanchez-Harguindey L, Vilacosta I. Bifasisk respons på dobutamin forutsier forbedring av venstre ventrikulær dysfunksjon etter revaskularisering: korrelasjon med positron utslipp og rest-omfordeling 201tl tomografier. Int J Cardiovasc Bildebehandling 2003; 19: 519-28.
- Porter TR, Mulvagh SL, Abdelmoneim SS, Et al. Kliniske anvendelser av ultralydforsterkende midler i ekkokardiografi: 2018 American Society Of Echocardiography guidelines update. J Am Soc Ekkokardiogr 2018;31: 241-74.
- Piwnica-Ormer D, Chiu ML, Kronauge JF. Divergerende kinetikk av 201Tl og 99mTc-SESTAMIBI i kultiverte chick ventrikulære myocytter under ATP uttømming. Sirkulasjon 1992; 85: 1531-41.
- Berman DS, Kiat H, Van Train KF, Friedman J, Garcia EV, Maddahi J. Sammenligning AV SPECT ved hjelp av technetium-99m-agenter og thallium – 201 og PET for vurdering av myokardial perfusjon og levedyktighet. Er J Cardiol 1990;66: 72e-79E.
- Lö AI, Kramer CM. Hjerteinfarkt levedyktighet testing for å veilede koronar revaskularisering. Interv Cardiol Clin 2018;7:355-65.
- Kim RJ, Wu E, Rafael A, et al. Bruken av kontrastforsterket magnetisk resonansavbildning for å identifisere reversibel myokarddysfunksjon. N Engl J Med 2000; 343:1445-53.
- Bax JJ, Poldermans D, Elhendy A, Boersma E, Rahimtoola SH. Sensitivitet, spesifisitet og prediktiv nøyaktighet av ulike ikke-invasive teknikker for å oppdage dvalemodus. Curr Probl Cardiol 2001; 26:147-186.
- Bax JJ, van Der Wall EE, Harbinson M. Radionuklide teknikker for vurdering av myokardial levedyktighet og dvalemodus. Hjerte 2004; 90: v26-v33.
- Pagano D, Bonser R, Townend J, Ordoubadi F, Lorenzoni R, Camici P. Prediktiv verdi av dobutamin ekkokardiografi og positronemisjonstomografi ved identifisering av infarkt i dvale hos pasienter med postiskemisk hjertesvikt. Hjerte 1998; 79: 281-8.
- Beanlands RSB, Nichol G, Huszti E, Et al. F-18-fluorodeoksyglukose positronemisjonstomografi bildeassistert behandling av pasienter med alvorlig venstre ventrikulær dysfunksjon og mistanke om koronar sykdom: en randomisert, kontrollert studie (PARR-2). J Am Coll Cardiol 2007;50: 2002-12.
Kliniske Emner: Arytmier OG Klinisk EP, Diabetes Og Kardiometabolsk Sykdom, Dyslipidemi, Hjertesvikt Og Kardiomyopatier, Ikke-Invasiv Bildebehandling, Implanterbare Enheter, SCD/Ventrikulære Arytmier, Atrieflimmer/Supraventrikulære Arytmier, Lipidmetabolisme, Nye Midler, Computertomografi, Ekkokardiografi/Ultralyd, Nukleær Bildebehandling
Nøkkelord: Dyslipidemias, Apoptosis, Arrhythmias, Cardiac, Biological Phenomena, Atherosclerosis, Ammonia, Cardiomyopathies, Cicatrix, Cardiovascular Diseases, Constriction, Pathologic, Contrast Media, Coronary Vessels, Death, Sudden, Cardiac, Dobutamine, Down-Regulation, Echocardiography, Echocardiography, Stress, Extracellular Space, Fatty Acids, Fluorodeoxyglucose F18, Gadolinium, Glucose, Hemodynamics, Hibernation, Hospitalization, Inflammation, Insulin Resistance, Myocardial Ischemia, Ischemia, Multimodal Imaging, Myocardium, Myocytes, Cardiac, Plaque, Atherosclerotic, Positron-Emission Tomography, Prognose, Kalium, Livskvalitet, Reproduserbarhet Av Resultater, Risikofaktorer, Rubidium, Rubidiumradioisotoper, Slagvolum, Technetium, Tallium, Trombose, Tomografi, Emisjonsberegning, Ventrikulær Funksjon, Venstre
< Tilbake til Oppføringer