Hurtig tager
- på trods af manglende langsgående resultatfordel i de tidligere kliniske forsøg, myocardial levedygtighed vurdering kan stadig spille en rolle på et personligt niveau af klinisk beslutningstagning for højrisikopatienter med moderat og avanceret koronararteriesygdom.
- tidligere forsøg brugte hovedsageligt computertomografi med enkelt fotonemission (SPECT) og dobutamin stress ekkokardiografi til levedygtighedsvurdering; emerging technology giver højere følsomhed med kontrastforbedret kardiovaskulær magnetisk resonans (CMR) og højere specificitet med dobutamin stress CMR for at forudsige forbedring af regional funktion efter revaskularisering.
- kliniske markører såsom iskæmiske symptomer samt tilstedeværelse af målkar til revaskularisering bør gennemgås omhyggeligt inden evaluering for ikke-invasiv levedygtighedsvurdering.
introduktion
kardiovaskulær sygdom er fortsat den førende årsag til dødelighed og sygelighed i den moderne æra af medicin.1 der har været adskillige forskningsundersøgelser med fokus på hjerte-kar-forebyggelsesstrategier for at hjælpe med at forhindre fremtidige akutte iskæmiske hændelser ved at bremse udviklingen af åreforkalkning og reducere risikoen for plakforstyrrelse og overlejret trombose. Vurdering af Myocardial levedygtighed har været i slutningen af dette spektrum og var designet til at vælge patienter med iskæmisk kardiomyopati, der kan udvise reversering af myocardial dysfunktion.
akutte og tilbagevendende iskæmiske hændelser fører til iskæmisk kardiomyopati, der er forbundet med tilbagevendende indlæggelser, dårlig livskvalitet og øget dødelighed. Denne proces kan vendes, hvis vi kan identificere dysfunktionelle, men levedygtige myokardceller hos patienter med iskæmisk kardiomyopati. I løbet af de sidste årtier er evnen til at opdage levedygtigt myokardium steget med nye teknologier inden for kardiovaskulær billeddannelse og fortsætter med at udvikle sig, når teknologien vokser.
på trods af alle fremskridt med at detektere levedygtige myokardceller har levedygtighedsafbildning ikke vist sig at have indflydelse på det kliniske resultat efter revaskularisering i prospektive undersøgelser.2,3 denne artikel vil gennemgå den aktuelle rolle som ikke-invasiv vurdering af myokardiel levedygtighed i den kliniske praksis og opsummere nøglepunkterne i det nyligt offentliggjorte avancerede dokument om billeddannelse for myokardiel levedygtighedsdokument fra American Heart Association (aha).4
irreversibel og reversibel iskæmisk skade: Fibrose, dvaletilstand og bedøvelse
med kronisk reduktion i myocardial blodgennemstrømning fører aktivering af de forskellige veje til betændelse, apoptose, nekrose og til sidst dannelse af arvæv. Når blodforsyningen er markant nedsat, men ikke fuldstændigt forstyrret, kan myokardskaden være af mindre grad; myokardceller ville stadig være levedygtige og potentielt genvinde deres funktion, efter at blodforsyningen blev genoprettet. Der er to forskellige typer af myokardisk dysfunktion i forbindelse med iskæmi: dvaletilstand og bedøvelse.
vedvarende nedsat blodforsyning kan inducere nedregulering af myokardiefunktionen i dvaletilstand, mens bedøvelse henviser til nedsat kontraktil funktion på trods af normal hvilestrøm.5,6 uanset blodgennemstrømningen reduceres koronarstrømningsreserve i begge typer myokardisk dysfunktion, hvilket til sidst fører til strukturelle og funktionelle ændringer i myokardiet ved at forårsage efterspørgsel iskæmi. Der kan også være et fald i koronar strømningsreserve hos patienter uden epikardiel strømningsbegrænsende sygdom, men med svær mikrovaskulær dysfunktion. Fibroser eller infarkt væv har skadelige virkninger på myocardial remodeling og er forbundet med negative resultater; dog kan selv dvale myokardium tjene som et substrat for hjertearytmier og øge risikoen for pludselig hjertedød.7
ikke-invasive billeddannelsesmetoder til vurdering af myokardiel levedygtighed
vurdering af venstre ventrikulær størrelse og funktion med ekkokardiografi er et vigtigt redskab til evaluering af myokardiel levedygtighed. Mens vægfortynding ikke er pålidelig til at estimere reversibel myokardiefunktion, er øget venstre ventrikulær størrelse forbundet med dårlig prognose efter revaskularisering.
Dobutamin stress ekkokardiografi har været meget anvendt til at vurdere myokardial kontraktilitet og levedygtighed. Ved kontinuerlig dobutamininfusion øges myokardieperfusion oprindeligt sammen med kontraktilitet, men når dobutamindosis øges, kan blodgennemstrømningen ikke eskaleres yderligere, hvilket resulterer i reduceret kontraktilitet. Dette fænomen er kendt som bifasisk reaktion, der forudsiger genopretning af myokardiefunktionen efter revaskularisering.8
Speckle tracking ekkokardiografi er en anden nye modalitet, der nøjagtigt kan estimere venstre ventrikulær genopretning efter myokardieinfarkt. Ekko-kontrast perfusionsbilleddannelse, der registrerer hjerte-mikrovaskulær integritet, er også lovende; på grund af meget variabel Reproducerbarhed vil dets anvendelighed til levedygtighedsvurdering imidlertid kræve yderligere undersøgelser.9
i de seneste årtier er computertomografi med enkeltfotonemission (SPECT) og positronemissionstomografi (PET) blevet brugt i vid udstrækning til at vurdere myokardiel levedygtighed. At være en kaliumanalog kan thallium bruges til at detektere myocardial cellemembranintegritet via Na/K ATPase-kanaler, hvor levedygtige celler demonstrerer forsinket optagelse sammenlignet med hvilende billeddannelse.10 i modsætning til thallium viser technetium-baseret SPECT ikke en forsinket distribution.11 i de seneste årtier er thallium sjældent blevet brugt på grund af stigning i ioniserende stråling sammenlignet med technetium.
en anden almindeligt anvendt nuklear billeddannelsesmodalitet til vurdering af myokardial vitalitet er cardiac PET. I et sundt myokardium stammer energikilden fra fedtsyrer, mens den i en iskæmisk tilstand skifter mod glukosebaseret metabolisme. 18F-fluoroksglukose (18F-FDG) kan detektere dette skift i levedygtigt myokardium. Den sædvanlige vurdering for levedygtighed består af hvilebilleddannelse og metabolisk billeddannelse med 18F-FDG. I områder uden hvileperfusion som vist med N-13 ammoniak eller rubidium-82 indikerer tilstedeværelsen af 18F-FDG optagelse levedygtighed. Sammenlignet med SPECT har PET højere rumlig opløsning, lavere stråling og har bedre dæmpningskorrektion. Bemærk, at hos patienter med insulinresistens kan FDG-opdatering i det normale område forblive mindre end for iskæmiske eller dvaleområder. En begrænsning af PET er variabiliteten af FDG-opdatering, som kan påvirkes af hjerteproduktion, hjertesvigt, grad af iskæmi og sympatisk aktivitet.12
når iskæmi vedvarer, forekommer myokardisk apoptose og nekrose, hvilket resulterer i øget ekstracellulært rum, der kan detekteres ved sen gadoliniumforbedring (LGE) kardiovaskulær magnetisk resonans (CMR). Hos patienter med kronisk iskæmisk kardiomyopati forudsiger den transmurale udstrækning af LGE reversibiliteten af myokardiekontraktionen efter vellykket revaskularisering.13 mens minimal LGE (<25%) i et dysfunktionelt myokardiesegment indikerer en høj sandsynlighed for bedring, er chancen for bedring i en >50% lge af transmural infarkt meget lav.13 i den henseende giver lge CMR nyttige oplysninger til vejledning om revaskularisering. I segmenter med grænse lge-involvering (25-50%) er genoprettelsesforudsigelsen med LGE ikke stærk nok.13
blandt alle ovennævnte undersøgelser har LGE-procentdelen af vægtykkelse den højeste følsomhed (95%), og dobutamin stress CMR har den højeste specificitet (91%) til at forudsige regional myocardial genopretning, mens dobutamin stress ekkokardiografi viste god forudsigelighed med 80% følsomhed og 78% specificitet. SPECT (87% og 83% for henholdsvis thallium-og technetium-billeddannelse) og PET (92%) – baserede nukleare levedygtighedsundersøgelser har god følsomhed; specificiteten har dog været lavere sammenlignet med andre modaliteter (<70%).14-16
rollen som Levedygtighedsbilleddannelse i klinisk praksis
forfatterne af den nyeste teknik: billeddannelse for Levedygtighed4 foreslog to forskellige algoritmer hos patienter med kronisk (Figur 1) og subakut (figur 2) iskæmisk kardiomyopati. For begge algoritmer er det vigtigt at vurdere flere faktorer, der inkluderer symptomerne, målskibe til revaskularisering og graden af ombygning.
Figur 1
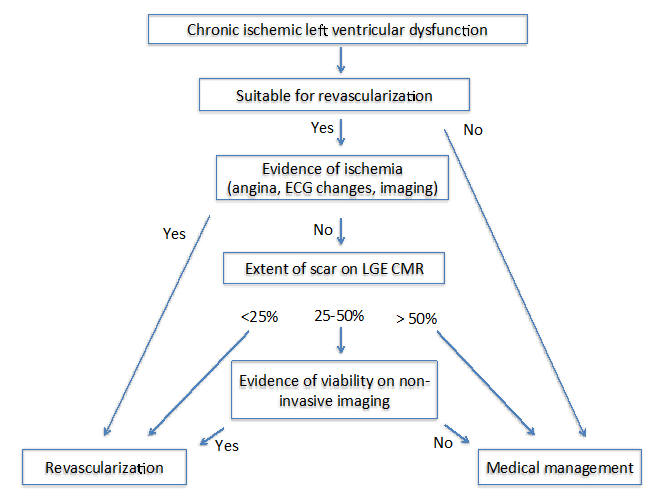
Figur 1

figur 2
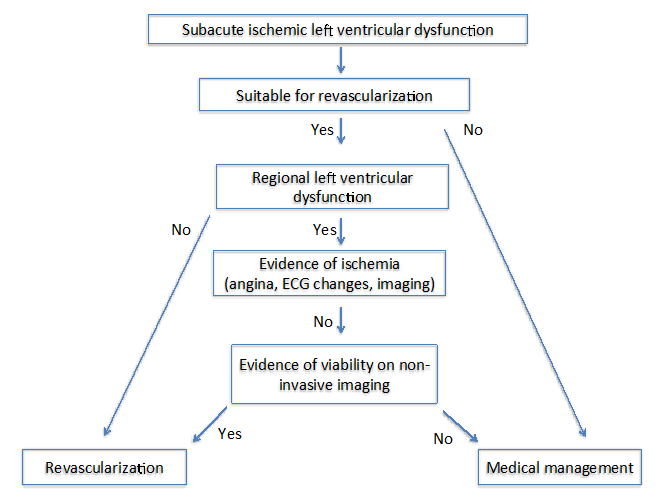
figur 2

virkningen på Levedygtighedsvurdering på resultatet
undergruppeanalysen af kirurgisk behandling for iskæmisk hjertesvigt (STICH)-studiet viste, at patienter med levedygtighed havde lavere langtidsdødelighed sammenlignet med patienter, der ikke viste tegn på levedygtighed, og der var signifikant forbedring i venstre ventrikulær ejektionsfraktion (LVEF) hos patienter, der demonstrerede myokardiel levedygtighed, uanset behandlingsstrategien. Resultatet efter koronar bypass-podning (CABG) var imidlertid ikke signifikant forskelligt hos patienter, der havde levedygtighed sammenlignet med patienter uden levedygtighed.3 forbedringen af LVEF var den samme hos patienter med levedygtighed, der havde revaskularisering sammenlignet med patienter, der blev behandlet med medicinsk behandling.3
bemærk, i STICH-forsøget blev levedygtigheden vurderet med dobutamin stress ekkokardiografi eller SPECT. På samme måde i F-18-fluordeoksglucosepositronemissionstomografi billedbehandlingsassisteret behandling af patienter med svær venstre ventrikulær dysfunktion og mistænkt koronar sygdom (PARR-2) forsøg var resultatet ikke anderledes, når levedygtigheden blev vurderet via PET hos patienter med iskæmisk kardiomyopati, der gennemgik CABG.17 Det er uklart, hvorfor levedygtighed ikke havde indflydelse på resultatet efter revaskularisering sammenlignet med medicinsk terapi; det kan skyldes en vellykket implementering af medicinsk terapi, eller det kan simpelthen afspejle kompleksiteten i beslutningsprocessen hos disse patienter, hvor flere andre risikofaktorer spiller en rolle ud over en billeddannelsesmodalitet.
konklusion
selvom myokardiel levedygtighed ikke har vist sig at have en effekt på overlevelse efter revaskularisering, kan det stadig spille en rolle i klinisk praksis, især hos højrisikopatienter med fremskreden alder eller med signifikante comorbiditeter, hvor risici og fordele ved revaskulariseringen forbliver uklare. Hos patienter med iskæmisk kardiomyopati og en High Society of Thoracic Surgeons (STS) risikoscore, ledelsen er kompleks, og fremtidige forsøg bør fortsætte med at udforske denne æra med multimodalitetsbilleddannelse under hensyntagen til flere andre risikofaktorer, der kan påvirke resultatet.
underliggende comorbiditeter og patientkarakteristika bør gennemgås omhyggeligt for at vælge den rigtige billeddannelsesmodalitet til levedygtighedsvurdering. Beslutningen om at bruge PET eller CMR træffes på patient-til-patient basis. PET bør overvejes, når en patient med et stort myokardieinfarkt, der blev anset for at være ikke-levedygtigt ved en alternativ billeddannelsesteknik, fortsat har ildfast eller symptombegrænsende angina, hjertesvigt forværringer på trods af maksimal medicinsk behandling, ventrikulære arytmier eller har en signifikant koronararteriestenose, hvor tilstedeværelsen af selv en lille ø levedygtigt myokardium sandsynligvis vil svinge beslutningen til fordel for revaskularisering. Hos patienter med nyresvigt eller en implanteret hjerteanordning foretrækkes PET. Hos patienter med dårligt kontrolleret diabetes, alvorligt reduceret udstødningsfraktion med slutdiastolisk tykkelse mindre end 6 mm eller dem med stenose i multipel koronararteriefordeling, bør PET undgås i svær klaustrofobi, nyresvigt eller tilstedeværelse af implanterede enheder, brugen af CMR er begrænset og/eller kontraindiceret.
- Murray CJ, Lopes AD. Alternative fremskrivninger af dødelighed og handicap efter årsag. 1990-2020: global undersøgelse af sygdomsbyrde. Lancet 1997; 349: 1498-504.
- Maurer G, Lee KL, et al. Myokardiel levedygtighed og overlevelse ved iskæmisk venstre ventrikulær dysfunktion. N Engl J Med 2011;364: 1617-25.
- Pansa JA, Ellis AM, Al-Khalidi HR, et al. Myokardiel levedygtighed og langsigtede resultater i iskæmisk kardiomyopati. N Engl J Med 2019;381: 739-8.
- Garcia MJ, ku RY, Scherrer-Crosbie M, et al. State of the art: billeddannelse for myokardiel levedygtighed: en videnskabelig erklæring fra American Heart Association. Circ Cardiovasc Imaging 2020; Jul 13:.
- Bolli R. grundlæggende og kliniske aspekter af myokardie bedøvelse. Prog Cardiovasc Dis 1998; 40: 477-516.
- Ryan MJ, Perera D. identificering og styring af hibernating myocardium: hvad er nyt, og hvad forbliver ukendt? Curr Hjertesvigt Rep 2018; 15:214-23.
- Canty Jm Jr, Susuki G, Banas MD, Verheyen F, Borgers M, Fallavollita JA. Hibernating myocardium: kronisk tilpasset iskæmi, men sårbar over for pludselig død. Circ Res 2004; 94: 1142-9.
- Hernandes-Pampaloni M, Peral V, Carreras JL, Sanches-Harguindey L, Vilacosta I. bifasisk respons på dobutamin forudsiger forbedring af venstre ventrikulær dysfunktion efter revaskularisering: korrelation med positron emission og rest-omfordeling 201tl tomografier. Int J Cardiovasc Imaging 2003;19:519-28.
- Porter TR, Mulvagh SL, Abdelmoneim SS, et al. Kliniske anvendelser af ultralydsforbedrende midler i ekkokardiografi: 2018 American Society of Echocardiography guidelines update. J Am Soc Ekkokardiogr 2018; 31: 241-74.
- ormene D, Chiu ML, Kronauge JF. Divergerende kinetik af 201Tl og 99mTc-SESTAMIBI i dyrkede chick ventrikulære myocytter under ATP-udtømning. Cirkulation 1992; 85:1531-41.
- Berman DS, Kiat H, Van Train KF, Friedman J, Garcia EV, Maddahi J. sammenligning af SPECT ved hjælp af technetium-99m-midler og thallium-201 og PET til vurdering af myokardieperfusion og levedygtighed. Am J Cardiol 1990; 66: 72E-79E.
- L liter AI, Kramer CM. Myokardiel levedygtighedstest for at guide koronar revaskularisering. Interv Cardiol Clin 2018; 7: 355-65.
- Kim RJ, vi E, Rafael A, et al. Anvendelsen af kontrastforstærket magnetisk resonansbilleddannelse til at identificere reversibel myokardisk dysfunktion. N Engl J Med 2000; 343: 1445-53.
- Poldermans D, Elhendy A, Boersma E, Rahimtoola SH. Følsomhed, specificitet og forudsigelige nøjagtigheder af forskellige ikke-invasive teknikker til påvisning af dvale myokardium. Curr Probl Cardiol 2001; 26: 147-186.
- JJ, van Der væg EE, Harbinson M. radionuklid teknikker til vurdering af myocardial levedygtighed og dvale. Hjerte 2004; 90: v26-v33.
- Pagano D, Bonser R, Byen J, Ordoubadi F, Lorenoni R, Camici P. Prædiktiv værdi af dobutamin ekkokardiografi og positronemissionstomografi til identifikation af dvaletilstand myokardium hos patienter med postiskæmisk hjertesvigt. Hjerte 1998; 79:281-8.
- Beanlands RSB, Nichol G, Hussti E, et al. F-18-fluortiltglucose positronemissionstomografi billedbehandling-assisteret behandling af patienter med svær venstre ventrikulær dysfunktion og mistanke om koronar sygdom: et randomiseret, kontrolleret forsøg (PARR-2). J Am Coll Cardiol 2007; 50: 2002-12.
kliniske emner: Arytmier og klinisk EP, Diabetes og kardiometabolisk sygdom, dyslipidæmi, hjertesvigt og kardiomyopatier, ikke-invasiv billeddannelse, implanterbare enheder, SCD/ventrikulære arytmier, atrieflimren/supraventrikulære arytmier, lipidmetabolisme, nye stoffer, computertomografi, ekkokardiografi/ultralyd, nuklear billeddannelse
nøgleord: Dyslipidemias, Apoptosis, Arrhythmias, Cardiac, Biological Phenomena, Atherosclerosis, Ammonia, Cardiomyopathies, Cicatrix, Cardiovascular Diseases, Constriction, Pathologic, Contrast Media, Coronary Vessels, Death, Sudden, Cardiac, Dobutamine, Down-Regulation, Echocardiography, Echocardiography, Stress, Extracellular Space, Fatty Acids, Fluorodeoxyglucose F18, Gadolinium, Glucose, Hemodynamics, Hibernation, Hospitalization, Inflammation, Insulin Resistance, Myocardial Ischemia, Ischemia, Multimodal Imaging, Myocardium, Myocytes, Cardiac, Plaque, Atherosclerotic, Positron-Emission Tomography, Prognose, kalium, livskvalitet, reproducerbarhed af resultater, risikofaktorer, Rubidium, Rubidium radioisotoper, slagvolumen, Technetium, Thallium, trombose, tomografi, Emission-beregnet, ventrikulær funktion, venstre
< tilbage til lister