Seuraava: 6.6 entropia ja poissa käytöstä: 6. Edellisen: 6.4 Brayton Cycle in Contents Index
Consider a system in contact with a heat reservoir during areverable process. Jos lämpö ![]() absorboi tereservoirin lämpötilassa
absorboi tereservoirin lämpötilassa ![]() , säiliön entropian muutos
, säiliön entropian muutos ![]() . Yleensä palautuvia prosesseja täydentävät lämmönvaihdot, jotka tapahtuvat eri temperatures.To analysoi nämä, voimme visualisoida sarjan lämpövarastoja eri lämpötiloissa niin, että aikana tahansa äärettömän pieni osa syklin ei ole mitään lämpöä siirretään yli rajallinen lämpötilaero.
. Yleensä palautuvia prosesseja täydentävät lämmönvaihdot, jotka tapahtuvat eri temperatures.To analysoi nämä, voimme visualisoida sarjan lämpövarastoja eri lämpötiloissa niin, että aikana tahansa äärettömän pieni osa syklin ei ole mitään lämpöä siirretään yli rajallinen lämpötilaero.
minkä tahansa äärettömän pienen osan aikana lämpö ![]() siirtyy järjestelmän ja yhden reservin välillä, joka on
siirtyy järjestelmän ja yhden reservin välillä, joka on![]() . Jos
. Jos ![]() absorboituu systeemiin, järjestelmän entropychange on
absorboituu systeemiin, järjestelmän entropychange on
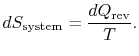
säiliön entropiamuutos on
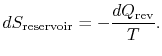
systeemin ja ympäristön entropiamuutos on
tämä pätee myös, jos on olemassa tietty määrä lämpöä, jonka järjestelmä hylkää.
johtopäätös on, että palautuvassa prosessissa ei tapahdu muutosta tuotetun entropian kokonaisuudessa, ts.systeemin entropiassa ja ympäristön entropiassa: ![]() .
.
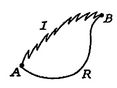
teemme nyt samantyyppisen analyysin peruuttamattomalle prosessille, joka vie järjestelmän samojen määrättyjen valtioiden välillä kuin palautuvassa prosessissa. Tämä on esitetty kaavamaisesti inFigure 6.7, jossa ![]() ja
ja![]() tarkoittavat peruuttamattomia ja palautuvia prosesseja. Niiden käänteisessä prosessissa järjestelmä vastaanottaa lämpöä
tarkoittavat peruuttamattomia ja palautuvia prosesseja. Niiden käänteisessä prosessissa järjestelmä vastaanottaa lämpöä ![]() ja toimii
ja toimii![]() . Peruuttamattoman prosessin sisäenergian muutos on
. Peruuttamattoman prosessin sisäenergian muutos on
palautuvalle prosessille
koska tilan muutos on sama näissä kahdessa prosessissa (wespecified that it was), muutos sisäenergiassa on sama.Rinnastetaan sisäenergian muutokset edellä mainituilla kahdella ekspressiokentällä
alaindeksi ”actual” viittaa todelliseen prosessiin (joka on muuttumaton). Valtiomuutokseen liittyvä entropian muutoseis
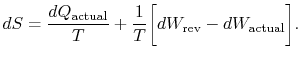 |
(6..3) |
jos prosessi ei ole palautuva, saamme vähemmän työtä (katso IAWnotes) kuin palautuvassa prosessissa,![]() , joten peruuttamattomassa prosessissa,
, joten peruuttamattomassa prosessissa,
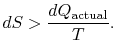
entropiamuutoksen![]() ja thequantyn
ja thequantyn![]() välillä ei ole tasa-arvoa peruuttamattomalle prosessille. Tasa-arvoa voidaan soveltaa vain käännettävään prosessiin.
välillä ei ole tasa-arvoa peruuttamattomalle prosessille. Tasa-arvoa voidaan soveltaa vain käännettävään prosessiin.
minkä tahansa prosessin entropian muutos, joka johtaa alkutilan `a” ja lopputilan`b” väliseen transformaatioon, on siis
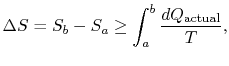
missä![]() on aktuaalisessa prosessissa vaihdettu lämpö. Tasa-arvo koskee vain käännettävää prosessia.
on aktuaalisessa prosessissa vaihdettu lämpö. Tasa-arvo koskee vain käännettävää prosessia.
ero ![]() edustaa työtä, jonka olisimme voineet saada, mutta emme saaneet. Sitä kutsutaan kadonneeksi työksi ja merkitään
edustaa työtä, jonka olisimme voineet saada, mutta emme saaneet. Sitä kutsutaan kadonneeksi työksi ja merkitään ![]() . Tämän määrän osalta voimme kirjoittaa,
. Tämän määrän osalta voimme kirjoittaa,
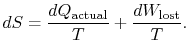 |
(6..4) |
yhtälön (6.4) sisältö on, ettäjärjestelmän entropiaa voidaan muuttaa kahdella tavalla: (i) heatexchangen ja (ii) peruuttamattomuuden kautta. Kadonnut työ (![]() yhtälössä (6.4)) on aina suurempi kuin nolla, joten systeemin entropiaa voi pienentää vain lämmönsiirron avulla.
yhtälössä (6.4)) on aina suurempi kuin nolla, joten systeemin entropiaa voi pienentää vain lämmönsiirron avulla.
toisen lain soveltamiseksi tarkastelemme kokonais entropiamuutosta (systemplus-ympäristö). Jos ympäristö on säiliö attemperature ![]() , jonka kanssa järjestelmä vaihtaa lämpöä,
, jonka kanssa järjestelmä vaihtaa lämpöä,

entropian kokonaismuutos on
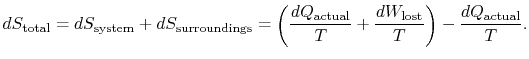
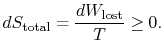
Suure (![]() ) on entropia, joka syntyy siirrettävyyden vuoksi.
) on entropia, joka syntyy siirrettävyyden vuoksi.
vielä yksi tapa todeta tekemämme ero on
| (6..5) |
kadonnutta teosta kutsutaan myös hajaannukseksi ja huomataan![]() . Käyttämällä tätä merkintää, systeemin äärettömän pieni entropiamuutos:
. Käyttämällä tätä merkintää, systeemin äärettömän pieni entropiamuutos:
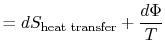 |
||
| tai | ||
yhtälö (6.5) voidaan kirjoittaa myös araattiyhtälönä,
 |
(6..6) |
joko yhtälön (6.5) tai(6.6) voidaan tulkita merkitsevän sitä, että systeemin antropiaan,![]() , vaikuttaa kaksi tekijää: lämmön virtaus
, vaikuttaa kaksi tekijää: lämmön virtaus![]() ja ylimääräisen entropian ilmaantuminen, jota merkitään
ja ylimääräisen entropian ilmaantuminen, jota merkitään![]() , johtuen peruuttamattomuudesta 6.1. Tämä ylimääräinen entropia on nolla, kun prosessi on palautuva ja aina positiivinen, kun prosessi on muuttumaton. Näin voidaan sanoa, että järjestelmä kehittääresurssit, jotka luovat entropiaa peruuttamattoman prosessin aikana.Toisen lain mukaan entropian nielut ovat mahdottomia luonteeltaan, mikä on graafisempi tapa sanoa, että
, johtuen peruuttamattomuudesta 6.1. Tämä ylimääräinen entropia on nolla, kun prosessi on palautuva ja aina positiivinen, kun prosessi on muuttumaton. Näin voidaan sanoa, että järjestelmä kehittääresurssit, jotka luovat entropiaa peruuttamattoman prosessin aikana.Toisen lain mukaan entropian nielut ovat mahdottomia luonteeltaan, mikä on graafisempi tapa sanoa, että![]() ja
ja![]() ovat positiivisia definiittejä(aina suurempia kuin nolla), tai nollia kääntymättömien prosessien erikoistapauksessa.
ovat positiivisia definiittejä(aina suurempia kuin nolla), tai nollia kääntymättömien prosessien erikoistapauksessa.
termi
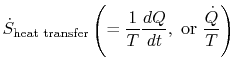
, joka liittyy lämmönsiirtoon systeemiin, voidaan tulkita entropian vuoksi. Rajan ylittää lämpö ja tämän lämpövuon suhde lämpötilaan voidaan määritellä entropian afluxiksi. Ei ole rajoituksia merkki tämänquantity, ja voimme sanoa, että tämä vuo joko edistää, tai valuu pois, järjestelmän entropia. Palautuvan prosessin aikana vain tämä vuo voi vaikuttaa systeemin entropiaan. Thisterminology ehdottaa, että tulkitsemme entropian eräänlaiseksi painottomaksi nesteeksi, jonka määrä säilyy (kuten aineen määrä)palautuvan prosessin aikana. Peruuttamattoman prosessin aikana tämä neste ei kuitenkaan säily; se ei voi kadota, vaan sitä syntyy kaikkialla järjestelmässä olevista lähteistä. Vaikka tätä tulkintaa ei pidä ottaa liian kirjaimellisesti, se tarjoaa helpon ilmaisutavan ja on samassa kategoriassa käsitteitä, kuten ne, jotka liittyvät lauseisiin ”energian vuo” tai ” lämmönlähteet.”Esimerkiksi virtausmekaniikassa tämä graafinen kieli on erittäin tehokas, eikä sen intermodynamiikan kopioimista pitäisi vastustaa.
Muddy Points
nähdäänkö entropialle koskaan absoluuttista muuttujaa? Toistaiseksi olemme työskennelleet vain deltojen kanssa (MP 6.8)
olen hämmentynyt siitä, että ![]() , kun taas
, kun taas ![]() .(MP 6.9)
.(MP 6.9)
peruuttamattomille prosesseille, miten voidaan laskea ![]() , jos ei ole sama kuin
, jos ei ole sama kuin ![]() ?(MP 6.10)
?(MP 6.10)
Seuraava: 6.6 entropia ja poissa käytöstä: 6. Edellisen Sovellukset: 6.4 Brayton Cycle in Contents Index
UnifiedTP